-
(12分)二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
请回答下列问题:
⑴ 煤的气化的主要化学反应方程式为:___________________________。
⑵ 煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为:________________________________________。
⑶ 利用水煤气合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)  CH3OH(g);ΔH = -90.8 kJ·mol-1
CH3OH(g);ΔH = -90.8 kJ·mol-1
② 2CH3OH(g)  CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
③ CO(g) + H2O(g)  CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g)  CH3OCH3(g) + CO2 (g) ΔH=-246.4kJ· mol -1;
CH3OCH3(g) + CO2 (g) ΔH=-246.4kJ· mol -1;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是_______(填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
⑷ 已知反应②2CH3OH(g)  CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
① 比较此时正、逆反应速率的大小:v正 ______ v逆 (填“>”、“<”或“=”)。
② 若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) = _________;该时间内反应速率v(CH3OH) = __________。
-
二氟甲烷是性能优异的环保产品,它可替代某些会破坏臭氧层的“氟利昂”产品,用作空调、冰箱和冰冻库等中的制冷剂。试判断二氟甲烷的结构简式
A.有4种 B.有3种 C.有2种 D.只有1种
-
化学与生产生活、环境保护、资源利用密切相关。下列做法不正确的是
A.用工业废水直接灌溉农田 B.用可降解塑料做购物袋
C.将煤气化或液化获得清洁燃料 D.火力发电厂的燃煤中加适量石灰石
-
(15分)二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为________。
A.加入某物质作催化剂 B.加入一定量CO
C.反应温度降低 D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为________;若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a=________mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)的△H=________;830℃时反应③的K=1.0,则在催化反应室中反应③的K________1.0(填“>”、“<”或“=”)。
CH3OCH3(g)+CO2(g)的△H=________;830℃时反应③的K=1.0,则在催化反应室中反应③的K________1.0(填“>”、“<”或“=”)。
(4)二甲醚的燃烧热为1455 kJ·mol-1,则二甲醚燃烧的热化学方程式为
________。

(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。b电极是________极,写出a电极上发生的电极反应式________。
-
下列关于化石燃料的加工说法正确的是( )
A.煤的气化和液化是物理变化,是高效、清洁地利用煤的重要途径
B.石油分馏是化学变化,可得到汽油、煤油、柴油等
C.石蜡油高温分解的产物中含有烷烃和烯烃
D.石油催化裂化主要得到乙烯
-
下列关于几种常见物质对人类主要“功与过”的分析,正确的是 ( )
A. 二氧化碳→光合作用的原料→大量排放导致酸雨
B. 氟利昂→制冷剂→向空气中排放导致臭氧空洞
C. 二氧化硫→工业制硫酸→大量排放导致光化学烟雾
D. 氮的氧化物→工业制氨气→大量排放导致温室效应
-
寻找清洁能源一直是化学家努力的方向,下列关于能源的说法错误的是
A. 氢气热值高,其燃烧产物是水,是一种理想的清洁燃料
B. 利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境
C. 煤的气化技术在一定程度上实现了煤的高效、清洁利用
D. 天然气、液化石油气、沼气属于一级能源
-
(12分)煤、天然气是社会生产、生活中重要的能源。
(1)工业上常把煤进行气化和液化处理,使煤变成清洁能源.煤气化和液化流程示意图如下:
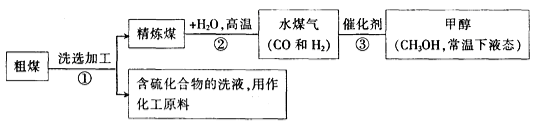
①已知H2、CO和CH3OH的燃烧热△H分别为-285.8kJ·mol-1、-283.0kJ·mol-1和-726.5kJ·mol-1。写出由CO和H2合成甲醇的热化学方程式_________________
②煤进行气化和液化的优点是
(2) 天然气催化重整也可生成CO和H2
①500℃,向一体积可变的密闭容器中充入一定量CH4和水蒸气进行催化重整, 下列能说明反应一定处于平衡状态的是
A.混合气体的密度不随时间变化
B.CO和H2的体积分数之比不随时间变化
C.v正(CH4)=3v逆(H2)
D.混合气体的平均相对分子质量不随时间变化
②CO和H2可用作燃料电池。一种熔融碳酸盐燃料电池原理示意如图:
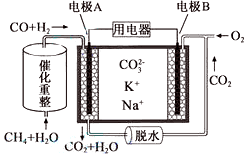
写出A电极反应式__________________
(3)CO一旦泄露会造成污染,环保检测中,有害气体的浓度常用1L有害气体的毫克值(mg/L)来表示,如对某气体样品中所含一氧化碳的浓度进行测定,其方法和实验步骤如下:
①首先将2.00L的气体样品通过盛有I2O5固体的加热管,反应后生成CO2和I2;
②用30.0mL 5.00×10-3mol/L的硫代硫酸钠溶液恰好吸收所产生的碘,发生的反应为:I2+2S2O32-=2I-+S4O62-
则样品中CO的浓度为
-
下列说法中不正确的是( )
A.与煤、石油相比较,天然气是一种比较清洁的化石燃料
B.乙醇是一种可再生能源,作为燃料的优点是完全燃烧的产物不污染环境
C.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量
D.煤转化为水煤气再燃烧放出的热量不会增加,因此煤的气化毫无意义
-
下列说法中不正确的是
A.与煤油、柴油相比较,天然气是一种比较清洁的化石燃料
B.乙醇是一种可再生能源,作为燃料的优点的是完全燃烧的产物不污染环境
C.利用太阳能、风能和氢能等能源替代化石能源能有效改善空气质量
D.煤的气化和液化不仅可以获得洁净燃料,而且再燃烧会放出更多的热量
CH3OH(g);ΔH = -90.8 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH= -23.5 kJ·mol-1
CO2(g) + H2(g);ΔH= -41.3 kJ·mol-1
CH3OCH3(g) + CO2 (g) ΔH=-246.4kJ· mol -1;
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:


