-
三氯氧磷(化学式:POCl3)无色透明的带刺激性臭味的液体,熔点1.25℃、沸点1.5℃,在潮湿空气中剧烈发烟,易与水反应。常用作半导体掺杂剂及光导纤维原料。工业上,“氯化水解法”生产三氯氧磷的方法一般是将三氯化磷加入反应釜中,通入氯气,同时滴加水,控制氯水比在3.94左右,并控制氯气和水的通入速率,其流程如下:
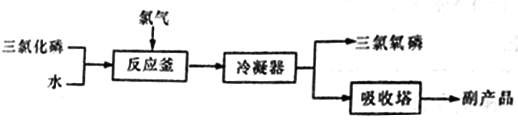
(1)在反应釜中将原料加热至105~109℃,“氯化水解法”生产三氯氧磷的化学方程式为___________。
(2)冷凝得到的粗三氯氧磷—般含有PCl3、H3PO3、PCl5和_________(填化学式)等杂质,进一步精制的方法是____________。
(3)已知H3PO3是—种易溶于水的二元弱酸。
①若将20 mL溶液与60 mL NaOH溶液等浓度混合并充分反应,化学方程式为______________。
②往废水中加入适量漂白粉并调节pH呈酸性,可将磷元素转化为磷酸钙沉淀回收,写出将H3PO3转化为磷酸钙的离子方程式:_____________________。
③经上述方法处理后的废水中c(PO43-) = 4×l0-7mol·L-1,溶液中c(Ca2+) =________mol·L-1。
(已知 Ksp[Ca3(PO4)2] = 2×10-29)
(4)工业上,还可以以三氯化磷为原料通过“氧气直接氧化法”制备三氯氧磷。从原理上看,与“氯化水解法”相比,该方法的优点是_______________________。(写出两点)
-
三氯氧磷(POCl3)是一种工业化工原料。无色透明的带刺激性臭味的液体,在潮湿空气中剧烈发烟。某化学小组采用PCl3氧化法制备POCl3。已知: POCl3的熔点为-112℃,沸点为75.5℃。在潮湿空气中二者均极易水解面剧烈“发烟”。回答下列问题:
I.制备PCl3
(1)实验室用高锰酸钾和浓盐酸反应制取氯气。发生装置可以选择图中的_____(填字母代号)。
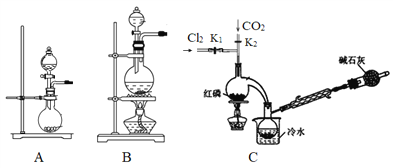
(2)检查装置气密性并装入药品后,先关闭K1,打开K2通入干燥的CO2,一段时间后, 关闭K2,加热曲颈瓶同时打开K1通入干燥氯气,反应立即进行。通干燥CO2的作用是_______。
II.制备POCl3(如图)
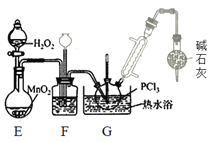
(3)盛放碱石灰的仪器的作用是________,装置G中发生反应的化学方程式为________ 。
(4) 装置F的作用除观察O2的流速之外,还有________。
III.测定POCl3含量
实验制得的POCl3中常含有PCl3杂质,通过下面方法可测定产品的纯度:
①快速称取5.000g产品,加水反应后配成250mL溶液;
②取以上溶液25. 00mL,向其中加入10. 00mL 0.1000mol/L碘水(足量),充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3溶液滴定;
④重复②、③操作,平均消耗0.1000mol/LNa2S2O3溶液8.00mL.
已知: H3PO3+I2+H2O==H3PO4+2HI,I2+2Na2S2O3==2NaI+Na2S4O6.
(5)滴定终点的现象为__________。该产品的纯度为________。
(6)若滴定管在滴定前无气泡,滴定后有气泡,则测定结果______(填“偏高”“偏低” 或“不变”)。
-
硫酰氯( SO2Cl2)是无色有刺激性气味的液体,熔点为-54.1℃,沸点为69℃,在潮湿空气中易“发烟”。实验室利用SO2(g)和Cl2(g)合成硫酰氯的实验装置如下图所示(部分夹持装置已省略):
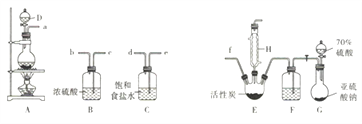
回答下列问题:
(1)实验室制备干燥纯净的氯气可以用A、B、C 装置来完成,请连接装置接口:a→___,____→___,______→f(按气流流动方尚;用小写学母表示)。
(2)实验过程中,使用分液漏斗滴加浓硫酸的操作是_____________。
(3)装置C的作用是____________;装置B 和F中浓硫酸起到的作用是①____________;②可观察到____________(填现象)来反映通入气体的速率,利用反应液滴加的快慢对气体通入速率加以控制,从而使通入反应器的SO2 和Cl2 达到最佳反应比例。
(4)该装置存在明显的缺陷,请指出:________________。
(5)已知该法合成硫酰氯为可逆反应,每生成2.7 g硫酰氯放出热量1940 J,写出该反应的热化学方程式: ________________。
-
硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。
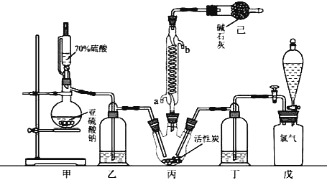
回答下列问题:
(1)装置己的作用是_________________________________________________;如何控制两种反应物体积相等:__________________________________________________。
(2)装置戊上方分液漏斗中最好选用下列试剂:_____(选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫会发生副反应,化学方程式是________________________________________________________;同时生成的SO2Cl2也会水解而“发烟”,该反应的化学方程式为______________________________________
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有(填序号)______。
①控制气流速率,宜慢不宜快 ②持续加热丙装置
③若丙装置发烫,可适当降温 ④先通冷凝水,再通气
(5)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H SO2Cl2 + H2SO4,分离两种产物的方法是__________(选填字母)。
SO2Cl2 + H2SO4,分离两种产物的方法是__________(选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
请设计实验方案检验产物中存在硫酸(可选试剂:稀盐酸、稀硝酸、氯化钡溶液、蒸馏水、石蕊试液)_______________________________________________________________________。
-
硫酰氯 可用作杀虫剂,通常条件下为无色液体,熔点为
可用作杀虫剂,通常条件下为无色液体,熔点为 ,沸点为
,沸点为 。在潮湿空气中“发烟”;
。在潮湿空气中“发烟”; 以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
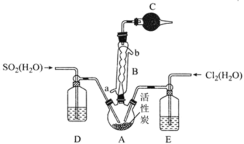
 ,所用装置如图所示。下列叙述错误的是
,所用装置如图所示。下列叙述错误的是

A.球形冷凝管B应从a口进水b口出水
B.可通过观察D和E中气泡产生速率控制通入A中的 和
和 的体积比
的体积比
C.仪器C,D,E中盛放的试剂依次为无水氯化钙、浓硫酸、浓硫酸
D.长期放置的硫酰氯液体会发黄的原因是溶解了氯气
-
硫酰氯 可用作杀虫剂,通常条件下为无色液体,熔点为
可用作杀虫剂,通常条件下为无色液体,熔点为 ,沸点为
,沸点为 。在潮湿空气中“发烟”;
。在潮湿空气中“发烟”; 以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
 ,所用装置如图所示。下列叙述错误的是
,所用装置如图所示。下列叙述错误的是

A.球形冷凝管B应从a口进水b口出水
B.可通过观察D和E中气泡产生速率控制通入A中的 和
和 的体积比
的体积比
C.仪器C,D,E中盛放的试剂依次为无水氯化钙、浓硫酸、浓硫酸
D.长期放置的硫酰氯液体会发黄的原因是溶解了氯气
-
硫酰氯 可用作杀虫剂,通常条件下为无色液体,熔点为
可用作杀虫剂,通常条件下为无色液体,熔点为 ,沸点为
,沸点为 。在潮湿空气中“发烟”;
。在潮湿空气中“发烟”; 以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
以上开始分解,生成二氧化硫和氯气,长期放置也可分解,制备时以活性炭为催化剂,反应的热化学方程式为
 ,所用装置如图所示。下列叙述错误的是
,所用装置如图所示。下列叙述错误的是
A.球形冷凝管B应从a口进水b口出水
B.可通过观察D和E中气泡产生速率控制通入A中的 和
和 的体积比
的体积比
C.仪器C,D,E中盛放的试剂依次为无水氯化钙、浓硫酸、浓硫酸
D.长期放置的硫酰氯液体会发黄的原因是溶解了氯气
-
硫酰氯( )是一种重要的化工试剂,实验室合成硫酰氯的实验装置如下图所示:
)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如下图所示:
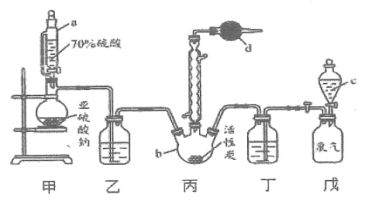
已知:① ,
,
②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
(1)仪器c的名称为_____,与c相比,仪器a的优点是__________。
(2)装置乙和丁中所装的试剂为_________________。
(3)球形冷凝管的作用___________________。
A.导气、冷凝回流 B.有利于平衡正向移动 C.防倒吸
(4)仪器d的作用为______________________。
(5)氯磺酸( )加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________________________。
)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________________________。
(6)当装置戊中排出氯气 (已折算成标准状况)时,最终得到
(已折算成标准状况)时,最终得到 纯净的硫酰氯,则硫酰氯的产率为____________。(保留三位有效数字)
纯净的硫酰氯,则硫酰氯的产率为____________。(保留三位有效数字)
(7)长期存放的硫酰氯会发黄,其原因可能为___________________。
-
硫酰氯(SO2Cl2)是一种化工原料,有如下有关信息:
常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气。氯化法是合成硫酰氯的常用方法,实验室合成反应和实验装置如下:
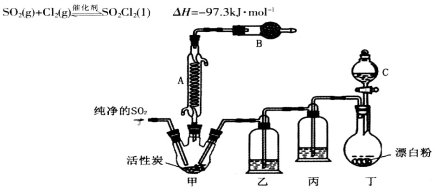
回答下列问题:
(1)仪器A的名称为______,甲中活性炭的作用是______,B中加入的药品是______。实验时从仪器C中放出溶液的操作方法是________。
(2)装置丁中发生反应的离子方程式为___________。用亚硫酸钠固体和浓硫酸制备二氧化硫气体时,如要控制反应速度,下图中可选用的发生装置是________(填写字母)。
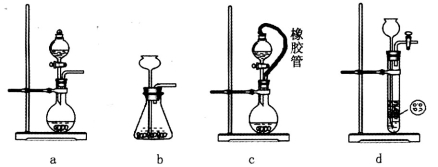
(3)氯磺酸(C1SO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________________,分离产物的方法是_________。
(4)若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为_______。为提高本实验中硫酰氯的产率,在实验操作中还需要注意的事项有(只答一条即可)_______。
-
硫酰氯(SO2Cl2)是一种化工原料,有如下有关信息:
常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气。氯化法是合成硫酰氯的常用方法,已知:SO2(g)+Cl2(g) SO2Cl2(l) △H=﹣97.3kJ/mol,实验室合成反应和实验装置如图所示:
SO2Cl2(l) △H=﹣97.3kJ/mol,实验室合成反应和实验装置如图所示:
回答下列问题:
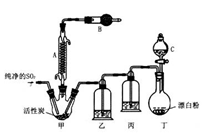
(1)仪器A的名称为_________,活性炭的作用是 B中加入的药品是_________。实验时从仪器C中放出溶液的操作方法是_________ 。
(2)装置丁中发生反应的离子方程式为_________ __。用亚硫酸钠固体和浓硫酸制备二氧化硫气体时,如要控制反应速度,下图中可选用的发生装置是________(填写字母)。

(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________________,分离产物的方法是_________。
(4)若缺少装置乙,氯气和二氧化硫可能发生反应的化学方程式为_____ 。为提高本实验中硫酰氯的产率,在实验操作中还需要注意的事项有(只答一条即可)_ 。












