-
(12分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质。
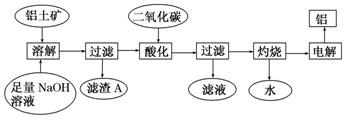
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式,滤渣A的主要成分为________。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是____
__________,通入过量的二氧化碳时,生成沉淀的离子方程式为_______________________。
(3)电解氧化铝,每生成1molAl时,生成________ g氧气。
-
(8分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质。
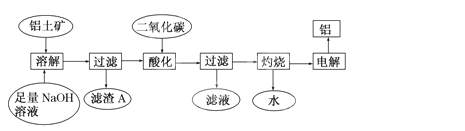
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式________,滤渣A的主要成分为________。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是____
__________,通入过量的二氧化碳时,生成沉淀的离子方程式为_______________________。
(3)电解氧化铝,每生成1molAl时,生成________ g氧气。
-
铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是从铝土矿中制备铝的工艺流程:

已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(1) 写出向铝土矿中加入足量氢氧化钠溶液操作中发生反应的离子方程式:__________________________;_____________________________。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂的原因是:_________。
(3)若将铝溶解,下列试剂中最好选用________(填编号)。理由是_________________。
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.浓硝酸
-
(14分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是从铝土矿中制备铝的工艺流程:
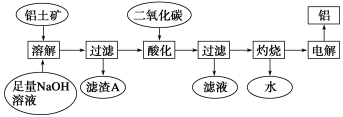
已知:①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
②除硅的方法:溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O===Na2Al2Si2O8↓+4NaOH。
回答下列问题:
(1)Al元素在元素周期表中的位置为 ;电解制取Al的化学反应中,反应物总能量 生成物总能量(填“大于”、“等于”或“小于”);二氧化碳的结构式为 。
(2)写出向Al2O3与氢氧化钠溶液发生反应的离子方程式 _____。
(3)滤渣A的主要成分为__________________________。
(4)在工艺流程第三步中,通入过量二氧化碳的化学反应方程式是_______________________。
(5)实验时取铝土矿ag,经过上述工艺流程最后得到bgAl,则铝土矿中的Al2O3质量分数为 。
A.=102b/54a B.>102b/54a C.<102b/54a D.均有可能
-
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:

已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为2Na2SiO3+2NaAlO2+2H2O===Na2Al2Si2O8↓+4NaOH。
请回答下列问题:
(1)铝土矿中Al2O3与氢氧化钠溶液反应的离子方程式为
________________________________________________________________________。
(2)在工艺流程中“酸化”时,加入的最佳物质B是______,理由是________________________________________________________________________,
写出酸化过程发生反应的化学方程式________________________________________________________________________。
(3)工业上用Al2O3与C、Cl2在高温条件下反应制取AlCl3,理论上每消耗6.0 g碳单质,转移1 mol电子,则反应的化学方程式为______________________________。
(4)某同学推测铝与氧化铁发生铝热反应得到的熔融物中还含有Fe2O3,设计了如下方案来验证:取一块该熔融物投入少量稀硫酸中,反应一段时间后,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色的变化,即可证明熔融物中是否含有Fe2O3。
则物质甲是________(填化学式),请判断该同学设计的实验方案的合理性________(填“合理”或“不合理”)。原因是_____________________________(若合理,则不用填写)。
-
金属铝质轻且有良好的防腐蚀性,在国防工业、生产、生活中具有非常重要
的作用。下图是从铝土矿中制备铝的工艺流程:
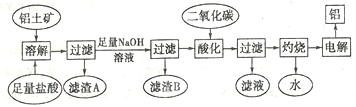
已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3、MgO杂质;回答下列问
题:
I、(1)铝土矿加入盐酸过滤后所得滤渣A的主要成分为____________。
(2)在工艺流程中,加入足量氢氧化钠溶液发生的离子反应共有_________个,其中发生沉淀溶解的离子反应方程式为____________。
(3)邋入过量的二氧化碳时,生成沉淀的离子方程式为____________。
(4)电解氧化铝,每生成1molA1时,生成____g氧气。
Ⅱ、测铝土矿组分的质量分数。
(1)若铝土矿样品质量为m,对滤渣A洗涤、干燥后称重为m1;对滤渣B洗涤、干燥、灼烧后称重为m2,该方案能测得质量分数的成份且相应的质量分数是____________;
(2)洗涤滤渣A后的洗涤液是否需加入到第一次过滤后的滤液中_____(“是”或“否”);检
测滤渣A是否洗涤干净的方法是____________。
-
铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是工业上从铝土矿(主要成分是Al2O3,含有少量SiO2、Fe2O3等杂质)中生产铝的工艺流程:
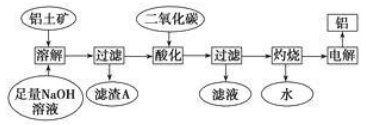
据此回答下列问题:
(1)电解制取铝的化学反应中,反应物的键能之和_____生成物的键能之和(填“大于”、“小于”或“等于”)。
(2)铝土矿中绝大部分成分都可以溶解在NaOH溶液中。请根据周期表对角线规则写出铍的氧化物与NaOH溶液反应的离子方程式:______________。
(3)滤渣A的主要成分____________。
(4)在工艺流程第三步中,通入过量二氧化碳所发生反应的化学方程式_______________。
(5)某同学在实验室模拟工业生产铝,称取ag铝土矿可制得bgAl(儇设每步反应进行完全),则铝土矿中Al2O3的质量分数为____________。
-
铝是应用广泛的金属,以铝土矿(主要成分为A12O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如图:
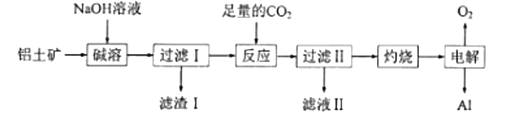
已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为__。
(2)“滤渣Ⅰ”的成分有___。
(3)向“过滤Ⅰ”所得滤液中通入足量的CO2,反应的离子方程式为___。
(4)“滤液Ⅱ”中加入足量的CaO,生成的__(填化学式)可循环利用。
(5)“灼烧”的化学方程式为___。
-
铝是一种重要金属,从铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)中冶炼Al的工业生产流程如下图:
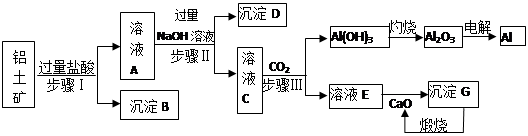
(1)沉淀B的化学式为________,溶液A中含的阳离子主要有________。
(2)写出步骤II生成溶液C 的离子方程式________,
步骤I、II、III都要用到的分离方法是________。
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有:________(填化学式)。
(4)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:
________
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)________(用含a、b的最简式表示)。
-
铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
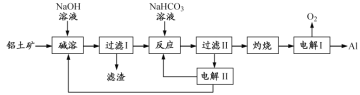
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________________________________________。
(2)“过滤Ⅰ”中所用到的玻璃仪器有___________________________________________。
(3)“过滤Ⅱ”中得到的固体中混有杂质,需要对沉淀进行洗涤,请你叙述如何洗涤?_______。









