-
已知有关热化学方程式为:
① 4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ/mol;
4NO(g)+6H2O(g) △H=-905kJ/mol;
② 3H2(g)+N2(g) 2NH3(g) △H=-92.4kJ/mol;
2NH3(g) △H=-92.4kJ/mol;
③ 2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol;
④ N2(g)+O2(g)=2NO(g) △H=QkJ/mol;
(1)Q=___________。
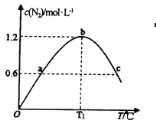
(2)向某密闭容器中充入amolNH3、bmolO2后,测得反应体系中某种量值X与压强P、温度T之间的变化如图1所示,图2表示温度为T2时,当容器为1L恒容密闭容器时,容器中NH3的平衡转化率与反应开始时两种反应物的投料之比(用M表示)的关系。
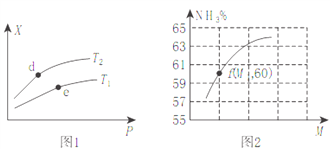
①若X表示NH3的百分含量,则T2_____T1(填>、<、无法确定);d、e两点的正反应的平衡常数K(d)_____K(e)。
②X还可以表示_____________。
a.混合气体的平均摩尔质量 b.NO的产率 c.△H值
③M=__________(用含a、b的式子表示,后同),若f点M=1.25,则此时O2的转化率为_________
(3)有科学家电解原理获得高产率的合成氨,则阴极上的电极反应式为(已知电解质能传递H+)_______________。
-
已知有关热化学方程式为:①4NH3(g)+5O2(g) 4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)
4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g) 2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H—O:463,H—N:391,O=O:497
2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H—O:463,H—N:391,O=O:497
(1)①Q=___________。
②NO中的化学键键能为_________kJ/mol。
(2)向某密闭容器中充入amolNH3、bmolO2后,测得反应体系中某种量值X与压强P、温度T之间的变化如图1所示,图2表示温度为T2时,当容器为1L恒容密闭容器时,容器中NH3的平衡转化率与反应开始时两种反应物的投料之比(用M表示)的关系。
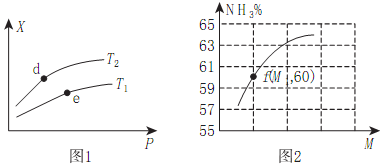
①若X表示NH3的百分含量,则T2_____T1(填>、<、无法确定);d、e两点的正反应的平衡常数K(d)_____K(e)。
②X还可以表示_____________。
A.混合气体的平均摩尔质量B.NO的产率C.△H值
③M=__________(用含a、b的式子表示,后同),若M1=1.25,则此时O2的转化率为__________%。
(3)有科学家电解原理获得高产率的合成氨,则阴极上的电极反应式为(已知电解质能传递H+)_______________。
-
(16分)(1)已知:①N2(g)+O2(g)=2NO(g); △H=+180.5 kJ·mol-1
②4NH3(g)+5O2(g)= 4NO(g)+6H2O(g);△H=-905 kJ·mol-1
③2H2(g)十O2(g)=2H2O(g):△H=-483.6 kJ·mol-1
则N2(g)+3H2(g) 2NH3(g)的△H=________。
2NH3(g)的△H=________。
(2)在一定条件下,将2mol N2与5mol H2混合于一个10 L的密闭容器中,反应情况如图1所示:
①求5min内的平均反应速率v(NH3)=________;②达到平衡时NH3的体积分数为________。

图1 图2 电解法合成氨装置
(3)近年来科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多品薄膜做电极,实现了高转化率的电解法合成氨(装置如图2)。钯电极A上发生的电极反应式是________。
(4)草酸(H2C2O4)是一种重要的化工原料。已知常温下0.01 mol·L-l的H2C2O4、KHC2O4、K2C2O4 溶液的pH如下表所示。
| H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.0 | 3.1 | 8.1 |
①用离子方程式表示KHC2O4呈酸性的原因:________
②取一定质量H2C2O4·2H2O和KHC2O4的混合物,加水溶解,配成250 mL溶液,取两份此溶液各25 mL,向第一份溶液中先加入几滴酚酞试液,再滴加0.25 mol·L-l NaOH溶液至20.00 mL时,溶液由无色变为浅红色;向第二份溶液中滴加适量3 mol·L-l H2SO4溶液酸化后,用0.10 mol·L-l KMnO4溶液滴定,当消耗KMnO4溶液16.00 mL时,溶液由无色变为浅紫红色。请回答下列问题:
a.完成离子方程式:________C2O42-+________MnO4-+________H+ =________CO2+________Mn2++________H2O。
b. 原混合物中H2C2O4·2H2O和KHC2O4的物质的量之比为__________。
-
(1)已知:
①N2(g)+O2(g)=2NO(g) △H1= +180.5 kJ•mol-1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H2=-905 kJ•mol-1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ•mol-1
请写出N2和H2在高温、高压、催化剂条件下生成NH3的热化学方程式________________。
(2)在一定温度下,某恒容密闭容器中,发生反应:2X(g)+Y(g) 2Z(g) △H<0,各物质的浓度随时间变化如图所示。
2Z(g) △H<0,各物质的浓度随时间变化如图所示。

①从反应开始到4min时平衡,Y的平均反应速率为____________________;
②根据图中数据,4min时的平衡常数K= ______________________;
③若使重新平衡时体系中c(X)=c(Z),则改变的条件为_____________________(只写一项)。
④若某时刻,V正(Y)=2V逆(Z),则反应_____达到平衡(填“已”或“未”)。
⑤图中a、b点对应的正反应速率大小关系为Va________Vb(填“大于”、“小于”或“等于”)。
-
氨的催化氧化过程主要有以下两个反应:
(ⅰ)4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.5 kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.5 kJ·mol-1
(ⅱ)4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=-1267 kJ·mol-1
2N2(g)+6H2O(g) ΔH=-1267 kJ·mol-1
测得温度对NO、N2产率的影响如图所示。下列说法错误的是( )
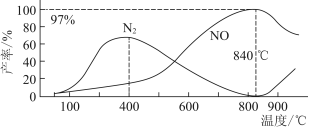
A.升高温度,反应(ⅰ)和(ⅱ)的平衡常数均减小
B.840 ℃后升高温度,反应(ⅰ)的正反应速率减小,反应(ⅱ)的正反应速率增大
C.900 ℃后,NO产率下降的主要原因是反应(ⅰ)平衡逆向移动
D.800 ℃左右时,氨的催化氧化主要按照(ⅰ)进行
-
已知:①4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH1=-905.5kJ·molˉ1
4NO(g)+6H2O(g) ΔH1=-905.5kJ·molˉ1
②N2(g)+O2(g) 2NO(g) ΔH2
2NO(g) ΔH2
一定条件下,NO可以与NH3反应转化为无害的物质,反应如下:
③4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH3=-1625.5 kJ·molˉ1。
4N2(g)+6H2O(g) ΔH3=-1625.5 kJ·molˉ1。

下列说法正确的是
A. 反应①使用催化剂,ΔH1减小
B. 反应②生成物总能量低于反应物总能量
C. 反应③一定能自发进行
D. 反应③达到平衡后升高温度,v(正)、v(逆)的变化如右图所示
-
一定条件下的密闭容器中: 4NH3(g)+5O2(g)⇌ 4NO(g)+6H2O(g),△H=-905.9kJ·mol-1, 下列叙述正确的是
A.4mol NH3和5mol O2反应, 达到平衡时放出热量为905.9kJ
B.平衡时v正(O2)=v逆(NO)
C.平衡后降低压强, 混合气体平均摩尔质量增大
D.平衡后升高温度, 混合气体中NO含量降低
-
一定条件下的密闭容器中:4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
4NO(g)+6H2O(g) ΔH=-905.9 kJ/mol,下列叙述正确的是( )
A.4 mol NH3和5 mol O2反应,达到平衡时放出的热量为905.9 kJ
B.平衡时v正(O2)= v逆(NO)
v逆(NO)
C.平衡后降低压强,混合气体平均摩尔质量增大
D.平衡后升高温度,混合气体中NO含量降低
-
利用氨气脱硝 除
除 是大气污染防治研究的热点,脱硝过程中涉及的反应为:
是大气污染防治研究的热点,脱硝过程中涉及的反应为:
主反应:
副反应:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905.5KJ/mol
②4NH3(g)+4O2(g)=2N2O(g)+6H2O(g) △H=-1104.9KJ/mol
③4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H=-1269.0KJ/mol
回答下列问题:
(1)主反应的△H为______
(2)如图所示,保持其它条件相同,使用两种不同的催化剂,主反应NO的转化率与温度关系如图所示:
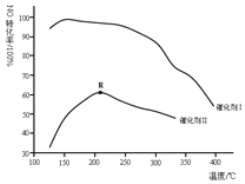
①选用催化剂I的优势有______ 写出一点
写出一点
②R点对应的温度为2100C,低于2100C,NO的转化率是不是对应温度下的平衡转化率,请作出判断并写出理由______.
(3)常温下,在通入氧气的条件下用 的NaOH溶液吸收NO也可实现脱硝
的NaOH溶液吸收NO也可实现脱硝 产物主要为
产物主要为 和
和 ,已知反应后溶液的
,已知反应后溶液的 ,溶液中
,溶液中 浓度为5.6×10-2mol/L,忽略反应过程中溶液体积变化,
浓度为5.6×10-2mol/L,忽略反应过程中溶液体积变化, 的电离平衡常数为5.1×10-4,则:
的电离平衡常数为5.1×10-4,则:
①c(NO2-)c(OH-)/c(HNO2)=______
②某溶液中c(NO2-)=1.0×10-6mol/L,取该溶液5mL,加入一滴 的硝酸银溶液
的硝酸银溶液 一滴为
一滴为 ,通过计算说明能否产生沉淀______[Ksp(AgNO2)=2×10-8]
,通过计算说明能否产生沉淀______[Ksp(AgNO2)=2×10-8]
-
氨作为重要化工原料,被大量应用于工业生产。氨在不同催化剂条件下可发生下列两个反应:
反应I:4NH3(g) +5O2(g)  4NO(g) +6H2O(g) △H=-905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=-905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)  2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
(1)写出NO分解生成N2与O2的热化学方程式:___________________________。
(2)反应I在容积固定的密闭容器中进行,容器内部分物质的物质的量浓度如下表:
| 时间 浓度 | c(NH3)/mol/Ll | c((O2)/mol/L | c(NO)/ mol/L |
| 第 0 min | 0.8 | 1.6 | 0 |
| 第 2 min | 0.3 | 0.975 | 0.5 |
| 第 3 niin | 0.3 | 0.975 | 0.5 |
| 第4 min | 0.7 | 1.475 | 0.1 |
①反应从开始到第2min时,v(H2O)=__________________。
②在第3 min时,改变的反应条件可能是_________(填选项字母)。
A.使用催化剂 B.臧小压强 C.升高温度 D.增加O2的浓度
③该反应达到平衡状态的标志是___________(填选项字母)。
A.在恒温恒容的容器中,混合气体的密度不再变化
B.单位时间内消耗n mol NO的同时消耗n mol NH3
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
(3)①若在容积为2L的密闭容器中充入8molNH3(g)和6molO2(g) ,发生反应II。保持其他条件不变,在相同时间内测得c(N2)与温度的关系如图所示。则T1℃下,NH3的平衡转化率为___。
②图中a、c两点对应的容器内部压强Pa____Pc(填“>”、“<”或“=”)
(4)氨气可用于生成硝酸铵化肥。25℃时,已知NH3·H2O的电离常数Kb=1.8×10-5,则硝酸铵在此温度下发生水解反应的平衡常数Kh=___________。
4NO(g)+6H2O(g) △H=-905kJ/mol;
2NH3(g) △H=-92.4kJ/mol;
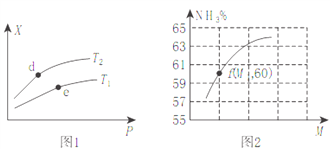






 2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1