-
以下是对重要金属及其化合物的讨论,根据要求回答问题:
(1)写出钠与水反应的离子方程式 ,Na2O2的用途之一是 。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是 ,
反应的离子方程式为 , 。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为 。
(4)刻蚀印刷电路板涉及的离子方程式为 ,检验Fe3+中混有Fe2+的试剂是 。
高一化学填空题中等难度题查看答案及解析
-
以下是对重要非金属及其化合物的讨论,根据要求回答问题:
(1)实验室盛装NaOH溶液是试剂瓶不能用玻璃塞,应该用橡胶塞,以防止发生反应:
(离子方程式)。
(2)氨是一种重要的化工产品,密度比空气 (填“大”或“小”)。工业上制备氨气的化学方程式为 。
(3)工业上制取漂白粉的反应化学方程式为 。
(4)浓H2SO4常用作气体干燥剂,是因为它具有____________;将适量的蔗糖放入烧杯中,滴入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
产生刺激性气味气体的化学方程式为 。
(5)铜和稀硝酸反应的离子方程式是 。若参加反应的Cu质量为6.4g,生成NO气体____________L(标准状况下),则转移电子物质的量为 mol,被还原的与未被还原的HNO3物质的量之比为 。
高一化学填空题中等难度题查看答案及解析
-
以下是对重要非金属及其化合物的讨论,根据要求回答问题:
(1)实验室盛装NaOH溶液的试剂瓶不能用玻璃塞,应该用橡胶塞,以防止发生反应: (离子方程式)。
(2)氨是一种重要的化工产品,密度比空气 (填“大”或“小”);工业上制备氨气的化学方程式为 。
(3)工业上制取漂白粉的化学反应方程式为 ;除去氯气中混有氯化氢的方法是将气体通入 溶液中。
(4)浓H2SO4常用作气体干燥剂,是因为它具有 ;将适量的蔗糖放入烧杯中,滴入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到 ;产生刺激性气味气体的化学方程式为 。
(5)铜和稀硝酸反应的离子方程式是 。若参加反应的Cu质量为6.4g,则转移电子物质的量为 mol。
高一化学填空题中等难度题查看答案及解析
-
以下是对重要非金属及其化合物的讨论,根据要求回答问题:
(1)实验室盛装NaOH溶液的试剂瓶不能用玻璃塞,应该用橡胶塞,以防止发生反应: (离子方程式);
(2)氨是一种重要的化工产品;实验室制备氨气的化学方程式为 ;
(3)工业上制取漂白粉的化学反应方程式为 ;除去氯气中混有氯化氢的方法是将气体通入 溶液中。
(4)浓H2SO4常用作气体干燥剂,是因为它具有 ;碳与浓硫酸反应的化学方程式为 。
(5)铜和稀硝酸反应的离子方程式是 。若参加反应的Cu质量为6.4g,则转移电子物质的量为 mol。
高一化学填空题困难题查看答案及解析
-
以下是对金属及其化合物的讨论,根据要求回答问题
(1)写出钠与水反应的离子方程式 。
(2)在AlCl3溶液中逐滴滴入过量的NaOH溶液,观察到的现象是 ,
反应的离子方程式为 , 。
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为 。
高一化学填空题中等难度题查看答案及解析
-
钠、氯及其化合物有如下转化关系,请按要求填空:
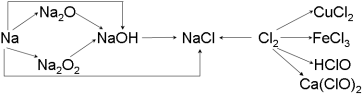
(1)金属钠的密度比水 ,实验室中金属钠通常保存
在 中。一小块金属钠投入水中的反应方程式是 。
(2)Na2O2 是
色的固体,Na2O2 的重要用途是 ,有关反应的化学方程式为 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为 。
(4)漂白粉的有效成份是 (填化学式),漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸,化学方程式为 。
高一化学填空题困难题查看答案及解析
-
钠、氯及其化合物有如下转化关系,请按要求填空:
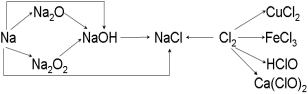
(1)金属钠的密度比水 ,实验室中金属钠通常保存在 中。一小块金属钠投入水中的反应方程式是 。
(2)Na2O2 是 色的固体,Na2O2 的重要用途是 ,有关反应的化学方程式为 ___________________。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为 。
(4)新制的氯水滴入AgNO3溶液中,观察到 现象,原因是 。
高一化学填空题中等难度题查看答案及解析
-
善于归纳元素及其化合物之间的转化关系,对学习元素化合物具有重要意义。回答下列问题:
(1)置换反应是中学常见基本反应类型之一。
①写出金属单质置换出非金属单质的离子反应方程式_____________;
②写出非金属单质置换出非金属单质的化学方程式_____________。
(2)“三角转化”是单质及其化合物之间相互转化中常见的转化关系之一。现有如图转化关系。
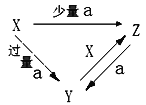
①若Z是一种能够与血红蛋白结合造成人体缺氧的气体。则a的名称为___________;
②若X是一种常见金属单质,a为一种含氧酸。Y转化为Z的离子方程式___________。
③若X是一种强碱,a是一种酸性氧化物。Z转化为Y的离子反应方程式____________;
(3)在下图的转化关系中,A、B、C、D、E为含有一种相同元素的五种物质。

①若A为淡黄色固体单质,则B→D的化学方程式为_____________;
②若A常温下为气体单质,收集气体B采用的方法为________;若将32 g铜投入稍过量的E的浓溶液中,产生气体的体积为11.2 L(STP),参加反应的硝酸的物质的量为_____;
高一化学综合题中等难度题查看答案及解析
-
某类化学反应可用如下通式表示:A+B→C+D+H2O 请按要求回答问题:
(1)若A、C、D中均含有氯元素,且A中的Cl的化合价介于C和D之间,写出该反应的离子方程式:______
(2)若A是紫红色金属,D为红棕色气体,写出该反应的化学方程式:______
(3)若C和D均为气体且都能使澄清的石灰水变浑浊,A呈固态,则B的化学式为______若产物D是还原产物,其化学式为______.
(4)若C是一种碱性气体,能使湿润的红色石蕊试纸变蓝,D是一种固体可作干燥剂(中性),则化学式依次为A(盐)______B______.高一化学解答题中等难度题查看答案及解析
-
物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:

(1)类比CO2的性质,学习SO2的性质,写出下列反应的离子方程式。
①少量的SO2通入澄清石灰水中:__________________。
②SO2通入Na2SO3溶液中: ________________________。
(2)Y的分子式:___________________。
(3)Z的稀溶液与铁反应的离子方程式为______________________。
(4)检验CO2是否混有SO2,可以使混合气体通过盛有品红溶液的洗气瓶,这是利用了SO2的_____________性,也可以使混合气体通过盛有酸性高锰酸钾稀溶液的洗气瓶,这是利用了SO2的_____________性。
(5)大苏打(Na2S2O3)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要用途。现欲在实验室制备大苏打,从氧化还原角度分析,合理的是__________(填字母选项)
A.Na2S+S B.Na2SO3+S C.Na2SO3+ Na2SO4 D.SO2+Na2SO4
(6)将X与SO2的水溶液混合后产生淡黄色沉淀,该反应的氧化产物与还原产物的质量之比为__________________
高一化学综合题中等难度题查看答案及解析