-
砷(33As)在元素周期表中与氮、磷同主族,其在自然界存在的主要化合物有砒霜(As2O3)、雄黄( As4S4)、雌黄(As2S3)等。
(1)砷在元素周期表中的位置为________。
(2)在一定条件下,雄黄(As4S4(雄黄中As元素化合价为+2)和雌黄As2S3之间的转化关系如图所示。
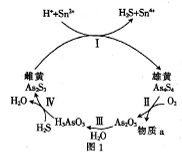
①H3AsO3中砷元素呈_______价;则在转化关系I中,被还原的元素名称是____________。
②反应Ⅱ中,若1mol As4S4参加反应时,转移12mole-,则物质a为______(填化学式);将As2O3(俗称砒霜)在高温下用焦炭还原可制备砷,同时产生一种无毒气体,写出用焦炭还原As2O3时的化学方程式:_________。
③在转化关系Ⅲ中,将As2O3溶于热水生成亚砷酸(H3AsO3),已知H3AsO3是两性偏酸性的化合物,Na3AsO3溶液呈碱性,原因是_________(用水解离子方程式表示)。
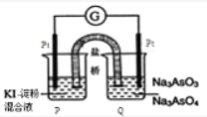
(3)某原电池装置如图,电池总反应为AsO43-+2I-+H2O AsO32-+I2+OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为___________。
AsO32-+I2+OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为___________。
-
希腊哲学家亚里士多德在其著作中记载了Arsenikon(雌黄),雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。
(1)雌黄和雄黄中均含有S元素。
①S在周期表中位于第_________周期_________族;
②S的最高价氧化物对应的水化物X的化学式为_________;
③在古特蔡特测砷法中,Na3AsO4溶液与Zn反应生成AsH3,该反应中Na3AsO4_________(填字母).
a.作氧化剂 b.作还原剂 c.既作氧化剂又作还原剂
(2)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,若As2S3和SnCl2恰好完全反应,则还原剂与还原产物的物质的量之比为_________;
(3)As2S3与足量浓硝酸发生反应,当生成48g S时,生成NO2的体积为112L(标准状况下),元素As在生成物中的化合价为_________(反应后的溶液中不含含硫微粒),该反应的化学方程式为:_________;
(4)雄黄在空气中加热至300℃时会 两种氧化物,其中之一一种氧化物为剧毒的砒霜(As2O3),另一种氧化物为_________(填化学式),可用双氧水将As2O3氧化为H3AsO4而除去,写出该反应的化学方程式:_________。
-
(14分)雄黄(AS4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生(其中的S元素均为—2价)。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为________。
(2)上述反应中的氧化剂是________,反应产生的气体可用________溶液[或CuSO4溶液]吸收。(均写化学式)
(3)As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为________。若将该反应设计成一原电池,则NO2应该在________(填“正极”或“负极”)附近逸出。酸性:HNO3________H3AsO4(填“>”、“=”或“<”)。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量________(选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
-
砷(As)及其化合物在生产、医疗、科技等方面有许多应用
(1)中国自古“信口雌黄”、“雄黄入药”之说。雄黄As2S3和雌黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图所示。
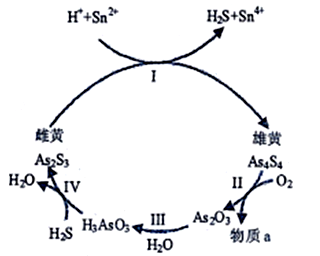
①砷元素有+2、+3+5等常见价态。,雌黄和雄黄中S元素的价态相同,其价态是______________。I中发生的离子方程式是______________________________。
②Ⅱ中,雄黄在空气中加热至300℃时会产生两种物质,若4.28g As4S4反应转移0.28mole-,则a为_______________(填化学式)砒霜(As2O3)可用双氧水将氧化成H3AsO4而除去,该反应的化学方程式为:____________________________________。
(2)AsH3是一种很强的还原剂,室温下, 0.4mol AsH3气体在空气中自燃,氧化产物为As2O3固体,放出b kJ 热量,AsH3自燃的热化学方程式是:____________________________________。
(3)将Na3AsO3(aq)+I2(aq)+H2O(l) Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
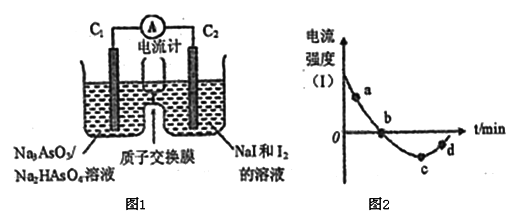
①如图中表示在该时刻上述可逆反应达到平衡状态的点是_________________(填字母)。
②已知:a点对应如图中电流由C1极经外电路流向C2极。则d点对应的负极的反应式为_____________。
③如图中,b→c改变条件可能是____________(填代号),c→d电流强度变化的原因是___________。
A.向左室中加入适量的浓Na3AsO3溶液 B.向左室中加入适量的烧碱溶液
C.向右室中加入适量的浓KI溶液 D. 向右室中加入适量的稀硫酸
-
砷(As)及其化合物在生产、医疗、科技等方面有许多应用
(1)中国自古“信口雌黄”、“雄黄入药”之说。雄黄As2S3和雌黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图所示。
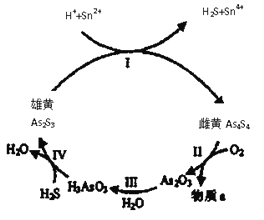
①雌黄和雄黄中S元素均为-2,I中发生的离子方程式是__________。
②Ⅱ中,雌黄在空气中加热至300℃时会产生两种物质,若4.28g As4S4反应转移0.28mole-,则a为__________(填化学式);砒霜(As2O3)可水将氧化成H3AsO4而除去,该反应的化学方程式为:__________。
(2)AsH3是一种很强的还原剂,室温下, 0.4mol AsH3气体在空气中自燃,氧化产物为As2O3固体,放出b kJ 热量,AsH3自燃的热化学方程式是:__________。
(3)将Na3AsO3(aq)+I2(aq)+H2O(l) Na2HAsO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
Na2HAsO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
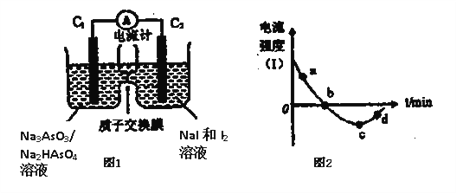
①如图中表示在该时刻上述可逆反应达到平衡状态的点是__________(填字母)。
②已知:a点对应如图中电流由C1极经外电路流向C2极。则d点对应的负极的反应式为__________。
③如图中,b→c改变条件可能是__________(填代号)。
A.向左室中加入适量的浓Na3AsO3溶液 B.向左室中加入适量的烧碱溶液
C.向右室中加入适量的浓KI溶液 D. 向右室中加入适量的稀硫酸
-
砷(As)及其化合物在生产、医疗、科技等方面有许多应用
(1)中国自古“信口雌黄”、“雄黄入药”之说。雄黄As2S3和雌黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图所示。
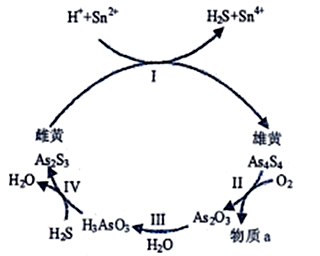
①砷元素有+2、+3+5等常见价态。,雌黄和雄黄中S元素的价态相同,其价态是______________。I中发生的离子方程式是______________________________。
②Ⅱ中,雄黄在空气中加热至300℃时会产生两种物质,若4.28g As4S4反应转移0.28mole-,则a为_______________(填化学式)砒霜(As2O3)可用双氧水将氧化成H3AsO4而除去,该反应的化学方程式为:____________________________________。
(2)AsH3是一种很强的还原剂,室温下, 0.4mol AsH3气体在空气中自燃,氧化产物为As2O3固体,放出b kJ 热量,AsH3自燃的热化学方程式是:____________________________________。
(3)将Na3AsO3(aq)+I2(aq)+H2O(l) Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
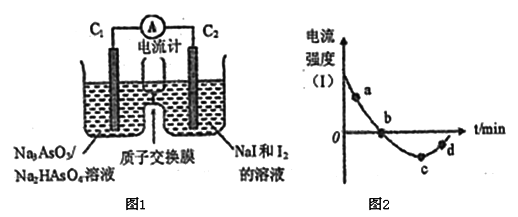
①如图中表示在该时刻上述可逆反应达到平衡状态的点是_________________(填字母)。
②已知:a点对应如图中电流由C1极经外电路流向C2极。则d点对应的负极的反应式为_____________。
③如图中,b→c改变条件可能是____________(填代号),c→d电流强度变化的原因是___________。
A.向左室中加入适量的浓Na3AsO3溶液 B.向左室中加入适量的烧碱溶液
C.向右室中加入适量的浓KI溶液 D. 向右室中加入适量的稀硫酸
-
中国自古有“信口雌黄”、“雄黄入药”之说。雌黄(As2S3)和雄黄(As4S4)都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
(1)砷元素有+2、+3两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。
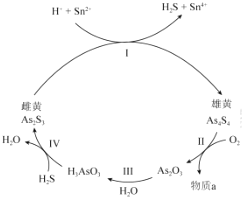
①Ⅰ中,氧化剂是______。
②Ⅱ中,若1mol As4S4反应转移28mole-,则反应Ⅱ的化学方程式是______。
(2)Ⅲ中产物亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH关系如图所示。
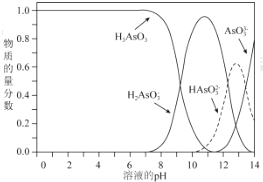
①人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是_____。
②将KOH溶液滴入亚砷酸溶液,当pH调至11时发生反应的离子方程式是______。
③下列说法正确的是 ______(填字母序号)。
a.n(H3AsO3):(H2AsO3-)=1:1时,溶液显碱性
b.pH=12时,溶液中c(H2AsO3-)+2c(HAsO32-)+3c(AsO33-)+c(OH-)=c(H+)
c.在K3AsS3溶液中,c(AsO33-)>c(HAsO32-)>c(H2AsO3-)
(3)工业含砷(III)废水常用铁盐处理后排放,其原理是:铁盐混凝剂在溶液中生产Fe(OH)3胶粒,其表面带有正电荷,可吸附含砷化合物。经测定不同pH条件下铁盐对含砷(Ⅲ)化合物的去除率如图所示。pH在5~9之间时,随溶液pH增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合(2)和(3)中图示解释可能的原因: _______。
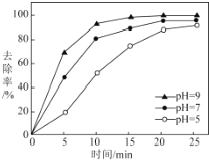
-
中国自古有“ 信口雌黄”、“雄黄入药”之说。雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。根据题意完成下列填空:
信口雌黄”、“雄黄入药”之说。雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。根据题意完成下列填空:
(1) 砷元素有+2、+3两种常见价态。As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,写出该反应的化学方程式_____________________。
(2) 上述反应中的氧化剂是___________;氧化产物是___________;反应产生的H2S气体可用____________吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++ 10NO3—=2H3AsO4+3S+10NO2↑+ 2H2O。若生成1mol H3AsO4,则反应中转移电子的物质的量为___________;若将该反应设计成一原电池,则NO2应该在___________(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2LO2(标准状况)混合后用水吸收全部转化 成浓HNO3,然后与过量的碳反应,写出碳与浓硝酸反应的化学方程式__________________;所产生的CO2的量___________(选填编号)。
成浓HNO3,然后与过量的碳反应,写出碳与浓硝酸反应的化学方程式__________________;所产生的CO2的量___________(选填编号)。
A.小于0.5mol B.等于0.5mol C.大于0.5mol D.无法确定
-
砷是生命的第七元素,可形成多种重要化合物,如雌黄(As2S3)、雄黄(As4S4)、砷酸(H3AsO4)和亚砷酸(H3AsO3)等。
(1)雄黄可入药。若0.5mo1雄黄与O2反应生成As2O3,转移14mol电子,则另一种产物为______________(填化学式)。
(2)砷酸(H3AsO4)是一种重要化工产品,可与足量NaOH溶液反应生成Na3AsO4。NaH2AsO4溶液水解反应的Kh=_________,该溶液显______(填“酸”或“碱”)性。若向该溶液中加入少量NaOH固体,则溶液中 将_______(填“增大”、“减小”或“不变”)。(已知:25℃,砷酸的Ka1=5×10-3,Ka2=1.7×10-7)
将_______(填“增大”、“减小”或“不变”)。(已知:25℃,砷酸的Ka1=5×10-3,Ka2=1.7×10-7)
(3)亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态。常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化如图所示。
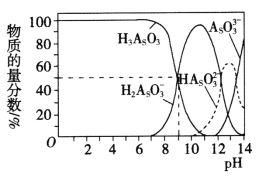
以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为红色时停止滴加。该过程中主要反应的离子方程式为_______________,pH=8时,溶液中,c(Na+)________c(H2AsO3-)(填“>”、“<”或“=”)。
-
(12分)雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为 ( 。)
(2)上述反应中的氧化剂是( ),反应产生的气体可用( )吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为( )。若将该反应设计成一原电池,则NO2应该在( )(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 ( )(选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定

AsO32-+I2+OH-。当P池中溶液由无色变成蓝色时,正极上的电极反应式为___________。










