-
下列关于元素周期表的结构、性质和用途叙述正确的是
A.过渡元素一定是金属元素
B.根据构造原理、泡利原理等核外电子排布规律可预测未来的第八周期包括的元素的种类有64个
C.合成新型农药可以在元素周期表的金属与非金属交界处区域探寻
D.原子最外层电子数为2的元素一定是 IIA元素
高三化学选择题中等难度题查看答案及解析
-
【化学一一选修3:物质结构与性质】过渡金属元素的单质及化合物在科学研究和工业生产中具有许多用途,根据所学知识回答下列问题:
(1)基态Ni2+的核外电子排布式_______________;配合物Ni(CO)4常温下为液态,易溶于CCl4,苯等有机溶剂,固态Ni(CO)4,属于_______________晶体;镍的羰基配合物Ni(CO)4是获得高纯度纳米镍的原料,该配合物中镍原子的价电子排布为3d10,则其杂化轨道类型为_______________,Ni(CO)4是_______________(填“极性”或“非极性” )分子。
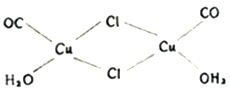
(2)氯化亚铜是一种白色固体,实验测得其蒸气密度是同条件下氢气密度的99.5倍,则氯化亚铜的分子式为_______________;氯化亚铜的盐酸溶液可定量吸收CO形成配合物Cu2(CO)2Cl2·2H2O(结构如图所示),该反应可用于测定空气中CO的含量,每个Cu2(CO)2Cl2·2H2O分子中含_______________个配位键。
(3)铜能与类卤素(SCN)2 反应生成 Cu(SCN)2,(SCN)2 分子中含有σ键与π键的数目比为__________; 类卤素 (SCN)2 对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是_______________。
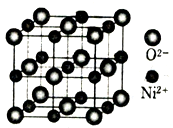
(4)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为apm,列式表示NiO晶体的密度为_______________g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。
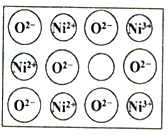
人工制备的NiO晶体中常存在缺陷(如图):一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。已知某氧化镍样品组成Ni0.96O,该晶体中Ni3+与Ni2+的离子个数之比为_______________。
高三化学填空题中等难度题查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是
A.
半径逐渐减小
B.还原性强弱:
C.核外电子排布相同的微粒化学性质一定相同
D.同主族元素含氧酸的酸性随核电荷数的增加而减弱
高三化学选择题中等难度题查看答案及解析
-
以下对粒子结构或性质的叙述正确的是( )
A.两种微粒,若核外电子排布完全相同,则化学性质一定相同
B.由单原子形成的离子,一定具有稀有气体元素原子核外电子排布
C.阴离子的核外电子排布一定与上一周期稀有气体原子核外排布相同
D.两原子,如果核外电子排布相同,则一定属于同一种元素
高三化学选择题中等难度题查看答案及解析
-
【化学—选修3:物质结构与性质】铜是重要的过渡元素,其单质及化合物具有广泛用途。回答下列问题:
(1)铜元素基态原子的价电子排布式________。
(2)铜能形成多种配合物,如Cu2+与乙二胺(H2N-CH2-CH2-NH2)可形成如图所示配离子。
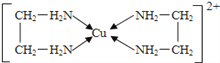
①Cu2+与乙二胺所形成的配离子中含有的化学键是________。
a.配位键 b.离子键 c.
键 d.
键
②乙二胺分子中氮原子的杂化轨道类型为________,C、N、H三种元素的电负性由大到小顺序是________。
③乙二胺和三甲胺[N(CH3)3]均属于胺,乙二胺的沸点比三甲胺高很多,原因是________。
(3)Cu2+在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+,其原因是________。
(4)Cu和S形成某种晶体的晶胞如图所示。
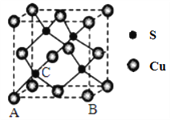
①该晶体的化学式为________。
②该晶胞原子坐标参数A为(0,0,0);B为(1,0,0)。则C原子的坐标参数为________。
③已知该晶体的密度为d g·cm-3,Cu2+和S2-的半径分别为a pm和b pm,阿伏加德罗常数值为NA。列式表示该晶体中原子的空间利用率________。
高三化学综合题中等难度题查看答案及解析
-
[化学一-选修3:物质结构与性质]由S、Cl 及Fe、Co、Ni 等过渡元素组成的新型材料有着广泛的用途,回答下列问题:
(1)钴元素基态原子的电子排布式为________,P、S、Cl的第一电离能由大到小顺序为______。
(2)SCl2 分子中的中心原子杂化轨道类型是______,该分子空间构型为_______。
(3)Fe、Co、Ni等过渡元素易与CO形成配合物,化学式遵循18电子规则:中心原子的价电子数加上配体提供的电子数之和等于18,如Ni 与CO形成配合物化学式为Ni(CO)4,则Fe与CO形成配合物化学式为_______。Ni(CO)4中σ键与π键个数比为_______,Ni(CO)4为____晶 体。
(4)已知NiO的晶体结构如图1所示。
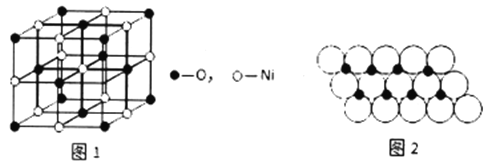
①NiO的晶体结构可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中。则NiO 晶体中镍原子填充在氧原子形成的______体空隙中。
②已知MgO 与NiO的晶体结构相同,其中Mg2+和Ni2+的离子半径分别为66pm 和69pm。则熔点:MgO_____ NiO( 填“ >”、“ <" 或“ =” ), 理由是______________。
③一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为am,每平方米面积上分散的NiO的质量为_________g。(用a、NA表示)
高三化学综合题中等难度题查看答案及解析
-
(化学-选修3:物质结构与性质)
由S、Cl及Fe、Co、Ni 等过渡元素组成的新型材料有着广泛的用途,回答下列问题:
(1)钴元素基态原子的电子排布式为____,P、S、C1的第一电离能由大到小顺序为______。
(2)SCl2分子中的中心原子杂化轨道类型是_______,该分子空间构型为________。
(3)Fe、Co、Ni等过渡元素易与CO形成配合物,化学式遵循18电子规则:中心原子的价电子数加上配体提供的电子数之和等于18,如Ni与CO形成配合物化学式为Ni(CO)4,则Fe与CO形成配合物化学式为_______。Ni(CO)4中σ键与π键个数比为______,已知:Ni(CO)4熔点-19.3℃,沸点43℃,则Ni(CO)4为_______晶体。
(4)已知NiO的晶体结构如图所示。
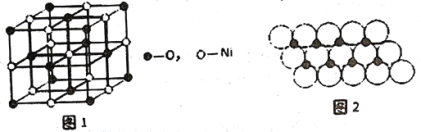
①NiO的晶体结构可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中。则NiO晶体中镍原子填充在氧原子形成的___体空隙中。
②已知MgO与NiO的晶体结构相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO____NiO( 填“ >”、“<”或“=”),理由是_______________。
③一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充O2-形成的正三角形空隙中(如图),己知O2-的半径为am,每平方米面积上分散的NiO的质量为______g。(用a、NA表示)
高三化学综合题困难题查看答案及解析
-
[化学-物质结构与性质]
研究物质结构是为更好的掌握物质的性质.
(1)第四周期过渡元素在性质上存在一些特殊性,在前沿科技中应用广泛.
①铜为第四周期过渡元素,其基态原子电子排布式为______,请解释金属铜能导电的原因______.
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测Ni(CO)4易溶于下列______.
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
③在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有______.
(2)已知:下表是14种元素的电负性的数值(用X表示).
①经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键,如NaCl;当小于1.7时,一般为共价键,如AlCl3.请写出铁元素和表中非金属元素形成的常见共价化合物:______.元素 Al B Be C Cl F Li X 1.5 2.0 1.5 2.5 2.8 4.0 1.0 元素 Mg Na O P S Si Fe X 1.2 0.9 3.5 2.1 2.5 1.7 1.8
②气态氯化铝通常以二聚分子形式存在,分子式为Al2Cl6,分子中所有原子均达到8电子稳定结构,则Al2Cl6的结构式为______.
③由表中两种元素形成的化合物中,分子中既含有σ键又含有π键,且二者数目相同的有(写一个即可)______,其分子空间构型为______.高三化学解答题中等难度题查看答案及解析
-
[物质结构与性质,13分]
(1)与铜同周期、基态原子最外层电子数相同的过渡元素,其基态原子的电子排布式 。
(2)下图曲线表示部分短周期元素的原子序数(按递增顺序排列)和其常见单质沸点的关系。其中A点表示的单质是 (填化学式)。
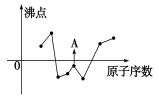
键长/(pm)
B—F
B—Cl
B—Br
计算值
152
187
199
实测值
130
175
187
(3)三氟化硼分子的空间构型是 ;三溴化硼、三氯化硼分子结构与三氟化硼相似,如果把B-X键都当作单键考虑来计算键长,理论值与实测键长结果如右表。硼卤键长实测值比计算值要短得多,可能的原因是 。
(4)海产品添加剂多聚磷酸钠是由Na+与多聚磷酸根离子组成的,某种多聚磷酸根的结构如图。
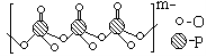
①磷原子的杂化类型为 。
②这种多聚磷酸钠的化学式为 。
(5)已知HF与F-通过氢键结合成HF
。判断HF
和HF
微粒间能否形成氢键,并说明理由。
。
高三化学填空题困难题查看答案及解析
-
物质结构与性质
VA族元素单质及其化合物在工农业生产中有重要用途。回答下列问题:

基态As原子的核外电子排布式为
________,有________个未成对电子。
元素周期表中,与P紧邻的4种元素中电负性最大的是________(填元素符号
。Si、P、S三种元素的第一电离能由大到小的顺序是________。
铵盐大多不稳定,
F、
中,较易分解的是________,原因是________。
咖啡因对中枢神经有兴奋作用,其结构简式如图1。常温下,咖啡因在水中的溶解度为
,加适量水杨酸钠
可使其溶解度增大,其原因可能是________,分子中氮原子的杂化类型有________。
氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示:
物质
BN
AIN
GaN
熔点
3000
2200
1700
试从结构的角度分析它们熔点不同的原因________。
的晶胞结构如图2所示,晶体中一个B原子周围距离最近的N原子有________个;若B、N的原子半径分别为
和
,密度为
,阿伏加德罗常数值为
,则BN晶胞中原子的体积占晶胞体积的百分率为________。
高三化学综合题困难题查看答案及解析