-
(16分)在氮单质和常见化合物中:
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是 。原因是 。
(2)常用作制冷剂的物质是 ,原因是 。
(3)能与酸反应生成盐、在常温下为气态的物质是 写出它与HCl等强酸反应的离子方程式: 。
(4)在通常状况下是晶体、易溶于水、可以作氮肥、遇碱会放出带刺激性气味气体的物质是 ,写出它们与NaOH等强碱溶液反应的离子方程式: 。
高一化学填空题困难题查看答案及解析
-
在氮的单质和常见化合物中:
(1)常用做保护气(如填充灯泡、焊接保护等)的物质是_________,原因是___________
(2)常用做制冷剂的物质是__________,原因是________________________
(3)能与酸反应生成盐、在常温下为气态的物质是____,写出它与HCl等强酸反应的离子方程式:______
(4)在通常状况下是晶体、易溶于水、可以作氮肥、遇碱会放出带刺激性气味的一类物质是____,写出它们与NaOH等强碱溶液反应的离子方程式:___________
高一化学填空题困难题查看答案及解析
-
氮元素的单质和常见的化合物在工、农业生产中用途广泛。NH3、NH3·H2O、NH4Cl、HNO3是最常见的含氮化合物。
(1)氮气常用作食品袋中填充气和某些场合下的保护气,与此相关的氮气的性质是______。
(2)上述4种含氮化合物中,属于盐的是_________,属于碱的是___________。
(3)NH3常用作制冷剂,其在空气中与HCl相遇产生白烟,这里“白烟”是_________,打开盛浓硝酸的试剂瓶塞,瓶口有白雾出现,这里“白雾”是___________。
(4)Fe粉与稀硝酸反应生成硝酸铁的化学方程式为________________________。该反应中硝酸表现出的化学性质主要有_____________________。
高一化学综合题中等难度题查看答案及解析
-
氮元素的单质和常见的化合物在工、农业生产中用途广泛。
(1)常用作食品袋中填充气的是_____,常用作制冷剂的化合物是_____,该物质在空气中与HCl相遇有白烟现象,产生该现象的化学反应方程式是_______。
(2)铵盐大多在农业上用作化肥。实验室可用固体NH4Cl与固体Ca(OH)2加热反应来制备氨气,其化学方程式为_____。
高一化学填空题简单题查看答案及解析
-
(12分)氮元素的单质和化合物在工、农业生产中用途广泛。而汽车尾气中含有NO等多种污染物。
(1)常用作食品袋中填充气的是 ;(填化学式)常用作制冷剂的化合物是 ,(填化学式)该物质在空气中与HCl相遇有白烟现象,产生该现象的化学反应方程式是 。
(2)铵盐在农业上大多用作化肥。实验室可用固体铵盐NH4Cl与固体Ca(OH)2加热反应来制备氨气,其化学方程式为 。
(3)汽车燃料中一般不含氮元素,但尾气却所含有NO,产生的原因用化学方程式表示 。
(4)NO对大气的影响之一是导致酸雨,用化学方程式表示NO形成酸雨的原因是 。
高一化学填空题中等难度题查看答案及解析
-
A、D是生活中常见的金属单质,B、C、E、F、G、H是中学常见的6种化合物,反应①可用于焊接钢轨,相关物质间的关系如下图所示。
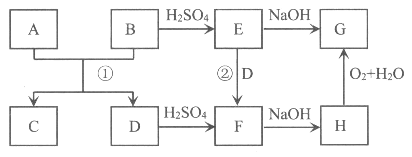
(1)H的化学式是______________。
(2)反应①的化学方程式是____________________________。
(3)反应②的离子方程式是____________________________。
(4)检验F溶液中金属阳离子的操作和现象是____________________________。
(5)H转化为G的实验现象是__________________________________________。
(6)为了更清楚地观察到生成H的现象,使F的溶液与NaOH溶液反应的正确操作是_______(填下图字母)
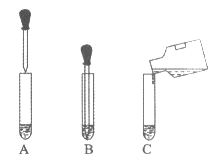
高一化学推断题困难题查看答案及解析
-
(10分)下图中,A、B、C、D、E是常见单质,其中B、C、E为金属。G、H、I、F是B、C、D、E分别和A形成的化合物,G物质有磁性。已知:①C与G反应生成B和H且放出大量的热,该反应可用于焊接铁轨;②I是一种常见的温室气体,它和E可以发生反应:
 ,F中E元素的质量分数为60%。回答问题:
,F中E元素的质量分数为60%。回答问题: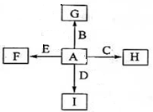
(1)C与G反应的化学方程式为 ;
(2)单质A的分子式为 ,化合物I的名称为 ;
(3)C与NaOH溶液反应的化学方程式为 ;
(4)过量I与NaOH溶液反应的离子方程式为 ;
高一化学填空题中等难度题查看答案及解析
-
右图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质。已知:①I是一种常见的温室气体,E原子核内有12个质子②G为红色物质,反应
能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题:

(1)分别写出F、G、H、I的化学式
F ________ G ________H ________ I________
(2)书写下列化学方程式
________;
________
(3)C与NaOH溶液反应的化学方程式为________,
反应后溶液与过量化合物I反应的化学方程式为________;
⑷1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量为:________
高一化学推断题困难题查看答案及解析
-
下图中,A,B,C,D,E是单质,G,H,I,F是B,C,D,E分别和A形成的二元化合物。
已知:①反应C+G
B+H能放出大量的热,该反应曾应用于铁轨的焊接;
②I是一种常见的温室气体,它和E可以发生反应:2E+I
2F+D,F中E元素的质量分数为60%。
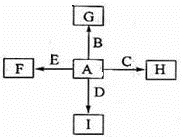
回答问题:
⑴①中反应的化学方程式为______________;
⑵化合物I的电子式为_______,它的空间结构是______;
⑶C与过量NaOH溶液反应的离子方程式为____________,反应后溶于与过量化合物I反应的离子方程式为____________________;
⑷E在I中燃烧观察到的现象是_____________________。
⑸1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量_____________;
高一化学推断题困难题查看答案及解析
-
(10分)在下图所示的物质转化关系中(反应条件已略去)。A是海水中含量最多的盐,B是最常见的无色液体,D、E、F、H为单质。反应①是海水资源综合利用的重要反应,反应②常用于钢轨的焊接,工业上用C与D反应制备漂白液。

请回答下列问题:
(1)E的化学式为__________。
(2)C的电子式为__________。
(3)F元素在元素周期表中的位置是__________。
(4)反应③的离子方程式为__________。
(5)反应④的化学方程式为__________。
(6)若G具有磁性,则反应②中每生成1mol H转移电子的数目为__________。
高一化学填空题简单题查看答案及解析