-
由ⅢA、VA族元素组成的新型材料有着广泛用途。
(1)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造。与BCl3互为等电子体,且由第二周期元素组成的一种阴离子为__________(填离子符号)。
(2)氨硼烷(H3N—BH3)和Ti(BH4)3均为广受关注的新型化学氢化物储氢材料。
①H3N—BH3中N 原子的轨道杂化类型为________________。
②Ti(BH4)3由TiCl3和LiBH4反应制得。基态Ti3+的未成对电子数为____________;BH4-的立体构型
是_______;该制备反应的化学方程式为______________ 。
(3)氨硼烷可由六元环状化合物(HB=NH)3通过如下反应制得:
3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。
下列有关叙述错误的是_____________
A.氨硼烷中存在配位键
B.第一电离能大小关系:N>O>C>B>H
C.反应前后碳原子的杂化类型不变
D.CH4、H2O、CO2分子空间构型分别是:正四面体型、V型、直线型
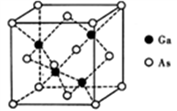
(3) GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为_____________。Ga的配位原子(As)数目为________;Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,原子半径分别为rGa cm和rAscm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为__________。
-
硼及其化合物在耐高温合金工业、催化剂制造、高能燃料等方面有广泛应用。
(1)硼原子的价电子排布图为____________。
(2)B2H6是一种高能燃料,它与Cl2反应生成的BCl3可用于半导体掺杂工艺及高纯硅制造。由第二周期元素组成的与BCl3互为等电子体的阴离子为________。
(3)氮硼烷化合物(H2N→BH2)和Ti(BH4)3均为广受关注的新型储氢材料。
①B与N的第一电离能:B__________N(填“>”“<”或“=”,下同)。H2N―→BH2中B原子的杂化类型为________。
②Ti(BH4)3由TiCl3和LiBH4反应制得。BH4-的立体构型是________;写出制备反应的化学方程式:____________。
(4)磷化硼(BP)是受到高度关注的耐磨材料,它可用作金属表面的保护层。如图为磷化硼晶胞。
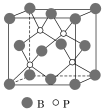
①磷化硼晶体属于______________晶体(填晶体类型),____________(填“是”或“否”)含有配位键。
②晶体中P原子的配位数为____________。
③已知BP的晶胞边长为a nm,NA为阿伏加德罗常数的数值,则磷化硼晶体的密度为____________g·cm-3(用含a、NA的式子表示)。
-
氯气用途十分广泛,可用于生产半导体材料硅,其生产的流程如下,下列说法不正确的是( )

A.①③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅的
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
-
氯气用途十分广泛,可用于生产半导体材料硅,其生产的流程如下,下列说法不正确的是( )

A.①③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅的
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
-
氯气用途十分广泛,可用于生产半导体材料硅,其生产的流程如下,下列说法不正确的是

A.①③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅的
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
-
由Cu、N、B等元素组成的新型材料有着广泛用途。
(1)基态 Cu+ 的核外电子排布式为____________。在高温下CuO 能分解生成Cu2O,试从原子结构角度解释其原因:_______________________________。
(2)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,它属于____晶体。
(3)化合物A (H3BNH3) 是一种潜在的储氢材料,它可由六元环状化合物 (HB=NH)3通过3CH4+ 2 (HB=NH)3+ 6H2O →3CO2 + 6H3BNH3 制得。
①与上述化学方程式有关的叙述不正确的是_________。(填标号)
| A.反应前后碳原子的轨道杂化类型不变 |
| B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形 |
| C.第一电离能:N>O>C>B |
| D.化合物A中存在配位键 |
②1个 (HB=NH)3分子中有__个σ键。
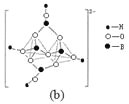
(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为________。图(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为_________。

-
三氯化硼(BCl3),主要用作半导体硅的掺杂源或有机合成催化剂,还用于高纯硼或有机硼的制取。某兴趣小组用氯气和硼为原料,采用下列装置(部分装置可重复使用)制备BCl3。
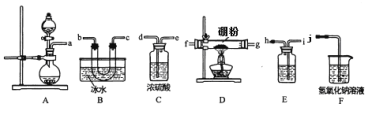
已知:①BCl3的沸点为12.5℃,熔点为-107.3℃;遇水剧烈反应生成硼酸和盐酸;②2B+6HCl  2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
请回答下列问题:
(1)A装置可用氯酸钾固体与浓盐酸反应制氯气,反应的化学方程式为___________。
(2)装置从左到右的接口连接顺序为a→___________________→j。
(3)装里E中的试剂为___________,如果拆去E装置,可能的后果是____________。
(4)D装置中发生反应前先通入一段时间的氯气,排尽装置中的空气。若缺少此步骤,则造成的结果是_____。
(5)三氯化硼与水能剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式________,硼酸也可用电渗析法制备,“四室电渗析法”工作原理如图所示:

则阳极的电极反应式__________________,分析产品室可得到H3BO3的原因________________。
-
肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面。请回答下列问题:
(1)肼是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键能如下:
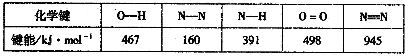
①N2H4中氮元素的化合价为__________。
②气态N2H4在氧气中燃烧的热化学方程式为__________。
(2)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式为__________。
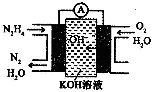
(3)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为__________.
(4)盐酸肼(N2H6Cl2)是一种化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4 Cl类似,但分步水解。
①写出盐酸肼第一步水解的离子方程式__________。
②盐酸肼水溶液中离子浓度的关系为__________ (填序号)。
A.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
B.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
C.c(N2H62+)+ c([N2H5·H2O+]) +c(H+)= c(Cl-)+c(OH-)
(5〕常温下,将0.2 mol/L盐酸与0.2 mol/L肼的溶液等体积混合(忽略混合后溶液体积变化〕。若测定混合液的pH=6,混合液中水电离出的H+与0.1mol/L盐酸中水电离出的H+浓度之比为__________。
-
化学在生产生活中有着广泛的应用,下列两项内容说法正确且存在因果关系的是( )
| 物质性质 | 实际应用 |
| A | 硅为半导体材料 | SiO2用于光纤通讯 |
| B | Cl2具有氧化性 | 氯水可以漂白有色布条 |
| C | Al表面易形成致密的氧化物薄膜 | 可以用铝槽车运送热的浓硫酸 |
| D | 乙醇可以使蛋白质变性 | 乙醇用于制作医用酒精 |
A.A B.B C.C D.D
-
碳和硅属于同主族元素,在生活生产中有着广泛的用途。
(1)甲烷可用作燃料电池,将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池,通入CH4的一极,其电极反应式是 ;
CH4催化还原NOX可以消除氮氧化物的污染,有望解决汽车尾气污染问题,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则NO2被甲烷还原为N2的热化学方程式为_____________________________________
(2)已知H2CO3 HCO3-+ H+ Ka1(H2CO3)=4.45×10-7
HCO3-+ H+ Ka1(H2CO3)=4.45×10-7
HCO3- CO32-+H+ Ka2(HCO3-)=5.61×10-11
CO32-+H+ Ka2(HCO3-)=5.61×10-11
HA H++A- Ka(HA)=2.95×10-8
H++A- Ka(HA)=2.95×10-8
请依据以上电离平衡常数,写出少量CO2通入到NaA溶液中的离子方程式
___________________________。
(3) 在T温度时,将1.0molCO2和3.0molH2充入2L密闭恒容器中,可发生反应的方程式为CO2 (g) + 3H2(g)  CH3OH(g) + 2H2O(g) 。充分反应达到平衡后,若容器内的压强与起始压强之比为a :1,则CO2转 化率为______,当a=0.875时,该条件下此反应的平衡常数为_______________(用分数表示)。
CH3OH(g) + 2H2O(g) 。充分反应达到平衡后,若容器内的压强与起始压强之比为a :1,则CO2转 化率为______,当a=0.875时,该条件下此反应的平衡常数为_______________(用分数表示)。
(4)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英(SiO2)与焦炭在高温的氮气流中反应生成,已知该反应的平衡常数表达式K=[c(CO)]6/[c(N2)]2,若已知CO生成速率为v(CO)=6mol·L-1·min-1,则N2消耗速率为v(N2)= ;该反应的化学方程式为________________________________________。










