-
分实验室需要450 mL 1.0 mol·L-1的硫酸溶液,某小组的同学设计如下实验步骤并依此进行配制,请回答相关问题。(已知所用98%浓硫酸的密度为1.84 g/mL)
①计算需98%的浓硫酸的体积;
②在烧杯中将浓硫酸稀释;
③接着将稀释后的硫酸转移到容量瓶中;
④洗涤烧杯和玻璃棒3次,并将洗涤液转移到容量瓶中;
⑤定容;
⑥摇匀。
(1)该实验中选用的定量仪器,除量筒外,还有________________。
(2)该实验应该用(多大规格)_____ ______的量筒(可供选择的量筒规格为10 mL、15 mL、20 mL、50 mL和100 mL),量取___________mL 98%的浓硫酸。
(3)①在配制过程中,如果没有洗涤烧杯和玻璃棒,其他操作都正确,那么所配溶液的实际浓度将_____________(填“偏大、偏小、无影响”)
②某同学转移溶液的操作如图所示,该同学操作中的错误是 。

③若用胶头滴管定容时,不小心滴水滴过了刻度线,你认为应该采取的处理方法是: 。
④下列操作中,可能造成所配制溶液的浓度偏高的是 (填选项)。
a.溶解后没有冷却至室温就将液体转移至容量瓶中
b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水
d.用量筒量取浓硫酸,读数时仰视刻度线
-
某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:
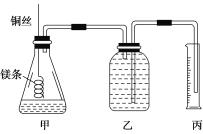
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol/L的盐酸溶液;
②用________(填仪器名称并注明规格)量取10.0 mL 1.0 mol/L的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)用文字表述实验步骤④中检查装置气密性的方法:
___________________________________________________
(2)实验步骤⑤中应选用________(填序号)的量筒。
A.100 mol B.200 mL C.500 mL
读数时除恢复到室温外,还要注意_________________________________________。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=________,若未除去镁条表面的氧化膜,则测量结果________(填“偏大”、“偏小”或“无影响”)。
-
实验室需要用质量分数为98%、密度为1.84g/cm3的浓硫酸配制1.0 mol·L-1的稀硫酸溶液450mL,请回答下列问题
(1)需要用量筒量取的浓硫酸的体积为__________mL。
(2)下面操作造成所配稀硫酸溶液浓度(填“偏高”、“偏低”或“无影响”)
①用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶__________。
②向容量瓶加水定容时眼睛俯视液面__________。
-
硫酸是中学化学实验室的常见药品,回答下列实验问题。
Ⅰ.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435ml。同学们发现实验室内没有450ml的容量瓶,某同学提议用1个200ml容量瓶和1个250ml容量瓶来配制,你认为该提议_________(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250ml。则需量取密度为1.84g/ml、98%的浓硫酸________ml。

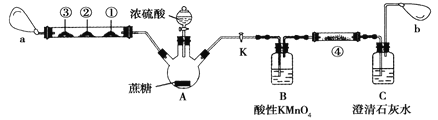
Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。某实验小组利用如下装置对该实验进行改进。回答下列问题:
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(1)图中盛装浓硫酸的仪器名称为________________。
(2)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是SO2,①、②、③处发生的变化分别说明SO2具有_____________、_____________和_____________(填SO2表现出的性质)。
(3)打开活塞K,a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位置的滤纸滴加______________溶液,该试剂的作用是_________________________________________。
-
硫酸是中学化学实验室的常见药品,回答下列实验问题。
Ⅰ.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435ml。同学们发现实验室内没有450ml的容量瓶,某同学提议用1个200ml容量瓶和1个250ml容量瓶来配制,你认为该提议_________(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250ml。则需量取密度为1.84g/ml、98%的浓硫酸________ml。
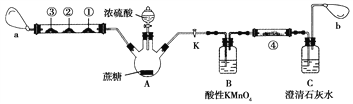
Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。某实验小组利用如下装置对该实验进行改进。回答下列问题:
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(1)图中盛装浓硫酸的仪器名称为________________。
(2)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是SO2,①、②、③处发生的变化分别说明SO2具有_____________、_____________和_____________(填SO2表现出的性质)。
(3)打开活塞K,a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位置的滤纸滴加______________溶液,该试剂的作用是_________________________________________。
-
硫酸是中学化学实验室的常见药品,回答下列实验问题。
Ⅰ.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435ml。同学们发现实验室内没有450ml的容量瓶,某同学提议用1个200ml容量瓶和1个250ml容量瓶来配制,你认为该提议_________(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250ml。则需量取密度为1.84g/ml、98%的浓硫酸________ml。
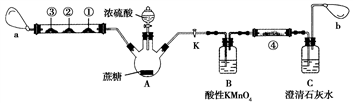
Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。某实验小组利用如下装置对该实验进行改进。回答下列问题:
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(1)图中盛装浓硫酸的仪器名称为________________。
(2)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是SO2,①、②、③处发生的变化分别说明SO2具有_____________、_____________和_____________(填SO2表现出的性质)。
(3)打开活塞K,a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位置的滤纸滴加______________溶液,该试剂的作用是_________________________________________。
-
硫酸是中学化学实验室的常见药品,回答下列问题:
I.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435mL。同学们发现实验室内没有450mL的容量瓶,某同学提议用1个200mL容量瓶和1个250mL容量瓶来配制,你认为该提议______(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250mL,则需量取密度为1.84g/mL、98%的浓硫酸________mL(结果保留小数点后一位)。
Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。 某实验小组利用如下装置对该实验进行改进。回答下列问题:
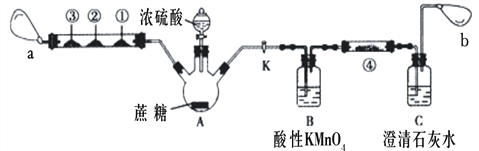
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(3)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是 SO2,
①、②、③处发生的变化分别说明SO2具有_______、________和__________(填SO2表现出的性质)。
(4)SO2和Cl2均可以使品红溶液褪色,但将两种气体按体积比1:1混合通入品红溶液中,品红溶液不褪色,其原因是___________(用化学方程式回答)。
(5)打开活塞K, a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位罝的滤纸滴加_______溶液,该试剂的作用是__________。
-
硫酸是中学化学实验室的常见药品,回答下列问题:
I配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435mL。同学们发现实验室内没有450mL的容量瓶,某同学提议用1个200mL容量瓶和1个250mL容量瓶来配制,你认为该提议______(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250ml。则需量取密度为1.84g/mL、98%的浓硫酸________mL。
Ⅱ蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。某实验小组利用如下装置对该实验进行改进。回答下列问题:
注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(3)图中盛装浓硫酸的仪器名称为_______。
(4)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是 SO2,①、②、③处发生的变化分别说明SO2具有_______、________和__________(填SO2表现出的性质)。
(5)打开活塞K, a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位罝的滤纸滴加_______溶液,该试剂的作用是__________。
-
实验室需用450 mL3.0 mol·L-1 H2SO4溶液,某同学用98%的浓硫酸 (密度为1.84 g/mL)按下列步骤来配制。
(1)请回答有关问题。
| 实验步骤 | 有关问题 |
| a.计算所需浓H2SO4的体积; | 量取浓H2SO4的体积为①__________ |
| b.量取浓硫酸; | |
| c.将浓H2SO4慢慢加入到装有蒸馏水的200 mL烧杯中; | |
| d.将烧杯中的溶液冷却后转移至②__________中; | |
| e.洗涤后,向容量瓶中加蒸馏水距刻度线1~2cm,改用③__________定容。 | |
(2)配制H2SO4溶液时,若出现下列操作,其结果偏高还是偏低?
A.量取浓H2SO4溶液时仰视读数 ____;
B.定容时仰视刻度线 ___;
C.浓硫酸溶于水后未经冷却就转移____。
-
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题。该小组设计的简易实验装置如图所示:
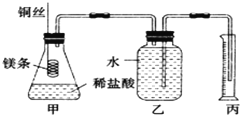
该实验的主要操作步骤如下:
①用已知浓度的浓盐酸配制100mL 1.0mol/L的盐酸溶液,需要用到的仪器有量筒、烧杯、玻璃棒、胶头滴管、______;
②用10mL量筒量取8.0mL 1.0mol/L的盐酸溶液加入锥形瓶中;
③准确称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为______;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,忽略导管中的水,读出量筒中水的体积为VmL。
请回答下列问题。
(1)步骤①中,配制100mL 1.0mol/L的盐酸溶液时,下列哪些操作会使配制浓度偏低_____(填写字母)
A. 用量筒量取浓盐酸时,俯视量筒的刻度
B. 容量瓶未干燥即用来配制溶液
C. 未洗涤烧杯和玻璃棒
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
(2)请填写操作步骤中的空格:步骤①__________ 步骤③__________
(3)实验步骤⑤中应选用________的量筒(填字母).
A.100mL B.200mL C.500mL
(4)读数时需要注意(至少写两点)____________
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积为Vm=____L/mol。(用含V的式子表示)






