-
以赤铁矿为原料,利用高炉炼铁的基本反应为:
i.Fe2O3(s)+3CO 2Fe(s)+3CO2(g)△H1
2Fe(s)+3CO2(g)△H1
其中CO产生的反应是:
ii.C(焦炭,s)+O2(空气,g)=CO2(g)△H2<0
iii.C(焦炭,s)+CO2(g)=2CO(g)△H3>0
(1)以焦炭炼铁的反应:3C(焦炭,s)+2Fe2O3(s) 4Fe(s)+3CO2(g)的△H=____________(请用含△H1、△H2或H3的式子表示)。
4Fe(s)+3CO2(g)的△H=____________(请用含△H1、△H2或H3的式子表示)。
(2)反应i的平衡常数与温度的关系如下表,请回答:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数K | 64.0 | 50.6 | 42.9 |
①当反应温度为1150℃,高炉中n(CO):n(CO2)=4:1时,v正_____v逆(填大于、小于、或等于)。
②己知高炉容积VL,反应温度1000℃。若提供给i反应的CO共2.24×103L(已折算标准状况),该反应经过tmin达平衡,则CO2在此段时间的反应速率为________(用V、t代数式表示)。
(3)T℃下,初始体积均为2L,初始压强均为100kPa的甲(固定体积),乙(固定压强)两容器中各充入2molCO进行反应iii,达平衡时甲中气体压强变为原来的4/5倍。请回答:
①下列可以判断甲中反应达平衡的是________________(填字母序号)。
a.2c(CO2)=c(CO)
b.v正(CO2)=2v逆(CO)
c.气体密度不再改变
d.气体平均分子量不再改变
②下图为甲、乙两容器中CO的百分含量(CO%)与时间(t)的关系示意图,其中代表乙容器的是___________(填字母编号),理由是______________________。
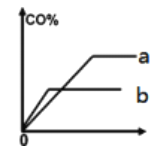
③乙容器中达平衡时的平衡常数Kp=___________________(Kp为用压强表达的平衡常数)。
-
下列工业生产的反应原理错误的是( )
A.高炉炼铁:Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
B.氨的氧化:4NH3+5O2 4NO+6H2O
4NO+6H2O
C.煅烧硫铁矿:4FeS2+15O2 2Fe2O3+8SO3
2Fe2O3+8SO3
D.制漂粉精:2Ca(OH)2+2Cl2→CaCl2+Ca(ClO)2+2H2O
-
下列工业生产的反应原理错误的是( )
A.高炉炼铁:Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
B.氨的氧化:4NH3+5O2 4NO+6H2O
4NO+6H2O
C.煅烧硫铁矿:4FeS2+15O2 2Fe2O3+8SO3
2Fe2O3+8SO3
D.制漂粉精:2Ca(OH)2+2Cl2→CaCl2+Ca(ClO)2+2H2O
-
2008年,中国人民经受了雪灾、震灾等自然灾害的严峻考验,漫长的灾后重建需要大量的钢铁.高炉炼铁中发生的基本反应为Fe2O3+3CO
 2Fe+3CO2,为更快更好的生产出优质钢材,下列措施不可行的是( )
2Fe+3CO2,为更快更好的生产出优质钢材,下列措施不可行的是( )
A.升高温度
B.建容量大的高炉,增大铁矿石的投入量
C.增大CO的浓度
D.将铁矿石粉碎,尽可能用小块的铁矿石
-
高炉炼铁的主要反应是:Fe2O3+3CO⇌2Fe+3CO2.下列说法正确的是( )
A.CO2的电子式为
B.Fe2O3分别与浓硝酸和稀硝酸反应,二者产物不同
C.在高炉炼铁过程中,若增加炼铁高炉的高度能提高CO的转化率
D.在高炉炼铁过程中,将铁矿石粉碎后投入高炉可以提高该反应的化学反应速率
-
工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:① 2C(焦炭)+O2(空气)=2CO;② Fe2O3+3CO=2Fe+3CO2该炼铁工艺中,对焦炭的实际使用量要远高于按照化学方程式计算所需,可能的主要原因是:
A.炼铁高炉的高度不够 B.CO与铁矿石接触不充分
C. CO过量 D.CO与Fe2O3的反应有一定限度
-
I.高炉炼铁的主要反应为Fe2O3+3CO2Fe+3CO2。
已知该反应的 H,在1000℃时,K=64。在1000℃的条,在容积10 L的密闭容器中,加入Fe、Fe2O3、CO、CO2各1.OmoI,反应经10 min后达到平衡。
H,在1000℃时,K=64。在1000℃的条,在容积10 L的密闭容器中,加入Fe、Fe2O3、CO、CO2各1.OmoI,反应经10 min后达到平衡。
(1)该时间范围内的平均反应速率v(CO2)=_________mol/L min
min
(2) 的最大转化率_________________。
(3)欲提高CO的平衡转化率,可采取的措施是_______________。
A.减少Fe的量 B.增加Fe2O3的量
C.升高反应温度 D.移出部分CO2
E.使用合适的催化剂 F.减少容器的容积
Ⅱ.已知化学反应①:Fe(s)+CO2(g) FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g) FeO(s)+H2(g),其平衡常数K2.在温度973K和1173K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数K2.在温度973K和1173K情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(4)通过表格中的数值可以推断:反应①的△H_________O。(填“>”“<”)
(5)现有反应③:该反应的平衡常数的数学表
达式K3=____。
(6)根据反应①和②可以推导出Ki,Kz和玛之间的关系式。K3=__________。据此关系式和上表数据,也能推断出反应③的△H__________0(填“>”“<”)。
-
高炉炼铁的主要反应为:3CO(g)+Fe2O3(s)⇌3CO2(g)+2Fe(s),已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
下列说法正确的是( )
A.增加Fe2O3固体可以提高CO的转化率
B.减小容器体积既能提高反应速率又能提高平衡转化率
C.该反应的正反应ΔH<0
D.当容器内气体密度恒定时,不标志该反应已达到平衡状态
-
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应:
Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ΔH
2Fe(s)+3CO2(g) ΔH
已知:
Ⅰ.Fe2O3(s)+3C(石墨,s)  2Fe(s)+3CO(g) ΔH1
2Fe(s)+3CO(g) ΔH1
Ⅱ.C(石墨,s)+CO2(g)  2CO(g) ΔH2
2CO(g) ΔH2
①ΔH=____________________(用含ΔH1、 ΔH2代数式表示)。
②保持温度不变,在恒容容器中进行反应Ⅰ,达到平衡状态,再次充入一定量的CO (Fe足量),则平衡______(填“正向”或“逆向”)移动,达到新平衡后c(CO)将________(填“变大”“变小”或“不变”)。
(2)在T ℃时,反应 Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g)的平衡常数K=64,在2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
2Fe(s)+3CO2(g)的平衡常数K=64,在2 L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
| Fe2O3 | CO | Fe | CO2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
①甲容器中CO的平衡转化率为__________________。
②下列说法正确的是________(填字母)。
A.若容器内压强恒定,说明反应达到平衡状态
B.增加Fe2O3的量能提高CO的转化率
C.甲容器中CO的平衡转化率大于乙容器
D.若容器中固体质量不再改变,说明反应达到平衡状态
③取五等份CO,分别加入温度不同但容积相同的恒容密闭容器中(已装有足量Fe2O3),反应相同时间后,分别测定体系中CO的体积分数(CO%),并作出其随反应温度(T)变化的关系图,请作出平衡时混合气体的平均相对分子质量随反应温度(T)的变化示意图。____________________________
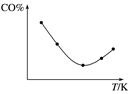
-
高炉炼铁是现代钢铁生产的重要环节,此法工艺简单,产量大,能耗低,仍是现代炼铁的主要方法,回答下列问题:
(1)已知炼铁过程的主要反应为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H1
还会发生3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=a kJ/mol;
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H3=b kJ/mol;
FeO(s)+CO(g)=Fe(s)+ CO2(g) △H4=c kJ/mol;
则△H1=________kJ/mol(用含a、b、c的代数式表示)。
(2)高炉炼铁产生的废气(CO、CO2)有多种处理方法,反应原理如下:
①生成甲醇:CO(g)+2H2(g) CH3OH(l)。一定温度下在恒容密闭容器中模拟此反应,下列化学反应速率最快的是_______________
CH3OH(l)。一定温度下在恒容密闭容器中模拟此反应,下列化学反应速率最快的是_______________
A.υ(CO)=1.2 mol/(L·min) B.υ(H2)=0.025 mol/(L·s) C.υ(CH3OH)=1 mol/(L·min)
②生成乙烯:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)。在两个容积相同的密闭容器中以不同的氢碳比[n(H2):n(CO2)]充入原料气,CO2平衡转化率α(CO2)与温度的关系如图所示
C2H4(g)+4H2O(g)。在两个容积相同的密闭容器中以不同的氢碳比[n(H2):n(CO2)]充入原料气,CO2平衡转化率α(CO2)与温度的关系如图所示
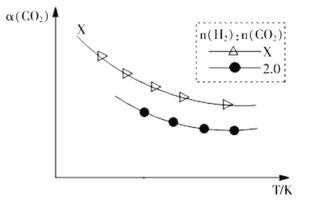
氢碳比X_____2.0(填>、<或=,下同),理由是___________________。
(3)反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),其化学平衡常数K与温度T关系如表:
CH3OH(g)+H2O(g),其化学平衡常数K与温度T关系如表:
| T/℃ | 700 | 800 | 1000 | 1200 |
| K | 0.6 | 1.0 | 2.3 | 3.6 |
①该反应是___________反应(填“吸热”或“放热”)。
②若某恒定温度下,向容积为1 L的恒容密闭容器中充入2 mol CO2、3 mol H2,10 min后反应达到平衡状态,测得υ (CH3OH)=0.075 mol/(L·min),则此反应条件下温度______800℃(填>、<或=)。
③若反应在1200℃进行试验,某时刻测得反应容器中各物质浓度满足关系式2c(CO2)·c3(H2)=3c(CH3OH)·c(H2O),此时反应在________向进行(填“正”或“逆”)。
2Fe(s)+3CO2(g)△H1
4Fe(s)+3CO2(g)的△H=____________(请用含△H1、△H2或H3的式子表示)。


