半导体工业中,有一句行话:“从沙滩到用户”,即由SiO2制Si。制取过程中不涉及到的化学反应是( )
A. SiO2+2CSi+2CO↑
B. SiO2+2NaOH=Na2SiO3+H2O
C. Si+2Cl2SiCl4
D. SiCl4+2H2Si+4HCl
高一化学单选题中等难度题
半导体工业中,有一句行话:“从沙滩到用户”,即由SiO2制Si。制取过程中不涉及到的化学反应是( )
A. SiO2+2CSi+2CO↑
B. SiO2+2NaOH=Na2SiO3+H2O
C. Si+2Cl2SiCl4
D. SiCl4+2H2Si+4HCl
高一化学单选题中等难度题
半导体工业中,有一句行话:“从沙滩到用户”,即由SiO2制取Si。制取过程中不涉及的化学反应是( )
A.2C+SiO2Si+2CO↑ B.SiO2+2NaOH=Na2SiO3+H2O
C.Si+2Cl2SiCl4 D.SiCl4+2H2
Si+4HCl
高一化学单选题简单题查看答案及解析
半导体工业中,有一句行话:“从沙滩到用户”,即由SiO2制Si。制取过程中不涉及到的化学反应是( )
A. SiO2+2CSi+2CO↑
B. SiO2+2NaOH=Na2SiO3+H2O
C. Si+2Cl2SiCl4
D. SiCl4+2H2Si+4HCl
高一化学单选题中等难度题查看答案及解析
在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4 SiCl4+2H2=Si(纯)+4HCl。若在25℃101KPa条件下反应生成HCl气体49L(注:25℃101KPa条件下气体摩尔体积为24.5L/mol)则:
(1)反应生成HCl气体的质量为__________,转移电子的个数为_____________。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为 。
(3)“从沙滩到用户”涉及到多个反应,其中制取粗硅的反应方程式为 ,纯净的石英砂与烧碱反应可以制得水玻璃,反应的离子方程式为 。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O 13%,CaO 11.7%,SiO2 75.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需要上述原料的质量是 t(保留两位小数)。
高一化学填空题困难题查看答案及解析
在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl。
若在25℃、101kPa条件下反应生成HCl气体49L,(注:25℃、101kPa条件下气体摩尔体积为24.5L•mol-1)则:
(1)反应生成HCl气体的质量为__,转移电子的总数为___。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g•mL-1的盐酸,此盐酸的物质的量浓度为___。
(3)“从沙滩到用户”涉及多个反应,其中制取粗硅的反应方程式为___。纯净的石英与烧碱反应可以制得水玻璃,反应的离子方程式为__。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O13%,CaO11.7%,SiO275.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需耍上述原料的质量是___t。(保留两位小数)
高一化学计算题中等难度题查看答案及解析
在半导体工业中有这样一句话:“从沙滩到用户”,其中一种工艺流程示意图如下:
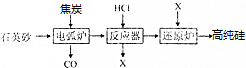
(1)焦炭的作用是 .
(2)已知反应器中的生成物有SiCl4、SiH2Cl2、SiH3Cl等,其中主产物的氯元素的质量百分含量为78.6%.则反应器中主要发生的化学反应方程式为 ,每生成 0.5molX,转移的电子物质的量为 mol.
(3)流程中可供循环使用的物质有 等(填化学式),它们也可以由 工业提供.
(4)以石英砂和 、 等为原料还可以制普通玻璃.
高一化学填空题困难题查看答案及解析
下列说法不正确的是( )
A. Si是常用的半导体材料,可以制作光电池
B. 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通足量的CO2
C. 二氧化硅不与任何酸反应,可用石英制造耐酸容器
D. 不能用石英坩埚加热熔化氢氧化钠固体
高一化学单选题中等难度题查看答案及解析
半导体工业用石英砂作原料通过三个重要反应生产单质硅。
①SiO2(s)(石英砂)+2C(s)═Si(s)(粗硅)+2CO(g) △H=+682.44kJ•mol-1
②Si(s)(粗硅)+2Cl2(g)═SiCl4(l) △H2=-657.01kJ•mol-1
③SiCl4(l) +2Mg(s)═2MgCl2(s)+Si(s)(纯硅)△H3=-625.63kJ•mol-1
生产1.00kg纯硅放出的热量为
A. 24372.86 kJ B. 21.44 kJ C. 600.20 kJ D. 21435.71 kJ
高一化学选择题简单题查看答案及解析
半导体工业用石英砂作原料通过三个重要反应生产单质硅。
①SiO2(s)(石英砂)+2C(s)═Si(s)(粗硅)+2CO(g) △H=+682.44kJ•mol-1
②Si(s)(粗硅)+2Cl2(g)═SiCl4(l) △H2=-657.01kJ•mol-1
③SiCl4(l)+2Mg(s)═2MgCl2(s)+Si(s)(纯硅)△H3=-625.63kJ•mol-1
生产1.00kg纯硅放出的热量为
A. 24372.86 kJ B. 21.44 kJ C. 600.20 kJ D. 21435.71 kJ
高一化学选择题简单题查看答案及解析
工业上利用硅的氧化物制取硅单质,主要反应为:SiO2 + 2C Si + 2CO↑。该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了2 mol C,则生成 _____mol Si,转移电子的物质的量为 mol。
高一化学填空题中等难度题查看答案及解析
硅是重要的无机非金属材料,工业上从硅的氧化物制取硅单质的主要反应为SiO2+2C=Si+2CO↑。其中,其中硅元素的化合价_______(填“升高”或“降低”),氧化剂是_____(填化学式),被氧化的物质是____(填化学式);若反应中消耗了2molC,则生成_____molSi。
高一化学填空题简单题查看答案及解析