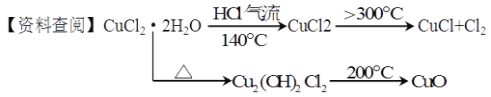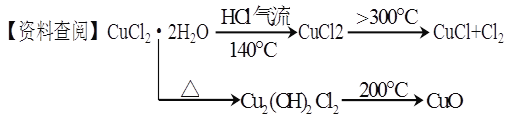-
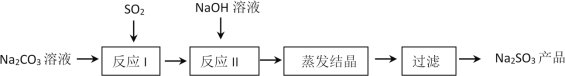
亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:

(1)SO2对环境的危害主要是形成 。
(2)用Na2CO3溶液能吸收SO2的原因是 。
(3)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中发生如下反应:
①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
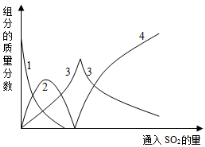
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为 (填化学式)。
(4)实验时,“反应II”中加入NaOH溶液的目的是 (用化学方程式表示)。
(5)获得的Na2SO3产品久置后质量变重,主要原因是 。
-
亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:
查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如下图是所示。

(1)如图中的线2表示的组分为____________(填化学式)
(2)写出如图曲线4的反应方程式:__________________________
(3)实验时,“反应Ⅱ”中加入NaOH溶液的目的是_______________________(用化学方程式表示)
(4)国家标准规定产品中Na2SO3的质量分数≥97.0%为优等品,≥93.0%为一等品。为了确定实验所得产品的等级,研究小组采用了下列方法进行测定。
称取2.570g产品,用蒸馏水溶解,加入足量的双氧水使Na2SO3完全氧化生成Na2SO4,再加入过量的BaCl2溶液,所得沉淀经过滤、洗涤、干燥后称重,质量为4.660g,通过计算确定产品中Na2SO3的质量分数(写出计算过程)。_________________
-
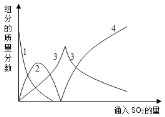
亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:
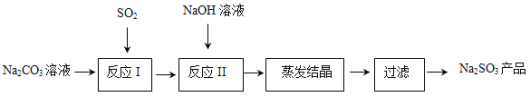
查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如右图是所示。
(1)下图中的线表示的组分为__________(填化学式)。
(2)实验时,“反应Ⅱ”中加入NaOH溶液的目的是____________________(用化学方程式表示)。
(3)国家标准规定产品中Na2SO3的质量分数≥97.0%为优等品,≥93.0%为一等品。为了确定实验所得产品的等级,研究小组采用了两种方法进行测定。
①方法Ⅰ: 称取2.570 g产品,用蒸馏水溶解,加入足量的双氧水使Na2SO3完全氧化生成Na2SO4,再加过量的BaCl2溶液,所得沉淀经过滤、洗涤、干燥后称重,质量为4.660 g。请通过计算确定产品中Na2SO3的质量分数(写出计算过程)__________。
②方法Ⅱ:称取1.326 g产品,配成100mL溶液。取25.00mL该溶液,滴加0.1250mol·L-1 I2 溶液,恰好使Na2SO3完全氧化生成Na2SO4时,消耗I2溶液20.00 mL。请通过计算确定产品中Na2SO3的质量分数(写出计算过程)__________。
③试判断Na2SO3产品的等级,并说明理由__________。
-
亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:
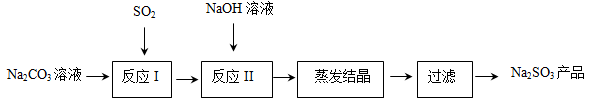
查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如右图是所示。

(1)上图中的线3表示亚硫酸钠,则线2表示的组分为 (填化学式)
(2)实验时,“反应II”中加入NaOH溶液的目的是 (用化学方程式表示)
(3)国家标准规定产品中Na2SO3的质量分数≥97.0%为优等品,≥93.0%为一等品。为了确定实验所得产品的等级,研究小组采用了两种方法进行测定。
①方法I:称取2.570g产品,用蒸馏水溶解,加入足量的双氧水使Na2SO3完全氧化生成Na2SO4,在加入过量的BaCl2溶液,所得沉淀经过过滤、洗涤、干燥后称量,质量为4.660g,通过计算确定产品中Na2SO3的质量分数(写出计算过程)
②方法II:称取1.326g产品,配成100mL溶液,取25.00mL该溶液,滴加0.1250mol/L I2溶液,恰好使Na2SO3完全氧化生成Na2SO4时,消耗I2溶液20.00mL。通过计算确定产品中Na2SO3的质量分数(写出计算过程)
③判断Na2SO3产品的等级,并说明理由 。
-
“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下,下列说法正确的是
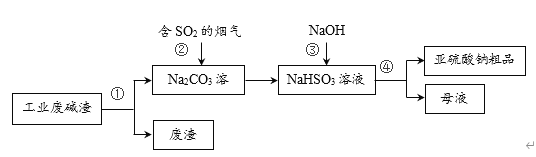
A.操作①、④均为过滤
B.步骤②中发生了置换反应
C.步骤③发生的反应为:NaHSO3+NaOH = Na2SO3+H2O
D.亚硫酸钠粗品中不可能含有Na2SO4
-
CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
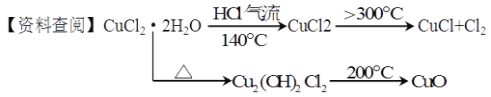
(实验探究)该小组用下图所示装置进行实验(夹持仪器略)。
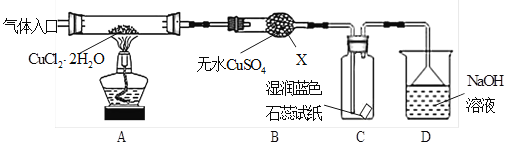
请回答下列问题:
(1)仪器X的名称是___。
(2)实验操作的先后顺序是 ______
______ (填操作的编号)。
(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是_______________。
(4)装置D中发生的氧化还原反应的离子方程式是___________________。
(探究反思)
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息
①若杂质是CuCl2,则产生的原因是_____________________________。
②若杂质是CuO,则产生的原因是________________________________。
-
CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解结晶水合物CuCl·2H2O制备CuCl,并进行相关探究。
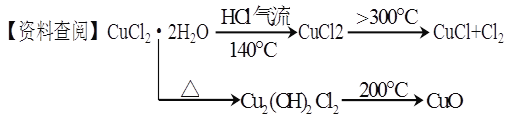
【实验探究】该小组用下图所示装置进行实验(夹持仪器略)。
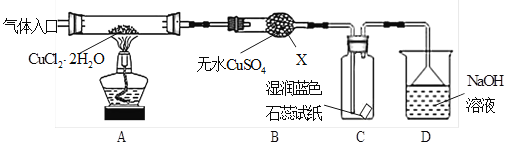
请回答下列问题:
(1)仪器X的名称是 。
(2)实验操作的先后顺序是
 (填操作的编号)。
(填操作的编号)。
a.检查装置的气密性后加入药品
b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl
d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是 。
(4)装置D中发生的氧化还原反应的离子方程式是 。
【探究反思】
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是 。
②若杂质是CuO,则产生的原因是 。
-
“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。它的制备流程如下:
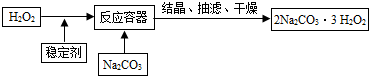
请回答下列问题:
(1)H2O2在催化或受热条件下易分解,其化学方程式为: ;在上述流程中加入稳定剂的作用是: ;
(2)在“过碳酸钠”中加入下列物质时,不会导致其变质的是 (填序号)
A、二氧化锰 B、稀硫酸 C、硫酸钠 D、石灰水
(3)在制取步骤“洗涤”中,通常采用无水乙醇而不用水洗涤,你认为可能的原因是: ;
(4)某化学学习小组为了定性探究铁离子对过碳酸钠的不良影响,取其水溶液100ml,加入25gFeCl3固体,产生大量无色无味的气体(已排除H2的可能),请选用下列试剂和实验用品完成对气体成分的探究过程:10%NaOH溶液、60%NaOH溶液、氯化钙溶液,稀氢氧化钡溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:
假设1:气体只有O2;
假设2:气体只有CO2
假设3: ;
②设计方案:针对假设1,设计实验方案证明你的假设,在下表中完成实验步骤、预期现象和结论:
| 实验步骤 | 预期现象与结论 |
| 将气体依次通过盛有 、 的洗气瓶中, 。 | 如 、 则假设1成立。 |
-
利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的流程如下:
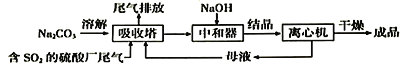
下列说法错误的是( )
A. 向大气中排放SO2可能导致酸雨发生
B. 中和器中发生反应的离子方程式为HSO3-+OH-= SO32-+H2O
C. 检验Na2SO3成品中是否含Na2SO4,可选用稀盐酸和Ba(NO3)2溶液
D. 进入离心机的分散系是悬浊液
-
利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的流程如下:
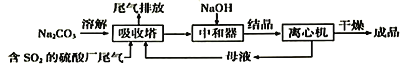
下列说法错误的是( )
A. 向大气中排放SO2可能导致酸雨发生
B. 中和器中发生反应的离子方程式为HSO3-+OH-= SO32-+H2O
C. 检验Na2SO3成品中是否含Na2SO4,可选用稀盐酸和Ba(NO3)2溶液
D. 进入离心机的分散系是悬浊液