-
某化学兴趣小组为验证SO2的还原性和Fe3+的氧化性,特邀你参与以下探究活动。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的
(1)确定选择SO2和FeCl3溶液的反应而不选择SO2和Fe(NO3)3溶液的反应来探究,你认为可能是基于什么原因作出的选择:_______________________________________。
(2)将SO2通入FeCl3溶液中,你认为可能观察到的现象是:______________________,你预测的理论依据是(用离子方程式表示):___________________________________。
II.实验探究
(1)配制1mol·L-1FeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:_________。
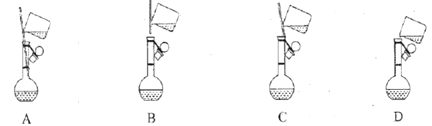
②检测得知溶液呈酸性,其原因是:___________________________(用离子方程式表示)。
(2)将SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知:[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:_____________________________________。
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2,溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。请你推测小组在实验方案设计中“加浓HCl酸化”的目的是:_____________________________________________________。
-
某化学兴趣小组为验证SO2的还原性,特邀你参与以下探究活动。
I.理论预测
该兴趣小组实验实施前进行了充分的讨论交流,确定选择SO2和FeCl3溶液的反应来探究,并预测将SO2通入FeCl3溶液中的现象。小组同学想听听你的分析,你认为可能观察到的现象是:_____________,你预测的理论依据是(用离子方程式表示):________________________。
II.实验探究
(1)配制1mol/LFeCl3溶液(未用盐酸酸化)
①下面是小组四位同学在配制溶液时的“转移”操作,其中正确的是:_______________。
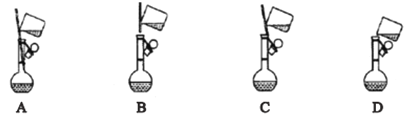
②测溶液的pH得知溶液呈酸性,其原因是:____________________ (用离子方程式表示)。
(2)SO2通入FeCl3溶液至饱和,观察到溶液由棕黄色变为红棕色,并没有观察到预期的现象。将反应后的溶液放置12小时后又出现了预期的结果。
查阅资料得知[Fe(HSO3)]2+为红棕色,生成[Fe(HSO3)]2+的反应为可逆反应。请你用化学方程式解释将SO2通入FeCl3溶液至饱和时观察到的现象:_______________。
(3)为了探究如何缩短红棕色变为预期颜色的时间,小组继续探究:另取少量FeCl3溶液,再通入SO2溶液变为红棕色,加浓HCl酸化,几分钟后变为预期颜色。
请你推测小组在实验方案设计中“加浓HC1酸化”的目的是:_______________。
III.感悟与分享
通过探究,小组同学深受启发、感悟良多。比如,有同学认为“实验才是化学的最高法庭”。请写出一种你的感悟与同学分享:______________________。
-
某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示:
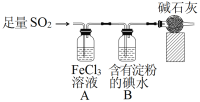
(1)装置A中的实验现象是____,B中反应的离子方程式是____。
(2)为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿色,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案中不合理的方案是______,原因是_____。
-
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示。下列说法不合理的是
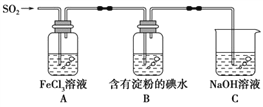
A. 为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫红色褪去
B. 能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
C. 装置C的作用是吸收SO2尾气,防止污染空气
D. 为了验证A中发生了氧化还原反应,加入稀盐酸酸化的BaCl2溶液,产生白色沉淀
-
(14分)硫是一种生命元素,组成某些蛋白质时离不开它。SO2是硫的一种重要氧化物,为探究SO2的性质,某化学兴趣小组的同学设计了如下系列实验:
(1)为验证SO2具有还原性。将SO2气体通入溴水中,溴水褪色。写出反应的化学方程式 。
(2)已知SO2与Na2O2的反应为进一步探究Na2O2与SO2的反应,用如图所示装置进行实验。
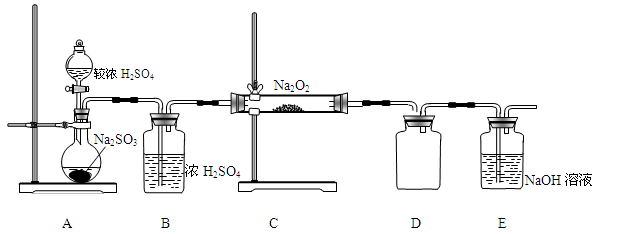
①写出A中反应的化学方程式 。
②B装置的作用是 。
③在F处检验到有O2生成,据此甲同学认为Na2O2与SO2发生了反应,反应的化学方程式为 。
④乙同学认为Na2O2与SO2反应除生成Na2SO3和O2外,还有Na2SO4生成,为检验是否有Na2SO4生成,他们设计了如下实验方案。
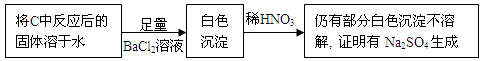
上述方案 (“合理”或“不合理”),简要说明理由 。
⑤E装置中溶液呈碱性,为检验吸收液中其他阴离子,完成下列实验方案。
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量吸收液于试管中滴加BaCl2溶液至过量 | 白色浑浊 | |
| 固体部分溶解,产生气泡 |
-
SO2是无色有刺激性气味的有毒气体,是一种主要的气态污染物.某化学兴趣小组拟对SO2的化学性质和用途进行探究.

(1)根据SO2中S元素的化合价,预测并通过实验验证SO2的性质.探究过程实验装置如图1所示(夹持仪器省略).
①A中发生反应的离子方程式为 .B中溶液可验证SO2具有 性,若C中的是品红溶液,设计该装置的实验目的是 .
②在上述装置中通入过量的SO2,为了验证A中发生了氧化还原反应,取A中溶液分成两份,并设计了如下实验:
方案一:往第一份试液中加入少量酸性KMnO4溶液,紫红色褪去;
方案二:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
上述方案不合理的是 ,原因是 .
(2)二氧化硫通常作为保护剂添加到葡萄酒中,有杀菌、抗氧化、改善风味和增酸的作用,但吸入过量的二氧化硫对人体有害.我国国家标准规定葡萄酒中SO2的最大使用量为0.25g/L.图2为该小组对葡萄酒中的SO2进行收集与测量的装置.
①仪器C的名称是 .
②A中加入200.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应.
③除去B中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,
滴定至终点时,消耗NaOH溶液20.00mL,该葡萄酒中SO2含量为 g/L.该测定结果比实际值偏高,原因是
(3)该小组同学设想将SO2生产硫酸的反应设计成原电池(如图3),并采用串联方式来电解处理工业制硝酸尾气中的NO,可制得副产品NH4NO3.已知:每个电池中通入SO2的体积均为33.6L(标准状况),且反应完全.则电池中负极的电极反应式为 ,电解池中阳极的电极反应式为 ,理论上最多能生成的NH4NO3的物质的量为 .
-
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
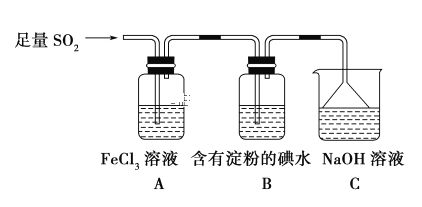
(1)装置C的作用是 ______________________。
(2)在上述装置中通入过量的SO2,请设计实验验证A中SO2与Fe3+发生了氧化还原反应: __________________。
(3)通入气体后B装置中观察到的现象是_____________。
-
(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
| 物质 | 类别 | 化学性
质预测 | 实验验证(仪器:试管、胶头滴管) |
| 实验操作 | 现象 | 实质(离子方程式表示) |
| SO2 | 酸性氧化物 | 可以和水反应 | 将盛满二氧化硫气体的试管倒立在水中,并测定试管中溶液的pH | | SO2+H2O=H2SO3 |
| 与碱反应 | | 出现白色沉淀 | |
(2)另一化学探究小组根据SO2中S元素的化合价,预测并通过实验探究验证了SO2的其它性质.探究过程中选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、酸性KMnO4溶液,品红溶液等.探究过程实验装置图如下.请你回答有关问题
①请你完成下面表格
| 装置 | 药品 | 作用 |
| B | 酸性KMnO4溶液 | 验证SO2的还原性 |
| C | | |
| D | | |
②B中反应的离子方程式为______.
③D中的现象为______.

-
(1)某化学探究小组对SO2的化学性质进行以下探究并写如下实验报告.请帮助他完成实验报告
| 物质 | 类别 | 化学性
质预测 | 实验验证(仪器:试管、胶头滴管) |
| 实验操作 | 现象 | 实质(离子方程式表示) |
| SO2 | 酸性氧化物 | 可以和水反应 | 将盛满二氧化硫气体的试管倒立在水中,并测定试管中溶液的pH | | SO2+H2O=H2SO3 |
| 与碱反应 | | 出现白色沉淀 | |
(2)另一化学探究小组根据SO2中S元素的化合价,预测并通过实验探究验证了SO2的其它性质.探究过程中选用的实验药品有浓硫酸、Na2SO3固体、Na2S溶液、酸性KMnO4溶液,品红溶液等.探究过程实验装置图如下.请你回答有关问题
①请你完成下面表格
| 装置 | 药品 | 作用 |
| B | 酸性KMnO4溶液 | 验证SO2的还原性 |
| C | | |
| D | | |
②B中反应的离子方程式为______.
③D中的现象为______.
-
某化学探究小组欲对SO2的化学性质进行如下探究,请你帮助他完成实验报告。
| 物质 | 类别 | 化学性 质预测 | 实验验证 |
| 实验操作 | 实验现象 | 实质(用离子 方程式表示) |
| 二氧 化硫 | 酸性 氧化物 | 与水 反应 | 将盛满SO2气体的试管倒立在水中,并测定试管中溶液的pH | ① | SO2+H2O  H2SO3 H2SO3
|
| 与碱 反应 | ② | 出现白 色沉淀 | ③ |
| | | | | |
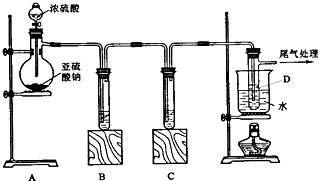
(2)该探究小组还根据SO2中S元素的化合价,预测并通过实验探究SO2的其他性质。探究过程中选用的实验药品有:浓硫酸、亚硫酸钠固体、Na2S溶液、酸性高锰酸钾溶液、品红溶液等。探究过程的实验装置图如图所示,请回答下列问题。
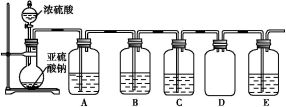
①请你完成下列表格。
| 装置 | 药品 | 作用 |
| A | | 验证二氧化硫的还原性 |
| B | | |
| C | 品红溶液 | |
②A中发生反应的离子方程式为 。
③实验时C中的实验现象是 。
④D装置的作用是 。E是尾气处理装置,有人认为E装置中可以加入足量的Ba(NO3)2溶液,你认为是否合理,请结合离子方程式加以说明: 。










