-
工业上从海水中提取溴单质时,可用纯碱溶液吸收空气吹出的溴,发生反应:
(I )3Br2+3Na2CO3===5NaBr+NaBrO3+3CO2;
(II )5NaBr+NaBrO3 +3H2SO4 ===3Na2SO4 +3Br2+3H2O
下列有关判断正确的是
A. 反应I中氧化剂与还原剂的物质的量之比为1:1
B. 溴元素由化合态转化成游离态时一定发生了还原反应
C. 反应Ⅱ中生成3 mol Br2时,必有5 mol电子转移
D. 氧化还原反应中化合价变化的元素一定是不同种元素
高三化学单选题中等难度题查看答案及解析
-
工业上制备溴单质时常用纯碱溶液吸收溴,发生的反应为:
3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3,下列有关说法正确的是
A.上述反应若有0.9molBr2反应,转移电子为1.5×6.02×1023个
B.反应后溶液的PH增大
C.若将NaBr和NaBrO3转变为Br2,需要在碱性条件下进行
D.该反应Na2CO3既是氧化剂又是还原剂
高三化学选择题中等难度题查看答案及解析
-
从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4===3Br2+3Na2SO4+3H2O,与上述反应在氧化还原原理上最相似的是( )
A.2NaBr+Cl2===2NaCl+Br2
B.AlCl3+3NaAlO2+6H2O===4Al(OH)3↓+3NaCl
C.2H2S+SO2===2H2O+3S↓
D.2FeCl3+H2S===2FeCl2+S↓+2HCl
高三化学选择题中等难度题查看答案及解析
-
在海水中提取溴的反应原理是5NaBr+NaBrO+3H2SO4=3Br2 +3Na2SO4+ 3H2O下列反应的原理与上述反应最相似的是( )
A.2NaBr+Cl2=2NaCl+Br2
B.2FeCl3+H2S=2FeCl2+S+2HCl
C.2H2S+SO2=3S+2H2O
D.AlCl3+3NaAlO3+6H2O=4Al(OH)3+3NaCl
高三化学单选题简单题查看答案及解析
-
从海水里提取溴的过程中,有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O。与上述反应在原理上最相似的反应是
A.2NaBr+Cl2=Br2+2NaCl
B.2KI+Br2=I2+2KBr
C.2H2S+SO2=3S+2H2O
D.Cl2+H2O=HCl+HClO
高三化学选择题简单题查看答案及解析
-
工业上利用空气吹出法提取溴的部分流程如下:
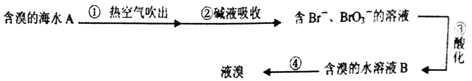
下列说法错误的是( )
A. ②中可以采用纯碱溶液,发生的反应是:3Br2+6CO32-+3H2O =5Br-+BrO3-+6HCO3-
B. 第③步,需加入氧化性酸,才能将Br-氧化为Br2
C. B溶液颜色要比A 溶液深
D. 第④步,采用的是蒸馏的方法
高三化学选择题中等难度题查看答案及解析
-
工业上利用空气吹出法提取溴的部分流程如下:
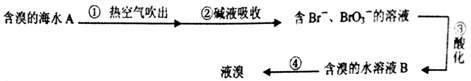
下列说法错误的是( )
A.②中可以采用纯碱溶液,发生的反应是:3Br2+6CO32-+3H2O =5Br-+BrO3-+6HCO3-
B.第③步,需加入氧化性酸,才能将Br-氧化为Br2
C. B溶液颜色要比A 溶液深
D.第④步,采用的是蒸馏的方法
高三化学选择题中等难度题查看答案及解析
-
工业上利用空气吹出法提取溴的部分流程如下:
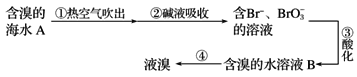
下列说法错误的是
A. ②中可以采用纯碱溶液,发生的反应是3Br2+6CO32—+3H2O=5Br-+BrO3—+6HCO3—
B. 第③步,需加入氧化性酸,才能将Br-氧化为Br2
C. B溶液颜色要比A溶液深
D. 第④步,采用的是蒸馏的方法
高三化学单选题中等难度题查看答案及解析
-
海水提溴过程中发生反应:3Br2 +6Na2CO3 +3H2O=5NaBr +NaBrO3 +6NaHCO3,下列说法正确的是
A.标准状况下 2 mol H2O 的体积约为 44.8 L
B.0.1 mol·L− 1Na2CO3 溶液中 CO3 2−的物质的量为 0.1 mol
C.反应中消耗 3 mol Br2 转移的电子数约为 5×6.02×1023
D.反应中氧化产物和还原产物的物质的量之比为 5∶1
高三化学单选题中等难度题查看答案及解析
-
(本题共14分)
溴化钠是工业提溴的中间产物,也是重要的化工生产原料,回答下列问题。
56.工业上用氯气氧化卤水中的溴离子,吹出溴蒸气后用10% 的纯碱溶液吸收,反应的化学方程式为:
3Na2CO3+ 3Br2 → 5NaBr + NaBrO3 + 3CO2若生成标准状况下3.36 L CO2,吸收的Br2为________g。
57.吹出的溴蒸气中会含有少量未反应的氯气,用纯碱吸收后实际生成的是NaCl、NaBr和NaBrO3。若所得溶液中含0.1 mol NaCl与0.6 mol NaBr,则溶液中NaBrO3的物质的量为_______mol。
58.将纯碱吸收后所得的溶液浓缩,加入2 mol/L H2SO4后蒸馏可以回收纯溴:
5NaBr + NaBrO3 + 3H2SO4 → 3Na2SO4+ 3Br2↑+ 3H2O
已知向一定质量的浓缩液中加入300mL硫酸可回收81.6 g液溴,硫酸全部转化为硫酸钠。若改为加入180 mL硫酸,计算可回收的液溴的质量。
59.向0.3 mol NaBr固体中加入足量浓硫酸并微热,产生的气体呈红棕色,且残留物中不含溴元素。将所得气体通入280 mL 2 mol/L的Na2SO3溶液中,无任何气体逸出,最终得到只含NaBr、Na2SO4和NaHSO3三种溶质的无色溶液。求红棕色气体中各组分的化学式与物质的量。
高三化学计算题困难题查看答案及解析