-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
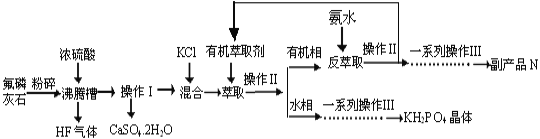
已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是________________。

(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):

已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______kg。
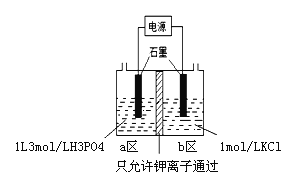
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是________________。
(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):

已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是________________。

(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
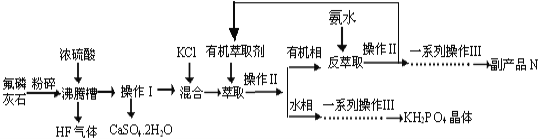
已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是____________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括____________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12,摩尔质量为504g/mol)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4(摩尔质量为136g/mol)的质量为_______kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是________________。

(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
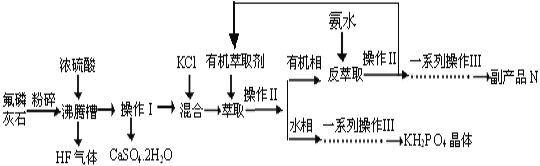
已知萃取的主要反应原理:KCl+H3PO4 KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是___________________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括______________________________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4的质量为_______kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是______________________________________。
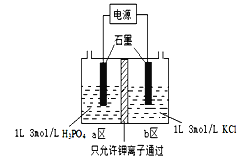
(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
-
据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。 某兴趣小组制备 KH2PO4,流程如下:
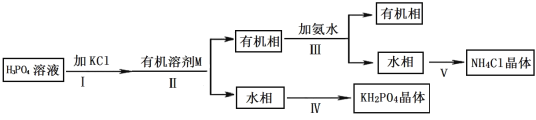
已知:
a.KH2PO4 有潮解性,溶于水,不溶于乙醇和醚等有机溶剂。
b.HCl 易溶于乙醇和醚等有机溶剂。
请回答:
(1)步骤Ⅱ的实验操作是_____。
(2)有关步骤Ⅲ,下列说法正确的是_____。
A.有机溶剂 M 可用乙醇
B.步骤Ⅲ与步骤Ⅱ的实验操作基本相同
C.NH4Cl 在水中溶解度明显大于在有机溶剂 M 中
D.有机溶剂 M 可循环使用
(3)试从平衡角度分析,由步骤Ⅰ、Ⅱ得到 KH2PO4 溶液的原理:_____。
(4)在下列仪器中,使用前需进行“检漏”操作的是_____。
A.吸滤瓶 B.球型分液漏斗 C.蒸馏烧瓶 D.碱式滴定管
(5)步骤Ⅳ,包括蒸发浓缩、冷却结晶、过滤、干燥等多步操作。在冷却结晶操作中,为了得到 磷酸二氢钾大晶体,常采取的措施有____________________。某同学发现使用加热浓缩、冷却结晶得到的磷酸二氢钾晶体欠佳,请提出针对性的改进实验方案:_____________,然后经过滤、干燥得到晶体。
-
磷酸二氢钾(KH2PO4)可应用于我国研制的巨型激光器“神光二号”中。一种利用氟磷灰石[Ca5(PO4)3F]制备磷酸二氢钾的工艺流程如图所示(部分流程步骤已省略):

已知:KCl+H3PO4 KH2PO4+HCl,其中HCl易溶于有机萃取剂。
KH2PO4+HCl,其中HCl易溶于有机萃取剂。
请回答下列问题:
(1)写出氟磷灰石在高温下与SiO2,C反应的化学方程式__。
(2)副产品M的化学式是__,写出它的一种用途__;在由水层得到KH2PO4晶体时需要进行的一系列操作,其主要包括__、过滤、洗涤、干燥等。
(3)从化学平衡角度分析,KCl和H3PO4反应制备KH2PO4时使用有机萃取剂的原因是___。
(4)为避免水体富营养化,废水中的KH2PO4要先处理达标后再排放。处理废水有两种方法。
①沉淀法:将石灰投加到待处理的废水中,将磷元素全部转化成磷酸钙,从而进行回收。已知常温下Ksp[Ca3(PO4)2]=2.0×10-29,当处理后的废水中c(Ca2+)=1.0×10-3mol•L-1时,溶液中c(PO43-)=__mol•L-1。
②电渗析法:用电渗析法从废水中提取KOH和H3PO4,装置如图所示。下列说法正确的是___(填字母)。

A.膜1为阳离子交换膜,y为正极
B.c为稀KOH溶液,b为浓H3PO4溶液
C.阳极反应式为2H2O+2e-=2OH-+H2↑
D.每转移0.1mol电子时理论上可以获得9.8gH3PO4
-
(1)已知4g甲烷气体充分燃烧生成CO2(g)和H2O(l)时,放出Q kJ的热量.甲烷燃烧的热化学方程式为______.
(2)我国自行研制的优质磷酸二氢钾(KDP)晶体被应用于大功率固体激光器中.反应方程式为H3PO4(aq)+KCl(aq) KH2PO4(aq)+HCl(aq),当反应时间不同时,产品产率和产品中Cl‑含量变化情况如图所示.KDP晶体的一级品标准:Cl-质量分数低于0.2%.
KH2PO4(aq)+HCl(aq),当反应时间不同时,产品产率和产品中Cl‑含量变化情况如图所示.KDP晶体的一级品标准:Cl-质量分数低于0.2%.
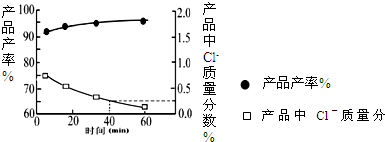
由图中可知,当反应进行到约______min时,KDP晶体达到一级品标准,此时的产品产率约为______.
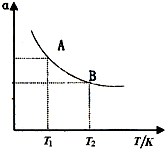
(3)如图在一定条件下,将1mol N2与3mol H2混合于一个10L密闭容器中,反应达到A平衡时,混合气体中氨体积分数为25%,试回答:
①N2的转化率αA为______;
②在状态A时,平衡常数KA=______(代入数值即可)当温度由T1变到T2时,KA______KB(填“>”、“<”或“=”);
(4)向20.00mL稀氨水中逐滴加入等物质的量浓度的盐酸,请回答相关问题:
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c______>c______>c______>c______
②当盐酸与氨水等物质的量反应时,溶液的pH______7(填“>”或“<”或“=”,下同)
③当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为:n______n(HCl),溶液中c( NH4+)______c(Cl-).
-
我国自行研制的优质磷酸二氢钾(KDP)晶体被应用于大功率固体激光器中.现以氯化钾和磷酸为原料制取磷酸二氢钾,反应方程式为:H3PO4(aq)+KCl(aq)⇌KH2PO4(aq)+HCl(aq),以下是在三正丁胺中制备磷酸二氢钾的工艺流程:
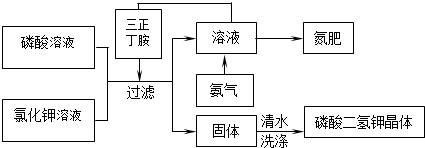
已知:三正丁胺是不溶于水的有机溶剂,与氯化氢反应生成一种可溶于水的盐,能使磷酸二氢钾在水中的溶解度降低.
(1)该流程中所获副产品氮肥的主要成份是________.
(2)使用三正丁胺能促进该反应进行的原因是________.除该方案外,促进该反应进行还可采取的措施有________.
(3)当反应时间不同时,产品产率和产品中Cl‑含量变化情况如图所示.KDP晶体的一级品标准:Cl‑质量分数低于0.2%.

由图中可知,当反应进行到约________分钟时,KDP晶体达到一级品标准,此时的产品产率约为________.
-
非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Ca2CO3, XO2(X= Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)基态硼原子的价电子排布图是____________,与硼处于同周期的非金属主族元素的第一电离能由大到小的顺序为________________。
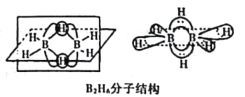
(2)B的简单氢化物BH3,不能游离存在,常倾向于形成较稳定的B2H6或与其他分子结合。
①B2H6分子结构如图,则B原子的杂化方式为____________________。
②氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______________,写出一种与氨硼烷互为等电子体的分子_________(填分子式)。
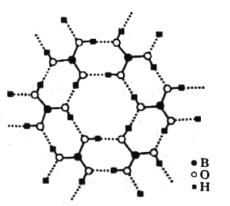
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为_______;硼酸在热水中比在冷水中溶解度显著增大的主要原因是____________。
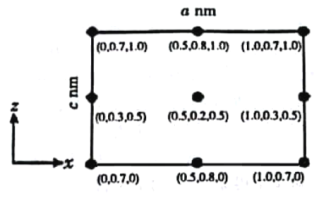
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子分数坐标。CsSiB3O7属于正交晶系(长方体形),晶胞参数为anm、bnm和cnm.如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为_________;CsSiB3O7的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为_____g·cm-3(用含字母的代数式表示)。

KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。


















