-
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol,这个热化学方程式表示
A. 2g碳燃烧生成一氧化碳时放出221.0kJ的热量
B. 2mol碳燃烧生成一氧化碳时吸收221.0kJ的热量
C. 2mol固体碳在氧气中燃烧生成2mol一氧化碳气体时放出221.0kJ的热量
D. 12g碳和氧气反应生成一氧化碳时放出221.0kJ的热量
高二化学单选题简单题查看答案及解析
-
2C(s)+O2(g)= 2CO(g)
H=-221.0 kJ·mol-1,这个热化学方程式表示( )
A. 2 g碳燃烧生成一氧化碳时放出221.0 kJ的热量
B. 2 mol碳燃烧生成一氧化碳时吸收221.0 kJ的热量
C. 2 mol固体碳在氧气中燃烧生成2 mol一氧化碳气体时放出221.0 kJ的热量
D. 12 g碳和氧气反应生成一氧化碳时放出221.0 kJ的热量
高二化学选择题简单题查看答案及解析
-
下列说法正确的是( )
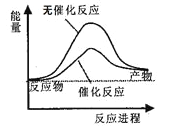
A. 如图可表示水分解过程中的能量变化
B. 若2C(s)+O2(g)=2CO(g)△=−221.0kJ/mol,则碳的燃烧热为110.5kJ/mol
C. 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D. 已知I:反应H2(g)+Cl2(g)=2HCl(g)△=−akJ/mol,II:
 且a、b、c均大于零,则断开1mol H−Cl键所需的能量为(−a−b−c)kJ/mol
且a、b、c均大于零,则断开1mol H−Cl键所需的能量为(−a−b−c)kJ/mol高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是
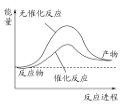
A. 上图可表示水分解过程中的能量变化
B. 若2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
C. 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D. 已知Ⅰ:反应H2(g)+Cl2(g)===2HCl(g) ΔH=-a kJ/mol
Ⅱ:

且a、b、c均大于零,则断开1 mol H—Cl键所需的能量为(a+b+c)kJ/mol
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是
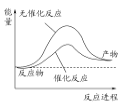
A. 上图可表示水分解过程中的能量变化
B. 若2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
C. 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D. 已知Ⅰ:反应H2(g)+Cl2(g)===2HCl(g) ΔH=-a kJ/mol
Ⅱ:

且a、b、c均大于零,则断开1 mol H—Cl键所需的能量为(a+b+c)kJ/mol
高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是

A.如图可表示水分解过程中的能量变化
B.若2C(s)+O2(g)=2CO(g) △=-221.0kJ/mol,则碳的燃烧热为110.5kJ/mol
C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D.已知I:反应H2(g)+Cl2(g)=2HCl(g) △=-akJ/mol
II:

且a、b、c均大于零,则断开1mol H—Cl键所需的能量为(-a-b-c)kJ/mol
高二化学选择题中等难度题查看答案及解析
-
根据下图所给信息,得出的结论正确的是
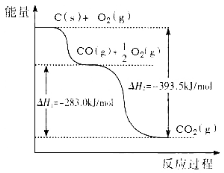
A.48g碳完全燃烧放出热量为1574 kJ/mol
B.2C(s)+O2(g)
2CO(g) △H=-221.0kJ/mol
C.2CO2(g)
2CO(g)+O2(g) △H=+283.0kJ/mol
D.C(s)+O2(g)
CO2(s) △H=-393.5kJ/mol
高二化学单选题简单题查看答案及解析
-
下列说法正确的是
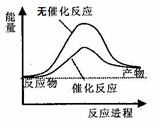
A.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
B.若 2C(s)+O2(g)=2CO(g) △H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol
C.右图可表示水分解过程中的能量变化
D.已知:Ⅰ:对于反应:H2(g)+Cl2(g)=2HCl (g) △H=-a kJ/mol,
Ⅱ:
且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为(a+b+c)kJ
高二化学选择题困难题查看答案及解析
-
.已知:①2C(s)+O2(g)====2CO(g) ΔH=-221.0 kJ·mol-1;②2H2(g)+O2(g) ====2H2O(g) ΔH=-483.6 kJ·mol-1。则反应C(s)+H2O(g) ====CO(g)+H2(g)的ΔH为( )
A.+262.6 kJ·mol-1 B.-131.3 kJ·mol-1
C.-352.3 kJ·mol-1 D.+131.3 kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
已知,在25℃、101 kPa时:① C(s)+O2(g)==CO2(g) ΔH=-393.5 kJ/mol
② 2C(s)+O2(g)==2CO(g) ΔH=-221.0 kJ/mol
③ 2H2(g)+O2(g)==2H2O(g) ΔH=-483.6 kJ/mol
下列判断不正确的是
A.6g碳完全燃烧时放出热量196.8 kJ
B.CO的燃烧热ΔH=-283.0 kJ/mol
C.H2的燃烧热ΔH=-241.8 kJ/mol
D.制备水煤气的反应热ΔH=+131.3 kJ/mol
高二化学选择题中等难度题查看答案及解析