-
工业纯碱中常含有少量NaCl,某校化学课外活动小组设计并完成了如下实验。
【实验目的】
测定工业纯碱中Na2CO3的含量。
【实验原理】
Na2CO3与酸反应生成的CO2被吸收剂吸收,通过分别称量反应前、后的U形干燥管E的总质量,求出Na2CO3的含量。
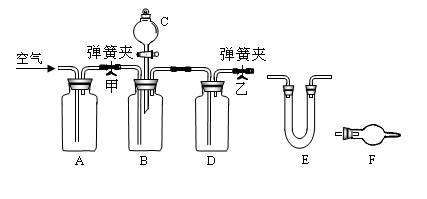 【实验装置】
【实验装置】
【实验试剂】
①NaOH溶液 ②饱和石灰水 ③碱石灰 ④无水氯化钙 ⑤无水硫酸铜
⑥浓盐酸 ⑦稀盐酸 ⑧浓硫酸 ⑨稀硫酸 ⑩试样(工业纯碱)
【实验步骤】(完成下列实验步骤)
①称量试样及装有吸收剂的E的质量,记录数据;
②如上图所示连接好装置,先检查装置的气密性;
③在有关仪器中装入适当试剂;
④打开甲、乙弹簧夹,用气卿鼓入空气,然后接上已称量过的E;
⑤;
⑥________;
⑦称量E的质量并记录数据。
(1)实验时,在仪器D中装入浓硫酸的作用是________,在仪器C中应装入的试剂是________。(填试剂序号)
(2)实验过程中,先、后共两次鼓入空气,第二次鼓入空气的目的是
。
(3)某同学认为在E装置后应再连接F装置(装有适当试剂),你认为是否必要?
________。(选填“必要”或“不必要”)
-
工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量.
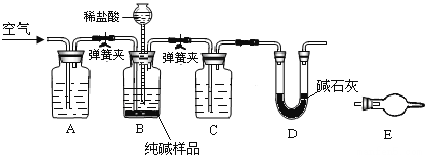
(1)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若________________,说明装置不漏气.
(2)装置A的作用是____,装置C中的试剂为___.
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?____(选填“必要”或“不必要”),判断的理由是____________________.
(4)实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为_____.
-
某小组设计如图所示装置,测定工业纯碱(含有少量NaCl)中Na2CO3的含量.

(1)检验装置B气密性:塞紧三孔橡胶塞,夹紧弹簧夹,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若________________,说明装置不漏气.
(2)装置A的作用是____,装置C中的试剂为___.
(3)某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?____(选填“必要”或“不必要”),判断的理由是____________________.
(4)实验前称取28.80g样品,实验后D装置增重8.80g,则样品中Na2CO3质量分数为_____.
-
(9分)碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀________(填操作)、洗
涤、烘干、称量.洗涤沉淀的操作是______________________________________
________________________________________________________________________.
方案二:气体分析法
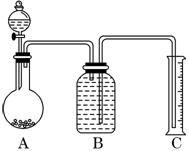
(2)把一定量的样品与足量盐酸反应后,用如图装置测定产生CO2气体的体积,为了测
定结果准确,B中的溶液最好采用________,但选用该溶液后实验结果仍然不够准确,
其原因是_______________________________________________________.
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.
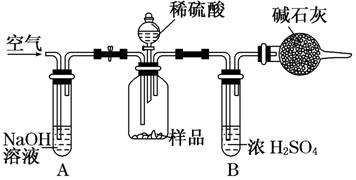
该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g ②取n g样品装入广口
瓶中 ③检验装置的气密性
④缓慢鼓入空气数分钟,再称量干燥管质量为w g ⑤关闭止水夹 ⑥打开止水夹 ⑦
缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟
Ⅰ.正确的操作顺序是(填写序号):
③→________→⑥→________→⑤→________→⑦→________→④
Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、
“偏小”或“无影响”).
-
(10分)碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀_________(填操作步骤)、洗涤、烘干、称量。洗涤沉淀的操作是________________________________。
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应后,用如图装置测
定产生CO2气体的体积,为了测定结果准确,B中
的溶液最好采用____________,从下列各选项中选
取:
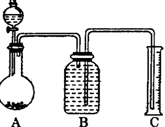
a.饱和碳酸钠溶液 b.饱和碳酸碳酸氢钠溶液.
c.饱和氢氧化钠溶液 d.饱和硫酸铜溶液。
若直接采用如图装置, 选用该溶液后实验结果仍
然不够准确,其原因可能是________________________________________。
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g ②取n g样品装入广口瓶中 ③检验装置的气密性。④缓慢鼓入空气数分钟,再称量干燥管质量为w g ⑤关闭止水夹 ⑥打并止水夹 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟。
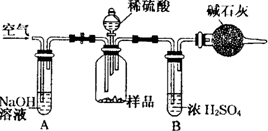
I.正确的操作顺序是(填写序号):
③→_______→⑥→________→⑤→_______→⑦→__________→④
Ⅱ.若去掉装置A,测定结果___________;若去掉装置B,测定结果__________(填“偏大”、“偏小”或“无影响”).
-
为了测定工业纯碱中Na2CO3的质量分数(含少量NaCl),甲、乙、丙三位学生分别设计了一套实验方案。
学生甲的实验流程如图所示:
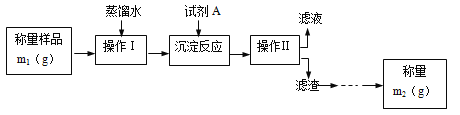
学生乙设计的实验步骤如下:
①称取样品,为1.150g;②溶解后配成250mL溶液;③取20mL上述溶液,加入甲基橙2~3滴;④用0.1140mol/L的标准盐酸进行滴定;⑤数据处理。
回答下列问题:
(1)甲学生设计的定量测定方法的名称是___法。
(2)试剂A可以选用___(填编号)
a.CaCl2 b.BaCl2 c.AgNO3
(3)操作Ⅱ后还应对滤渣依次进行①___、②___两个实验操作步骤。其中,证明前面一步的操作已经完成的方法是___;
(4)学生乙某次实验开始滴定时,盐酸溶液的刻度在0.00mL处,当滴至试剂B由___色至___时,盐酸溶液的刻度在14.90mL处,乙同学以该次实验数据计算此样品中Na2CO3的质量分数是___(保留两位小数)。乙同学的这次实验结果与老师给出的理论值非常接近,但老师最终认定他的实验方案设计不合格,你认为可能的原因是什么?___。
(5)学生丙称取一定质量的样品后,只加入足量未知浓度盐酸,经过一定步骤的实验后也测出了结果。他的实验需要直接测定的数据是___。
-
为了测定工业纯碱中Na2CO3的质量分数(含少量NaCl),甲、乙两位学生分别设计了一套方案。学生甲的实验流程如图所示:
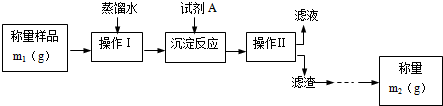
学生乙设计的实验步骤如下:
①称取样品,为1.150g;
②溶解后配成250mL溶液;
③取20mL上述溶液,加入甲基橙 2~3滴;
④用0.1140mol/L的标准盐酸进行滴定;
⑤数据处理.
回答下列问题:
(1)甲学生设计的方案中试剂A可以选用____________(填编号)
a.CaCl2 b.BaCl2 c.AgNO3
(2)操作Ⅱ后还应对滤渣依次进行①__________②__________两个实验操作步骤.其中,证明前面一步的操作已经完成的方法是_______________。
(3)学生乙某次实验开始滴定时,盐酸溶液的刻度在0.00mL处,当滴至_____________时达到滴定终点,此时盐酸溶液的刻度在14.90mL处,乙同学以该次实验数据计算此样品中Na2CO3的质量分数是___________(保留两位小数).乙同学的这次实验结果与老师给出的理论值非常接近,但老师最终认定他的实验方案设计不合格,你认为可能的原因是_________________。
-
工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取m g纯碱样品与足量稀盐酸充分反应,加热、蒸干、灼烧,得ng固体。则该样品中纯碱的质量分数为( )
A. ×100% B.
×100% B. ×100% C.
×100% C. ×100% D.
×100% D. ×100%
×100%
-
工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取a g纯碱样品与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体。则该样品中纯碱的质量分数为( )
A.  ×100% B.
×100% B.  ×100%
×100%
C.  ×100% D.
×100% D.  ×100%
×100%
-
某实验小组同学为了测定工业纯碱的纯度,进行了一系列实验。
(1)和索氏制碱法相比,侯氏制碱法的优势有___________________________________;
(2)工业纯碱中常含有少量NaCl杂质,解释原因__________________________,检验是否含有氯化钠杂质的方法为__________________________________________________________;
(3)使用重量法测定纯碱的纯度,用到的试剂有__________________________________;
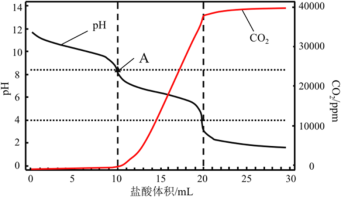
(4)使用滴定法测定纯碱的纯度,用_________________(填仪器名称)称量1.200g工业纯碱样品,溶解,用1mol/L盐酸做标准液,滴定过程中溶液pH变化和生成CO2的量如图所示,A点溶液呈碱性的原因______________________________________________________,计算该工业纯碱样品的质量分数_______________。(计算结果保留两位小数)
 。
。

 【实验装置】
【实验装置】





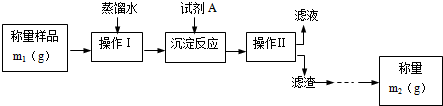
 。
。