-
已知在稀溶液里,强酸跟强碱发生中和反应生成1 mol液态水时反应热叫做中和热。现利用下图装置进行中和热的测定,请回答下列问题:
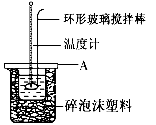
(1)图中未画出的实验器材是________________、________________。
(2)做一次完整的中和热测定实验,温度计需使用________次。
(3)实验时,将0.50 mol·L-1的盐酸加入到0.55mol·L-1的NaOH溶液中,两种溶液的体积均为50 mL,各溶液的密度均为1 g /cm3,生成溶液的比热容c=4.18 J /(g· oC),实验的起始温度为t1 oC,终止温度为t2 oC。测得温度变化数据如下:
| 序号 | 反应物 | 起始温度t1/ oC | 终止温度t2/ oC | 中和热 |
| ① | HCl+NaOH | 14.8 | 18.3 | ΔH1 |
| ② | HCl+NaOH | 15.1 | 19.7 | ΔH1 |
| ③ | HCl+NaOH | 15.2 | 18.5 | ΔH1 |
| ④ | HCl+NH3·H2O | 15.0 | 18.1 | ΔH2 |
①试计算上述两组实验测出的中和热ΔH1=______________。
②某小组同学为探究强酸与弱碱的稀溶液反应时的能量变化,又多做了一组实验④,用0.55mol·L-1的稀氨水代替NaOH溶液,测得温度的变化如表中所列,试计算反应的ΔH2=____________。
③两组实验结果差异的原因是___________________________________________。
④写出HCl+NH3· H2O反应的热化学方程式:_______________________________________。
-
已知在稀溶液中,强酸跟强碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:

(1)该图中有两处未画出,它们是______________、________________。
(2)做一次完整的中和热测定实验,温度计需使用________次。
(3)把温度为15.0 ℃,浓度为0.5 mol·L-1的酸溶液和0.55 mol·L-1的碱溶液各50 mL混合(溶液密度均为1 g·mL-1),生成溶液的比热容c=4.18 J · g-1 · ℃-1,轻轻搅动,测得酸碱混合液的温度变化数据如下:
| 反应物 | 起始温度t1/℃ | 终止温度t2/℃ | 中和热 |
| HCl+NaOH | 15.0 | 18.4 | ΔH1 |
| HCl+NH3·H2O | 15.0 | 18.1 | ΔH2 |
①计算上述第一组实验测出的中和热ΔH1=______。
②写出HCl+NH3·H2O的热化学方程式:____________________________________。
③两组实验结果差异的原因是______________________________________。
-
已知在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:
(1)图示装置有两处重要组成部分未画出,它们是____________ 、_______________。
(2)烧杯间填满碎泡沫塑料的作用是 ________________。
(3)若操作时分几次注入反应液,求得的反应热数值_____(填“偏大”“偏小”或“无影响”)。
(4)做一次完整的中和热测定实验,温度计需使用__________次。
(5)量取0.5 mol/L的盐酸和0.55 mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,生成溶液的比热容c= 4.18 J/g•℃。请列式计算中和热:△H= ______________kJ/mol(不用化简)。
-
已知在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:
(1)图示装置有两处重要组成部分未画出,它们是____________ 、_______________。
(2)烧杯间填满碎泡沫塑料的作用是 ________________。
(3)若操作时分几次注入反应液,求得的反应热数值_____(填“偏大”“偏小”或“无影响”)。
(4)做一次完整的中和热测定实验,温度计需使用__________次。
(5)量取0.5 mol/L的盐酸和0.55 mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,生成溶液的比热容c= 4.18 J/g•℃。请列式计算中和热:△H= ______________kJ/mol(不用化简)。
-
已知在稀溶液中强酸与强碱反应生成1 mol水时放出的热量,叫做中和热,下列说法中正确的是
A. 中和热的测定实验中需要用到的主要玻璃仪器有:两只大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒
B. 可以用保温杯来代替烧杯做有关测定中和热的实验
C. 在测定中和热的实验中,至少需要测定并记录的温度是2次
D. 测定中和热实验中,若所使用的稀NaOH溶液的物质的量稍大于稀盐酸,则会导致所测得的中和热数值偏高
-
已知在稀溶液中强酸与强碱反应生成1 mol水时放出的热量,叫做中和热,下列说法中正确的是
A.中和热的测定实验中需要用到的主要玻璃仪器有:两只大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒
B.可以用保温杯来代替烧杯做有关测定中和热的实验
C.在测定中和热的实验中,至少需要测定并记录的温度是2次
D.测定中和热实验中,若所使用的稀NaOH溶液的物质的量稍大于稀盐酸,则会导致所测得的中和热数值偏高
-
分别取40mL的0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题。
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式____________________;
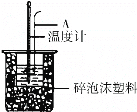
(2)如图所示,仪器A的名称是____________;烧杯间填满泡沫塑料的作用:________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H________(填“偏大”、“偏小”或“无影响”);
(3)假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g·℃)。为了计算中和热,某学生实验记录数据如下:
| 实验序号 | 起始温度t1℃ | 终止温度t2℃ |
| 盐酸 | 氢氧化钠 | 混合溶液 |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热△H=________;(结果保留一位小数)
(4)_______(填“能”或“不能”)用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是____________________。
-
分别取40 mL的0.50 mol/L盐酸与40 mL0.55 mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
(1)理论上稀强酸、稀强碱反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式______________________________
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃棒,两个小孔不能开得过大,其原因是__________________;反应需要多次测量温度,每次测量温度后在进行下一次测量以前都必须采取的操作是____________________.
(3)假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容c=4.18 J/(g·℃).为了计算中和热,实验时还需测量的数据有(填序号)__________;
A.反应前盐酸溶液的温度 B.反应前盐酸溶液的质量 C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量 E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
| 实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ |
| 盐酸 | 氢氧化钠 | 混合溶液 |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
| | | |
依据该学生的实验数据计算,该实验测得的中和热ΔH=____________;
(5)假定该学生的操作完全同上,实验中改用100 mL 0.5 mol/L盐酸跟100 mL 0.55 mol/L氢氧化钠溶液进行反应,与上述实验相比,所放出的热量_______(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”).
-
(1)稀强酸、稀强碱反应生成1mol液态水时放出57.3kJ的热量.
①实验室中可用稀盐酸和氢氧化钡稀溶液反应来测定中和热.请写出能表示该反应中和热的热化学方程式________;
②分别取100mL 0.50mol/L盐酸与100mL 0.55mol/L NaOH溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.假设盐酸和氢氧化钠溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/.实验时,测得反应前盐酸与NaOH溶液的平均温度为21.5℃,反应后混合溶液的温度为24.9℃.则实验测得的中和热△H=________(保留1位小数);
③如果用含1mol CH3COOH的稀醋酸与足量稀氢氧化钠溶液反应,反应放出的热量________57.3kJ(填“大于”、“小于”或“等于”);理由是________.
(2)在催化剂的作用下CH4还原NO可以得到三种产物(该条件下均为气体),利用此反应能消除环境污染物NO.理论上每消耗标况下22.4L NO就能放出290kJ的热量.写出该反应的热化学方程式________.
-
下列说法正确的是( )
A.中和热一定是强酸跟强碱反应放出的热量
B.1 mol酸与1 mol 碱完全反应放出的热量是中和热
C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热
D.测定中和热时可用稀硫酸和稀Ba(OH)2溶液





