-
铁及其化合物在生产、生活中应用广泛。
(1)一定条件下,Fe与CO2可发生反应:
2Fe(s)+3CO2(g) Fe2O3(s)+3CO(g)
Fe2O3(s)+3CO(g)
该反应的平衡常数(K ) 随温度(T ) 升高而增大。
①该反应的平衡常数K=______。(填表达式)
②下列措施中,能使平衡时c(CO)/c(CO2) 增大的是________(填标号)。
A.升高温度 B.增大压强
C.充入一定量CO D.再加一些铁粉
(2)图1装置发生反应的离子方程式为________。

(3)图2装置中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。

① 电源的M端为________极,甲烧杯中铁电极的电极反应为________。
② 乙烧杯中电解反应的化学方程式为________。
③ 停止电解,取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g,甲烧杯中产生的气体标准状况下体积为________mL 。
-
铁及其化合物在生产、生活中应用广泛.
(1)一定条件下,Fe与CO2可发生反应:2Fe(s)+3CO2(g)⇌Fe2O3(s)+3CO(g)该反应的平衡常数(K)随温度(T)升高而增大.
①该反应的平衡常数K=______.(填表达式)②下列措施中,能使平衡时 增大的是______(填标号).
增大的是______(填标号).
A.升高温度 B.增大压强 C.充入一定量CO D.再加一些铁粉

(2)图1装置发生反应的离子方程式为______.
(3)图2装置中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红.
①电源的M端为______极,甲烧杯中铁电极的电极反应为______.
②乙烧杯中电解反应的化学方程式为______ 2Cu+O2↑+2H2SO4
-
氧化还原反应在生产、生活中应用广泛。下列反应不属于氧化还原反应的是
A.木炭燃烧:C+O2 CO2
CO2
B.煅烧石灰石:CaCO3 CaO+CO2↑
CaO+CO2↑
C.铁的冶炼:Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
D.电解水:2H2O 2H2↑+O2↑
2H2↑+O2↑
-
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g)
Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
温度/℃ 1000 1115 1300
平衡常数 4.0 3.7 3.5
(1)该反应的平衡常数表达式K= ;△H 0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是 .
A.提高反应温度
B.移出部分CO2
C.加入合适的催化剂
D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正 υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)= .
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是 ;生成0.5mol K2FeO4转移电子的物质的量是 mol.
-
金属铁用途广泛,高炉炼铁的总反应为:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g),请回答下列问题:
2Fe(s)+3CO2(g),请回答下列问题:
(1)一定温度下,在体积固定的密闭容器中发生上述反应,可以判断该反应已经达到平衡的是___________
A.密闭容器中总压强不变
B.密闭容器中混合气体的平均摩尔质量不变
C.密闭容器中混合气体的密度不变
D.c(CO)=c(CO2)
E.Fe2O3的质量不再变化
(2)一定温度下,上述反应的化学平衡常数为3.0,该温度下将4molCO、2molFe2O3、6molCO2、5molFe加入容积为2L的密闭容器中,此时反应将向________________反应方向进行(填“正”或“逆”或“处于平衡状态”);反应达平衡后,若升高温度,CO与CO2的体积比增大,则正反应为______________反应(填“吸热”或“放热”)。
(3)已知:3Fe2O3(s)+CO(g) 2Fe3O4(s)+CO2(g) △H=–47kJ/mol
2Fe3O4(s)+CO2(g) △H=–47kJ/mol
Fe3O4(s)+CO(g) 3FeO(s)+CO2(g) △H=+19kJ/mol
3FeO(s)+CO2(g) △H=+19kJ/mol
FeO(s)+CO(g) Fe(s)+CO2(g) △H=–11kJ/mol
Fe(s)+CO2(g) △H=–11kJ/mol
则Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)的 △H=________________。
2Fe(s)+3CO2(g)的 △H=________________。
-
(9分) 铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K=________
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁ll.2g。则10min内CO的平均反应速率为________。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
① ________② ________
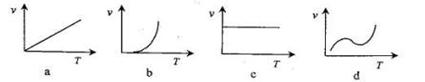
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列反应速率(V)和温度(T)的关系示意图中与铝热反应最接近的是________。
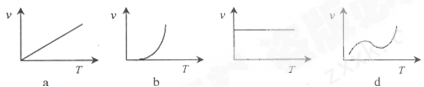
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:________
欲使上述体系中Al3+浓度增加,可加入的物质是________。
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质.
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)⇌2Fe(s)+3CO2(g)
①该反应的平衡常数表达式为:K=______
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g.则10min内CO的平均反应速率为______
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①______②______
(3)写出氢氧化铝在水中发生碱式电离的电离方程式:______
欲使上述体系中Al3+浓度增加,可加入的物质是______.
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生反应:Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
请回答下列问题:
①该反应的平衡常数表达式K=__________,ΔH____0(填“>”、“<”或“=”)。
②在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=________,CO的平衡转化率为________。
③欲提高②中CO的平衡转化率,可采取的措施是_____________________。
A.减少Fe的量 B.增加Fe2O3的量
C.移出部分CO2 D.提高反应温度
E.减小容器的容积 F.加入合适的催化剂
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。
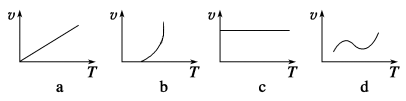
(3)写出氢氧化铝在水中发生碱式电离的电离方程式:
_________________________________________________________。
欲使上述体系中Al3+浓度增加,可加入的物质是______________________。
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
①该反应的化学平衡常数表达式为:K=________。
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。则10min内CO的平均反应速率为________。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到化学平衡状态:
①________②________。
(3)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应。下列化学反应速率(v)和温度(T)的关系示意图与铝热反应最接近的是________。
(4)写出氢氧化铝在水中发生酸式电离的电离方程式:________ ,
欲使上述体系中Al3+浓度增加,可加入的物质是________。
-
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g) ⇌2Fe(s)+3CO2(g)
(1)该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2 g。则10min内CO的平均反应速率为________。
(2)请用上述反应中某种气体的有关物质理量来说明该反应已达到平衡状态:
①____________________________________________________;
②____________________________________________________。
(3)写出氢氧化铝在水中发生碱式电离的电离方程式:________________;欲使上述体系中铝离子浓度增加,可加入的物质是______________________。