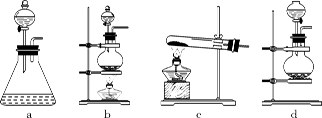-
氯气是一种重要的化工原料。
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是 。
(2)资料显示: 。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
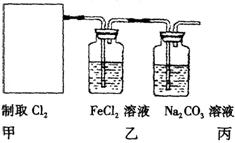
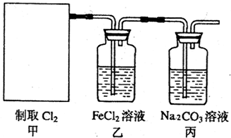
①在该实验中,甲部分的装置是 (填字母);指出a中m仪器的名称 。


②乙装置中FeCl2溶液Cl2反应的离子方程式是 。证明FeCl2与Cl2发生了氧化还原反应的实验方法是(填加试剂的名称、至少填二种)方法 、
;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、清毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是 ;
(3)为测定漂白粉中Ca(ClO)2的质量分数,该小组将2.0g漂白粉配制成250mL溶液,取出25mL并向其中依次加入过量稀H2SO4、过量KI溶液,完全反应后,再滴入 溶液:
溶液: ,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。
-
(12分)氯气是一种重要的工业原料。
(1)实验室可用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式是:__________________。
(2)资料显示:
某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
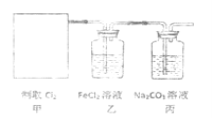
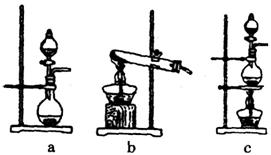
①在该实验中,甲部分的装置是______(填字母)。如何检查该装置的气密性?_________________。
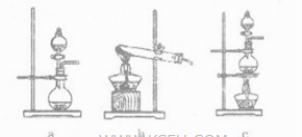
②乙装置中FeCl2溶液与Cl2反应的离子方程式是_______________。
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸。则丙中发生反应的化学方程式是____________。
④该实验存在明显的缺陷.改进的方法是_______________________________________________。
-
氯气是一种重要的工业原料。
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是________。
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O他们利用该反应设计如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O他们利用该反应设计如下制取氯气并验证其性质的实验。
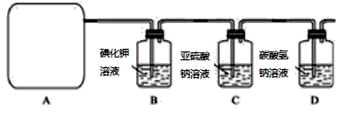
回答下列问题:(1)该实验中A部分的装置是_______(填标号)。
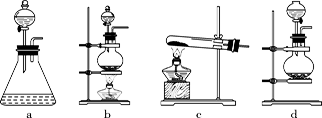
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):_____________________________。
(3)写出D装置中发生反应的离子方程式_________________
(4)该实验存在明显的缺陷,请你提出改进的方法__________________________________________写出反应离子方程式_____________________________________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol.L−1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2===Na2S4O6+2NaI,共用去Na2S2O3溶液20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为________。
-
(12分)氯气是一种重要的工业原料。
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是________。
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4  2CaSO4+2Cl2↑+2H2O
2CaSO4+2Cl2↑+2H2O
他们利用该反应设计如下制取氯气并验证其性质的实验。

(1)回答下列问题:(1)该实验中A部分的装置是________ (填标号) 。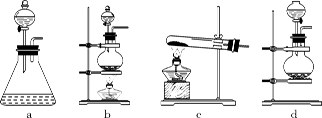
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):________。
(3)写出D装置中发生反应的离子方程式________(4)该实验存在明显的缺陷,请你提出改进的方法________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取出25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol·L?1的Na2S2O3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na2S2O3+I2 === Na2S4O6+2NaI,共用去Na2S2O3溶液20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为________。
-
氯气是一种重要的工业原料。
(1)实验室可用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式是:__________。
(2)资料显示:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
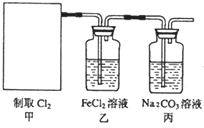
①在该实验中,甲部分的装置是__________(填字母)。
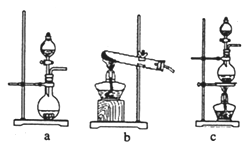
如何检查该装置的气密性?__________________________________________。
②乙装置中FeCl2溶液与Cl2:反应的离子方程式是_______________。
③丙装置中通人少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中发生反应的化学方程式是____________。
④该实验存在明显的缺陷,改进的方法________________________________。
-
氯气是一种重要的工业原料。
(1)写出实验室制取氯气反应的化学方程式________________________。
(2)资料显示:

 。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
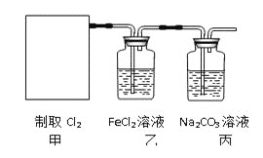
 在该实验中,甲部分的装置是_______
在该实验中,甲部分的装置是_______ 填字母
填字母 。
。
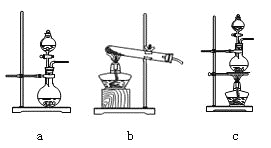
 乙装置中
乙装置中 溶液与
溶液与 反应的离子方程式是________________。
反应的离子方程式是________________。
 已知酸性:
已知酸性: ,丙装置中通入少量
,丙装置中通入少量 ,可制得具有漂白、消毒的物质,这种物质是_______
,可制得具有漂白、消毒的物质,这种物质是_______ 化学式
化学式 。
。
 有人认为该实验存在明显的缺陷,如何改进:______________,请你写出Cl2和“
有人认为该实验存在明显的缺陷,如何改进:______________,请你写出Cl2和“ ”中“最合适的化学试剂”反应的离子方程式_________________________。
”中“最合适的化学试剂”反应的离子方程式_________________________。
(3)家庭中常用消毒液 主要成分
主要成分 与洁厕灵
与洁厕灵 主要成分盐酸
主要成分盐酸 清洁卫生。某品牌消毒液包装上说明如下图。
清洁卫生。某品牌消毒液包装上说明如下图。

 “与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:__________。
“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:__________。
 漂粉精
漂粉精 主要成分
主要成分 与消毒液有相同的消毒功效,也需“密封保存”,请用化学方程式解释漂粉精因保存不当而变质失效的原因_________。
与消毒液有相同的消毒功效,也需“密封保存”,请用化学方程式解释漂粉精因保存不当而变质失效的原因_________。
-
氯气是一种重要的化工原料.
(1)实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是______.MnCl2+Cl2↑+2H2O
-
氯气是一种重要的工业原料.
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是______ MnCl2+Cl2↑+2H2O
-
氯气是一种重要的化工原料.某学习小组在实验室中利用如图所示装置制取氯气并探究其性质.
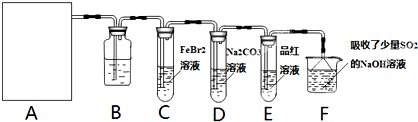
(1)若A是用二氧化锰和浓盐酸反应制取氯气的发生装置,除圆底烧瓶和导管外还用到的玻璃仪器有______;
(2)①装置B中盛有的试剂是______,作用是______.
②若E中品红溶液褪色,则C装置中发生反应的离子方程式是______.证明FeBr2与Cl2发生了氧化还原反应的实验方法是______(填操作方法).
③已知碳酸的酸性强于次氯酸,则装置D中反应的化学方程式为______.
(3)某研究性学习小组用刚吸收过少量SO2的NaOH溶液吸收处理上述实验后的尾气.吸收尾气一段时间后,吸收液(呈强碱性)中肯定存在Cl-、OH-、CO32-和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑盐类的水解;在碱性条件下ClO-也有强氧化性.).
①提出合理假设:
假设1:只存在SO32-;
假设2:只存在ClO-;
假设3:既存在SO32-,也存在ClO-;
假设4:既不存在SO32-,也不存在ClO-.
指导老师经分析认为,其中一个假设并不合理,它是______;判断的原因是______.
②设计实验方案,进行实验,请写出实验步骤以及预期现象和结论.限选实验试剂.
a.3mol/L H2SO4 b.0.01mol/L KMnO4 c.1mol/L BaCl2溶液
d.淀粉一KI溶液 e.酚酞试液 f.品红溶液
步骤一;取少量吸收液于试管中,滴加3mol/L H2SO4至溶液呈酸性,然后将所得溶液分装于A、B两试管中.
步骤二:向A试管中滴加1~2滴______ (填序号).若溶液______(填现象),则假设1成立.
步骤三:向B试管中滴加1~2滴______(填序号);若溶液______(填现象),则假设2成立.
③若假设2成立;写出步骤三中的离子方程式:______.
-
氯气是一种重要的工业原料。
(1)实验室可用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式是:
_______________________________________________________________________。
(2)资料显示:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质:

①在该实验中,甲部分的装置是__________(填字母)。
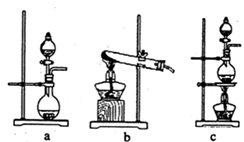
如何检查该装置的气密性?______________________________________________。
②乙装置中FeCl2溶液与Cl2:反应的离子方程式是_______________。
③丙装置中通人少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸.则丙中发生反应的化学方程式是____________。
④该实验存在明显的缺陷.改进的方法是________________________________________________。
。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。


溶液:
,共消耗20mLNa2S2O3溶液,则漂白粉中Ca(ClO)2的质量分数为 。