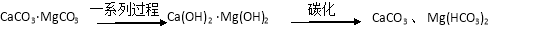-
碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,还含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
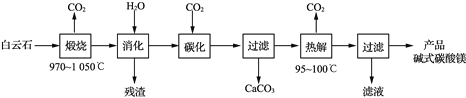
(1) “煅烧”时发生主要反应的化学方程式为____________________________。
(2)常温常压下“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
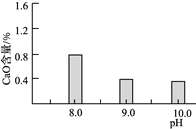
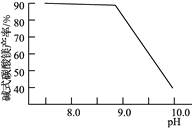
图1 CaO含量与碳化终点pH的关系 图2 碱式碳酸镁产率与碳化终点pH的关系
①应控制“碳化”终点pH约为________,发生的主要反应的化学方程式为______________________和____________________。
②图2中,当pH=10.0时,镁元素的主要存在形式是____________(写化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为________________________________。
(4)该工艺为达到清洁生产,可以循环利用的物质是____________(写化学式)。
-
碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,还含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
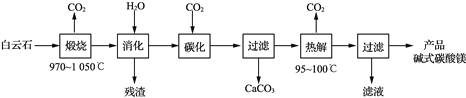
(1) “煅烧”时发生主要反应的化学方程式为____________________________。
(2)常温常压下“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
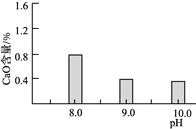
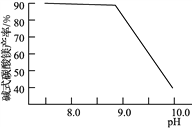
图1 CaO含量与碳化终点pH的关系 图2 碱式碳酸镁产率与碳化终点pH的关系
①应控制“碳化”终点pH约为________,发生的主要反应的化学方程式为______________________和____________________。
②图2中,当pH=10.0时,镁元素的主要存在形式是____________(写化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为________________________________。
(4)该工艺为达到清洁生产,可以循环利用的物质是____________(写化学式)。
-
碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]是一种重要的无机化工产品。一种由白云石[主要成分为CaMg(CO3)2,含少量SiO2、Fe2O3等]为原料制备碱式碳酸镁(国家标准中CaO的质量分数≤0.43%)的实验流程如下:
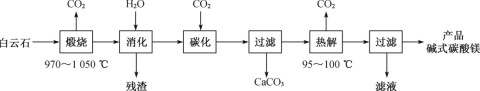
(1)“煅烧”时发生主要反应的化学方程式为___。
(2)常温常压下,“碳化”可使镁元素转化为Mg(HCO3)2,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
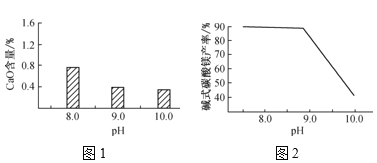
①应控制“碳化”终点pH约为___,钙元素的主要存在形式是___(填化学式)。
②根据图2,当pH=10.0时,镁元素的主要存在形式是___(填化学式)。
(3)“热解”生成碱式碳酸镁的化学方程式为___。
(4)该工艺为达到清洁生产,可以循环利用的物质是___(填化学式)。
-
水合碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O],又称轻质碳酸镁。常利用菱镁矿(质量含量为碳酸镁90%,碳酸钙10%)碳化法制取:
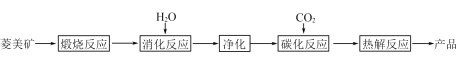
(1)根据下列表格数据,选择消化反应的最佳温度__________;理由是___________________________。
| 消化温度/℃ | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 转化率/% | 50.3 | 58.2 | 85.1 | 85.2 | 90.7 | 91.2 | 91.5 |
(2)碳化反应可生成Mg(HCO3)2,生成Mg(HCO3)2的化学方程式为____________。
(3)流程图中__________和__________可以为碳化反应提供二氧化碳源。
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5mol·L-1时,可以认为完全除去。常温时当调节溶液PH 为9.5时,此时Mn2+小于__________mol·L-1,不会沉淀出来。
| 物质 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| Ksp | 10-11 | 10-39 | 10-17 | 10-14 |
②如果把Fe2+转化为Fe3+,从环境角度选择最合适的氧化剂为__________。
A.Ca(ClO)2 B.Cl2 C.H2O2 D.HNO3
③下列方案中,较好的为__________,理由是______________________。

-
白钠镁矾(mNa2SO4·nMgSO4·xH2O)俗称硝板,工业上用白钠镁矾制备碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]晶须的过程如下:向碳酸钠溶液中加入白钠镁矾,保持50℃加热0.5h,有大量的5MgCO3·3H2O生成,然后升高温度到85℃加热2h发生热解反应,过滤得碱式碳酸镁晶体。
(1)热解反应的方程式为________________。
(2)碱式碳酸镁可用作化学冷却剂,原因是________________。
(3)为测定白钠镁矾的组成,进行下列实验:
①取白钠镁矾3.340 g溶于水配成100.00 mL溶液A;
②取25.00 mL溶液A,加入足量的氯化钡溶液,得BaSO4 1.165 g;
③另取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA标准溶液滴定Mg2+(离子方程式为Mg2+ + H2Y2-=MgY2-+ 2H+),滴定至终点,消耗标准溶液25.00 mL。通过计算确定白钠镁矾的化学式(写出计算过程)。___________________
-
白钠镁矾(mNa2SO4·nMgSO4·xH2O)俗称硝板,工业上用白钠镁矾制备碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]晶须的过程如下:向碳酸钠溶液中加入白钠镁矾,保持50℃加热0.5h,有大量的5MgCO3·3H2O生成,然后升高温度到85℃加热2h发生热解反应,过滤得碱式碳酸镁晶体。
(1)热解反应的方程式为________________。
(2)碱式碳酸镁可用作化学冷却剂,原因是________________。
(3)为测定白钠镁矾的组成,进行下列实验:
①取白钠镁矾3.340 g溶于水配成100.00 mL溶液A;
②取25.00 mL溶液A,加入足量的氯化钡溶液,得BaSO4 1.165 g;
③另取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA标准溶液滴定Mg2+(离子方程式为Mg2+ + H2Y2-=MgY2-+ 2H+),滴定至终点,消耗标准溶液25.00 mL。通过计算确定白钠镁矾的化学式(写出计算过程)。___________________
-
碱式碳酸镁 是重要的无机化工产品。一种由白云石
是重要的无机化工产品。一种由白云石 主要成分为
主要成分为 ,还含少量
,还含少量 、
、 等
等 为原料制备碱式碳酸镁
为原料制备碱式碳酸镁 国家标准中CaO 的质量分数
国家标准中CaO 的质量分数
 的实验流程如下:
的实验流程如下:
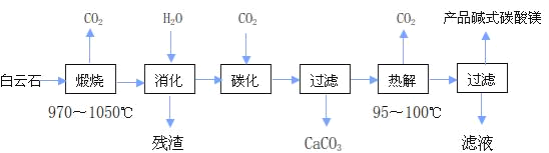
 “煅烧”时发生主要反应的化学方程式为________________。
“煅烧”时发生主要反应的化学方程式为________________。
 常温常压下“碳化”可使镁元素转化为
常温常压下“碳化”可使镁元素转化为 ,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
图1 CaO含量与碳化终点pH的关系
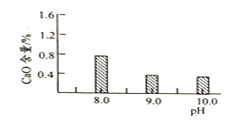
图2碱式碳酸镁产率与碳化终点pH的关系
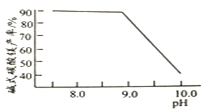
 应控制“碳化”终点PH 约为__________。
应控制“碳化”终点PH 约为__________。
 图
图 中,当
中,当
 时,镁元素的主要存在形式是__________________
时,镁元素的主要存在形式是__________________ 写化学式
写化学式 。
。
 “过滤”时须用到的玻璃仪器有:烧杯、玻璃棒、__________________。
“过滤”时须用到的玻璃仪器有:烧杯、玻璃棒、__________________。
 一种测定碱式碳酸镁
一种测定碱式碳酸镁 组成的方法如下:
组成的方法如下:
 称取一定量的碱式碳酸镁晶体溶于足量的盐酸,收集到气体
称取一定量的碱式碳酸镁晶体溶于足量的盐酸,收集到气体 标准状况
标准状况 ;往所得溶液中加入足量的NaOH溶液,过滤,将所得沉淀洗涤、干燥,称量得固体
;往所得溶液中加入足量的NaOH溶液,过滤,将所得沉淀洗涤、干燥,称量得固体 。
。
 另取一定量的碱式碳酸镁晶体在空气中加热,固体残留率
另取一定量的碱式碳酸镁晶体在空气中加热,固体残留率 固体样品的剩余质量
固体样品的剩余质量 固体样品的起始质量
固体样品的起始质量 随温度的变化如下图所示
随温度的变化如下图所示 样品在
样品在 时完全失去结晶水
时完全失去结晶水 。
。
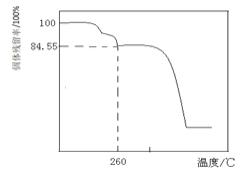
根据以上实验数据计算确定碱式碳酸镁晶体的化学式 写出计算过程
写出计算过程 _________。
_________。
-
“变废为宝”是化工的重要主题。工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有CuCl2,FeCl2等)制备碱式碳酸铜Cu2(OH)2CO3],其制备过程如下图所示:
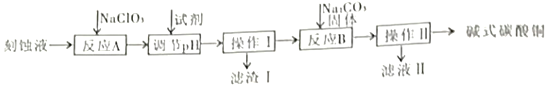
查阅资料得知,一定浓度的Cu2+、Fe2+、Fe3+生成氢氧化物沉淀的pH如下表:
| 金属离子 | Cu2+ | Fe2+ | Fe3+ |
| 开始沉淀的pH | 4.2 | 6.5 | 1.4 |
| 沉淀完全的pH | 6.7 | 9.7 | 3.7 |
(1)电子工业中用FeCl3溶液制作铜制印刷电路板,该反应的离子方程式为___________。
(2)操作I、操作Ⅱ所用的玻璃仪器除烧杯外还需要______________________。
(3)氯酸钠的作用是____________________________________________;反应A中氧化剂与还原剂物质的量之比是___________。
(4)调节pH的范围为___________,可以选择的试剂是___________(填序号)。
A.氨水 B.硫酸铜 C.氧化铜 D.氢氧化铜
(5)已知滤液Ⅱ中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式:___________。
(6)若废液中CuCl2的含量为13.5%,则1吨废液理论上可提炼碱式碳酸铜________吨。
-
白云石的主要成分是CaCO3·MgCO3,在我国有大量的分布。以白云石为原料生产的钙镁系列产品有广泛的用途。
(1)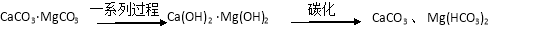
已知碳化反应是放热反应,化学方程式是Ca(OH)2 + Mg(OH)2 + 3CO2 CaCO3 + Mg(HCO3)2 + H2O,已知某次碳化时溶液中钙离子浓度随时间的变化如图所示。
CaCO3 + Mg(HCO3)2 + H2O,已知某次碳化时溶液中钙离子浓度随时间的变化如图所示。

①15 min之后钙离子浓度增大,原因是_______________(用化学方程式表示)。
②碳化温度保持在50℃-60℃。温度偏高不利于碳化反应,原因是 、 。温度偏低也不利于碳化反应,原因是 。
(2)用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如图:
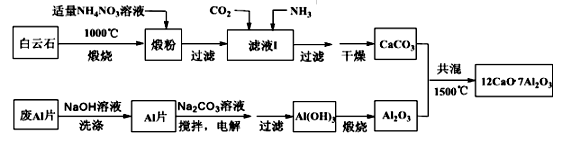
① 由流程知,锻粉中的氧化镁几乎不溶解,滤液1中的离子反应是 。
② 该工艺中不能用(NH4)2SO4代替NH4NO3,原因是 。
③ 用NaOH溶液可除去Al片表面的氧化膜,反应的离子方程式为 。
④ 电解制备Al(OH)3时,电极分别为Al片和石墨,阳极反应为 。
-
以橄榄石(主要成分是Mg9FeSi5O20)等为原料生产硅胶、碱式碳酸镁[Mg2(OH)2CO3]的部分工艺流程如下图所示:
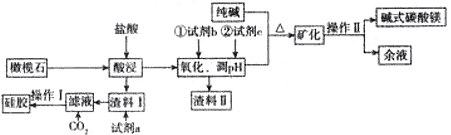
(1)Mg9FeSi5O20中铁元素的化合价为 ,为提高镁的浸出率,可采用的两种主要措施是 渣料II的成分是 。
(2)若试剂b是氯碱工业中的某种气体产物,写出加入b后反应的离子方程式 。试剂c的用途是调节溶液的pH,比较恰当的物质是 (写化学式,后同),余液中溶质的主要成分是 。
(3)操作I的名称是 ,写出生成碱式碳酸镁(同时有气体生成)的离子方程式 。