-
实验室制备氯化氢的反应化学方程式为:H2SO4(浓)+NaCl=HCl↑+NaHSO4,回答以下问题:
(1)该反应能发生的原因是________________。
A.硫酸酸性强于盐酸 B.盐酸易挥发 C.硫酸氧化性强于盐酸
(2)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,反应的离子方程式为_____________________。
(3)实验室需要配制0.50 mol·L-1 NaCl溶液240 mL。
①所需的仪器有:托盘天平、药匙、烧杯、________、______、______以及等质量的两片滤纸。
②配制该溶液需取NaCl晶体______ g。
③配制一定物质的量浓度溶液定容时的操作是____________________________________
(4)在标准状况下,将44.8 L HCl气体溶于127 mL水中,所得盐酸的密度为1.18 g·cm-3。该盐酸的物质的量浓度是______________________。
高二化学实验题中等难度题查看答案及解析
-
(13分)用1-丁醇、溴化钠和较浓H2SO4混合物为原料,在实验室制备1-溴丁烷,并检验反应的部分副产物。(已知:NaCl+H2SO4(浓)=NaHSO4+HCl↑)现设计如下装置,其中夹持仪器、加热仪器及冷却水管没有画出。请回答下列问题:
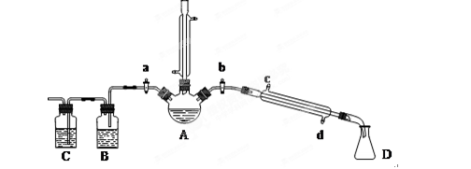
(1)仪器A的名称是 。
(2)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷。写出该反应的化学方程式 。
(3)理论上,上述反应的生成物还可能有:丁醚、1-丁烯、溴化氢等。熄灭A处酒精灯,在竖直冷凝管上方塞上塞子,打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物。B、C中应盛放的试剂分别是 、 。
(4)在实验过程中,发现A中液体由无色逐渐变成黑色,该黑色物质与浓硫酸反应的化学方程式为 ,可在竖直冷凝管的上端连接一个内装吸收剂碱石灰的干燥管,以免污染空气。
(5)相关有机物的数据如下:
物质
熔点/0C
沸点/0C
1-丁醇
-89.5
117.3
1-溴丁烷
-112.4
101.6
丁醚
-95.3
142.4
1-丁烯
-185.3
-6.5
为了进一步精制1-溴丁烷,继续进行了如下实验:待烧瓶冷却后,拔去竖直的冷凝管,塞上带温度计的橡皮塞,关闭a,打开b,接通冷凝管的冷凝水,使冷水从 (填c或d)处流入,迅速升高温度至 ℃,收集所得馏分。
(6)若实验中所取1-丁醇、NaBr分别为7.4 g、13.0 g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6 g 1-溴丁烷,则1-溴丁烷的产率是 。
高二化学实验题困难题查看答案及解析
-
实验室制备溴乙烷(C2H5Br)的方法为:
NaBr + H2SO4 = NaHSO4 + HBr
C2H5OH + HBr
C2H5Br + H2O
其中可能会发生副反应:
2HBr + H2SO4(浓) = Br2 ↑+ SO2↑ + 2H2O
制取的装置和步骤如图(已知溴乙烷的沸点38.4℃,不溶于水):
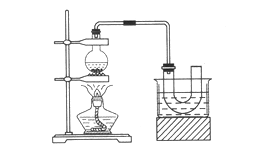
①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;
②在圆底烧瓶中加入10 mL 95%乙醇、28 mL 78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;
③小心加热.使其充分反应.
请根据信息回答下列问题:
(1)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为___________,同时生成的无色气体分子式为________________。
(2)为了更好的控制温度,除用图示的小火加热外,更好的加热方式为________。
(3)反应结束后,U形管内粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可以选择下列试剂中的________________________(填序号)。
A.NaOH溶液 B.H2O C.Na2SO3溶液 D.CCl4
要进一步制得纯净的C2H5Br,可用水洗,然后加入无水CaCl2,再进行__________(填操作名称)。
(4)下列几项实验步骤,为了检验溴乙烷中溴元素,取出少量溴乙烷产品,而后正确的操作顺序是:___________________(填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH水溶液;⑤冷却
A. ④①⑤③② B. ④③①⑤② C. ④③②①⑤ D. ④②①③⑤
高二化学实验题中等难度题查看答案及解析
-
回答有关问题:
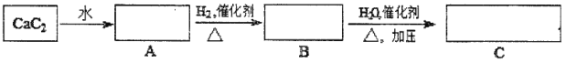
(1)A→B的反应类型是___________,实验室制取B的反应条件是________________。
(2)A和氯化氢为原料可以制得塑料聚氯乙烯。写出制备过程中最后一步发生的方程式:__________。
高二化学推断题中等难度题查看答案及解析
-
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):
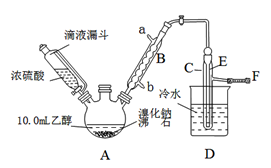
H2SO4(浓)+NaBrNaHSO4+HBr↑
CH3CH2OH+HBr
CH3CH2Br+H2O。有关数据见下表:
乙醇
溴乙烷
溴
状态
无色液体
无色液体
深红色液体
密度/(g·cm-3)
0.79
1.44
3.1
沸点/℃
78.5
38.4
59
(1)A装置的名称是______________。
(2)实验中用滴液漏斗代替分液漏斗的优点为_______________________。
(3)给A加热温度过高或浓硫酸的浓度过大,均会使C中收集到的粗产品呈橙色,原因是A中发生了副反应,写出此反应的化学方程式________________________。
(4)给A加热的目的是________________________,F接橡皮管导入稀NaOH溶液,其目的主要是___________________。
(5)图中C中的导管E的末端须在水面以下,其目的是______________________。
(6)粗产品洗涤、分液后,再经过蒸馏水洗涤、分液,然后加入少量的无水硫酸镁固体,静置片刻后过滤,再将所得滤液进行蒸馏,收集到的馏分约10.0 g。从乙醇的角度考虑,本实验所得溴乙烷的产率是________________。
高二化学实验题困难题查看答案及解析
-
以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是_____(填字母)。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl
CH3CH2Cl+H2O
C.CH3CH3+Cl2
CH3CH2Cl+HCl
D.CH2=CHCl+H2
CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______(填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:______,该方法的优点是_______。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:
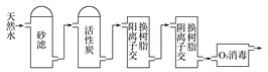
活性炭的作用是_______;O3消毒的优点是_______。
高二化学推断题中等难度题查看答案及解析
-
以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是_____(填字母)。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl
CH3CH2Cl+H2O
C.CH3CH3+Cl2
CH3CH2Cl+HCl
D.CH2=CHCl+H2
CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______(填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:______,该方法的优点是_______。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:
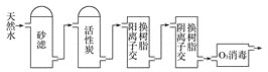
活性炭的作用是_______;O3消毒的优点是_______。
高二化学推断题中等难度题查看答案及解析
-
下列方程式书写正确的是
A.NaHSO4在熔融状态下的电离方程式:NaHSO4=Na++HSO4-
B.H2SO4溶液与NaOH溶液发生中和反应的热化学方程式为(已知H2SO4 溶液与NaOH溶液发生反应的中和热为57.3 kJ/mol):H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq) △H=-57.3kJ/mol
C.CO32-的水解方程式:CO32-+2H2O
H2CO3+2OH-
D.CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
高二化学单选题中等难度题查看答案及解析
-
某一化工厂为了综合利用生产过程中的副产品CaSO4,和相邻的合成氨厂联合设计了以下制备(NH4)2SO4的工艺流程:
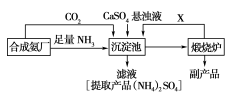
请回答以下问题:
(1)合成氨反应的化学方程式是_____。沉淀池中发生的主要反应方程式是____________。该反应能够发生的原因是______________________。
(2)在上述流程的沉淀池中通入足量氨气的目的是_______________________________________,可以循环使用的X是________。
(3)该生产过程中的副产品是__,从绿色化学和资源综合利用的角度说明上述流程的主要优点是_____;从物质的性质和工业生产实际的角度考虑该流程的主要缺陷是________________________________。
高二化学填空题困难题查看答案及解析
-
在下列各说法中,正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.热化学方程式中的化学计量数表示物质的量,可以是分数
C.中和热可以选用稀H2SO4与稀Ba(OH)2溶液进行实验测定
D.HCl和NaOH反应的中和热ΔH =-57.3kJ/mol,则NaOH和CH3COOH反应的中和热ΔH<-57.3kJ/mol
高二化学选择题中等难度题查看答案及解析