-
某无色溶液可能含有K+、Na+、NH4+ 、Ba2+、Fe3+、Fe2+、Cl-、Br-、SO32-、SO42-中若干种(忽略水电离出的H+、OH-),且离子浓度相同,依次进行下列实验,且每步所加试剂均过量,观察到现象如下:
①用pH试纸检验,溶液的pH大于7
②向溶液中滴加氯水,再加入CCl4振荡,静置,CCl4层呈橙色
③向所得水溶液中加入Ba(NO3)2溶液和稀HNO3,有白色沉淀产生过滤,向滤液中加入AgNO3溶液和稀HNO3,有白色沉淀产生
根据上述实验,以下说法正确的是
A. 无法推断原混合溶液中是否含有NH4+和SO42-
B. 原混合溶液中Br-、SO32-肯定存在,Cl-可能存在
C. 确定溶液中是否存在Na+,需要做焰色反应
D. 原混合溶液中阳离子Ba2+、Fe3+、Fe2+一定不存在,K+、Na+、NH4+一定存在
高三化学单选题困难题查看答案及解析
-
某无色溶液可能含有K+、Na+、NH4+ 、Ba2+、Fe3+、Fe2+、Cl-、Br-、SO
、SO
中若干种(忽略水电离出的H+、OH-),且离子浓度相同,依次进行下列实验,且每步所加试剂均过量,观察到现象如下:
①用pH试纸检验,溶液的pH大于7。
②向溶液中滴加氯水,再加入CCl4振荡,静置,CCl4层呈橙色。
③向所得水溶液中加入Ba(NO3)2溶液和稀HNO3,有白色沉淀产生过滤,向滤液中加入AgNO3溶液和稀HNO3,有白色沉淀产生。
根据上述实验,以下说法正确的是
A. 无法推断原混合溶液中是否含有NH4+和SO
B. 原混合溶液中Br-、SO
肯定存在,Cl-可能存在
C. 确定溶液中是否存在Na+,需要做焰色反应
D. 原混合溶液中阳离子Ba2+、Fe3+、Fe2+一定不存在,K+、Na+、NH4+一定存在
高三化学选择题困难题查看答案及解析
-
某无色溶液,只可能含有以下离子中的若干种(忽略水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+、NO3一、CO32一、SO42-,现取三份100 mL溶液进行如下实验:
① 第一份加足量AgNO3溶液后,有白色沉淀产生;
② 第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为4.66 g;
③ 第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如下图。
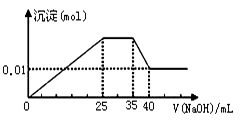
根据上述实验,以下推测不正确的是( )
A.依据电荷守恒,原溶液中NO3-的物质的量应为0.03 mol
B.原溶液一定不存在H+、Fe3+、CO32-
C.原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+)∶n(Al3+)∶n( NH4+) = 1∶1∶2
D.实验所加的NaOH的浓度为2 mol·L-1
高三化学选择题困难题查看答案及解析
-
有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量的BaCl2溶液后,有白色沉淀
产生,经洗涤、干燥后,称量沉淀质量为6.99g;
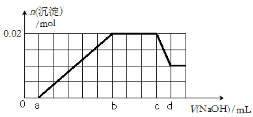
②第二份逐滴滴加NaOH溶液,测得沉淀的物质的
量与NaOH溶液的体积关系如右图所示。根据上述
实验事实,回答以下问题:
(1)该溶液中一定不存在的阳离子有 ;
(2)在实验②中,NaOH溶液滴至b ~c段过程中发生的离子反应方程式为 ;NaOH溶液的浓度为 (用字母c、d表示);
(3)原溶液确定含有Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为 ;
(4)原溶液中NO3-的浓度为c(NO3-),则c(NO3-)的取值范围为 。
高三化学填空题中等难度题查看答案及解析
-
离子推断题:有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量的BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,称量沉淀质量为6.99g;
②第二份逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如下图所示。
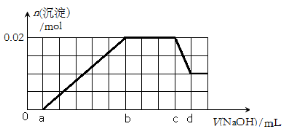
根据上述实验事实,回答以下问题:
⑴该溶液中一定不存在的阳离子有 ;
⑵在实验②中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为 ;NaOH溶液的浓度为 (用含字母c、d的代数式表示);
⑶确定原溶液一定含有Mg2+、Al3+、H+,其物质的量之比n(Mg2+): n(Al3+):n(H+)为 (填数字,下同);
⑷原溶液中NO3-的浓度为c(NO3-),则c(NO3-)的取值范围为 。
高三化学填空题困难题查看答案及解析
-
pH=1的某溶液X中还含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种(忽略水的电离及离子的水解), 取该溶液进行如下实验:
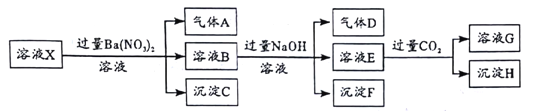
下列有关推断不正确的是
A. 沉淀H为Al(OH)3、BaCO3的混合物
B. 根据上述连续实验不能确定溶液X中是否含有Fe2+、Cl-
C. 溶液X中一定含有NH4+、Al3+、Fe2+、SO42-、H+
D. 若溶液X 为100mL ,产生的气体A为44.5mL(标况),则X中c(Fe2+)=0.06mol·L-1
高三化学单选题困难题查看答案及解析
-
pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图:下列有关推断不正确的是( )
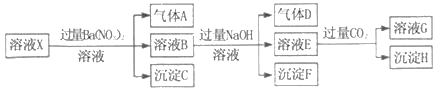
A. 溶液X中一定含有H+、Al3+、NH4+、Fe2+、SO42﹣
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl﹣
C. 沉淀H为Al(OH)3、BaCO3的混合物
D. 若溶液X为100mL,产生的气体A为44.8mL(标准状况),则X中c(Fe2+)=0.06mol•L﹣1
高三化学单选题困难题查看答案及解析
-
pH=1的某溶液X中还含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32–、SO32–、SO42–、Cl–、NO3–中的一种或几种(忽略水的电离及离子的水解),取该溶液进行如下实验:

下列有关推断不正确的是( )
A. 沉淀H为Al(OH)3、BaCO3的混合物
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl–
C. 溶液X中一定含有Al3+、NH4+、Fe2+、SO42–、H+
D. 若溶液X为100 mL,产生的气体A为44.8 mL(标况),则X中c(Fe2+)=0.06 mol·L–1
高三化学选择题困难题查看答案及解析
-
pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图:下列有关推断不正确的是( )
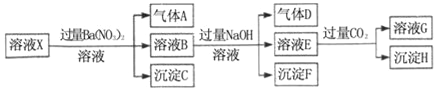
A. 溶液X中一定含有H+、Al3+、NH4+、Fe2+、SO42﹣
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl﹣
C. 沉淀H为Al(OH)3、BaCO3的混合物
D. 若溶液X为100mL,产生的气体A为44.8mL(标准状况),则X中c(Fe2+)=0.06mol•L﹣1
高三化学单选题困难题查看答案及解析
-
pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图:下列有关推断不正确的是( )

A. 溶液X中一定含有H+、Al3+、NH4+、Fe2+、SO42﹣
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl﹣
C. 沉淀H为Al(OH)3、BaCO3的混合物
D. 若溶液X为100mL,产生的气体A为44.8mL(标准状况),则X中c(Fe2+)=0.06mol•L﹣1
高三化学单选题困难题查看答案及解析