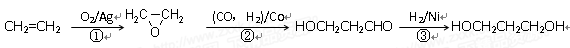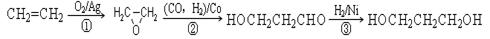-
CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。
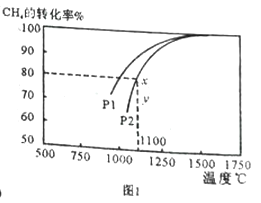
①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
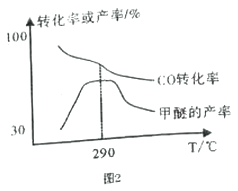
①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
-
CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。
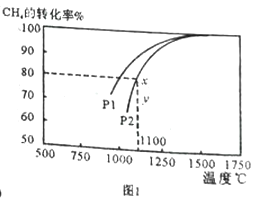
①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
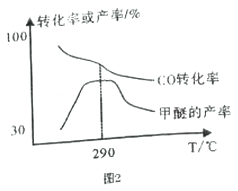
①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
-
CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。
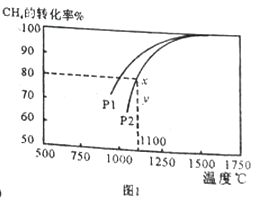
①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
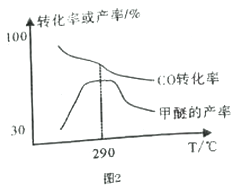
①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
-
合成气(CO+H2)广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气。
(1)已知标况下,5.6LCH4与水蒸气完全反应时吸收51.5KJ的热量,请写出该反应的热化学方程式____;
(2)在150℃时2L的密闭容器中,将2 mol CH4和2 mol H2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的变化量来表示该反应速率v(H2)=____。
②在该温度下,计算该反应的平衡常数K=____。
③下列选项中能表示该反应已达到平衡状态的是____
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.C (CH4) = C (CO)
(3)合成气中的氢气也用于合成氨气:N2 + 3H2 2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是____;
2NH3。保持温度和体积不变, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是____;
| 容 器 | 体积 | 起始物质 | 平衡时NH3的物质的量 | 平衡时N2的 体积分数 | 反应开始时的速率 | 平衡时容器内压强 |
| 甲 | 1L | 1molN2+3molH2 | 1.6mol | φ甲 | ν甲 | P甲 |
| 乙 | 1L | 2molN2+6molH2 | n1 mol | φ乙 | ν乙 | P乙 |
| 丙 | 2L | 2molN2+6molH2 | n2 mol | φ丙 | ν丙 | P丙 |
A.n1=n2=3.2 B.φ甲=φ丙>φ乙 C.ν乙>ν丙>ν甲 D.P乙>P甲=P丙
(4)合成气制甲醚的反应方程式为2CO(g) + 4H2(g) CH3OCH3(g)+ H2O(g) △H = b kJ/mol。有研究者在催化剂(Cu—Zn—Al—O和A12O3)、 压强为5.OMPa的条件下,由H2和CO直接制备甲醚,结果如下图所示。
CH3OCH3(g)+ H2O(g) △H = b kJ/mol。有研究者在催化剂(Cu—Zn—Al—O和A12O3)、 压强为5.OMPa的条件下,由H2和CO直接制备甲醚,结果如下图所示。
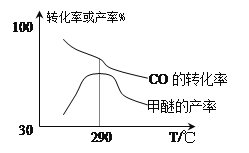
① 290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是____;
② b____0,(填“>”或“<”或“=”)理由是____。
-
合成气(CO+H2) 广泛用于合成有机物,工业上常采用天然气与水蒸气反应等方法来制取合成气,
(1)已知标况下,5.6LCH4与水蒸气完全反应时吸收51.5kJ的热量,请写出该反应的热化学方程式________________;
(2)在150℃时2L 的密闭容器中,将2molCH4和2mol H2O(g)混合,经过15min达到平衡,此时CH4的转化率为60%。回答下列问题:
①从反应开始至平衡,用氢气的变化量来表示该反应速率v(H2)=________。
②在该温度下,计算该反应的平衡常数K=________。
③下列选项中能表示该反应已达到平衡状态的是________。
A.V(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.C(CH4)=C(CO)
(3)合成气中的氢气也用于合成氨气:N2+3H2 2NH3。保持温度和体积不变,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是_______________;
2NH3。保持温度和体积不变,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是_______________;
| 容器 | 体积 | 起始物质 | 平衡时NH3的物质的量 | 平衡时N2 的体积分数 | 反应开始时的速率 | 平衡时容器内压强 |
| 甲 | 1L | 1molN2+3molH2 | 1.6mol | φ甲 | v甲 | P甲 |
| 乙 | 1L | 2molN2+6molH2 | n1 mol | φ乙 | v乙 | P乙 |
| 丙 | 2L | 2molN2+6molH2 | n2 mol | φ丙 | v丙 | P丙 |
A.n1=n2=3.2 B.φ甲=φ丙>φ乙 C.v乙 >v丙>v甲 D.P乙>P甲=P丙
(4)合成气可以制取甲醚,绿色电源“二甲醚-氧气燃料电池”工作原理如下图所示
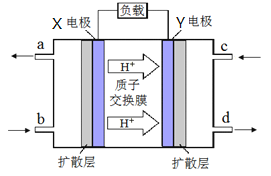
① 电极Y 上发生的反应式为__________ ;
②电池在放电过程中,电极X周围溶液的pH_______(填“增大、减小、不变”)。
-
以氢气、一氧化碳为主要成分,供化学合成的一种原料气体叫合成气。工业上通过“天然气蒸气转化”反应来得到合成气,其反应为:CH4+H2O(g) CO+3H2;△H>0。工业上通过采用合适的温度和压强、适宜的催化剂以及合适的CH4与H2O配比来获得最佳的生产效率。对于该转化反应的有关叙述正确的是( )
CO+3H2;△H>0。工业上通过采用合适的温度和压强、适宜的催化剂以及合适的CH4与H2O配比来获得最佳的生产效率。对于该转化反应的有关叙述正确的是( )
A.增大压强,有利于得到更多的合成气
B.反应温度越低,越有利于合成气的生产
C.工业生产中采用加入过量水蒸气来提高甲烷的利用率
D.工业生产中使用催化剂的目的在于提高甲烷的利用率
-
(14分)氨的合成是最重要的化工生产之一。
Ⅰ.工业上合成氨用的H2有多种制取的方法:
① 用焦炭跟水反应:C(s)+H2O(g)  CO(g) + H2(g);
CO(g) + H2(g);
② 用天然气跟水蒸气反应:CH4(g)+H2O(g)  CO(g)+3H2(g)
CO(g)+3H2(g)
已知有关反应的能量变化如下图,且方法②的反应为吸热反应,则方法②中反应的ΔH =___________ kJ/moL。
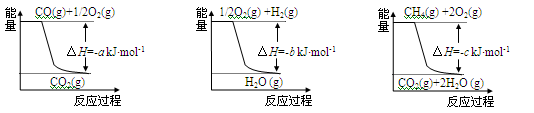
Ⅱ.在3个1L的密闭容器中,同温度下、使用相同催化剂分别进行反应:
3H2(g)+N2(g)  2NH3(g)
2NH3(g)
按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 | 2 mol NH3 |
| 达到平衡的时间(min) | t | 5 | 8 |
| 平衡时N2的浓度(mol·L-1) | c1 | 3 | c2 |
(1)下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)甲容器中达到平衡所需要的时间t 5min,表中c1 c2。(填“>”、“<” 或“=”)
(3)用氨合成尿素的反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)。工业生产时,原料气带有水蒸气。图1表示CO2的转化率与氨碳比
CO(NH2)2(s)+H2O(g)。工业生产时,原料气带有水蒸气。图1表示CO2的转化率与氨碳比 、水碳比
、水碳比 的变化关系。
的变化关系。
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是 。
②测得B点氨的转化率为30%,则x1= 。
Ⅲ.有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图2所示。
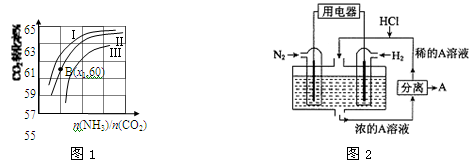
电池正极的电极反应式是 ,A是 。
-
(12分)利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O=CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式________。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 mol H2,,此时N2的转化率为a。则平衡时NH3的浓度为________。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
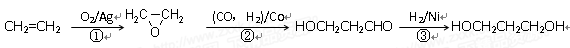
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭________吨、甲烷________吨,
才能满足生产需要。
-
 利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径。回答下列问题:
(1)甲烷在高温下与水蒸气反应的化学方程式为:CH4+H2O CO+3H2。部分物质的燃烧热数据如下表:
| 物 质 | 燃烧热(kJ·mol-1) |
| H2(g) | -285.8 |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
已知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量。写出CH4和水蒸气在高温下反应的热化学方程式。
(2)500℃、50MPa时,在容积为V L的容器中加入1 mol N2、3 molNH3,反应达平衡后测得平衡常数为K,此时CH4的转化率为a。则K和a的关系是K=。
(3)1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
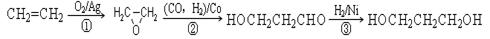
某化工厂已购得乙烯11.2 t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:C+H2O CO+H2 CH4+H2O
CO+H2 CH4+H2O CO+3H2
CO+3H2
假设在生产过程中,反应①、②、③中各有机物的转化率均为100%。且反应②中CO和H2、反应③中H2的转化率都为80%,计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
-
氨的合成是最重要的化工生产之一。
I.工业上合成氨用的H2有多种制取的方法:
① 用焦炭跟水反应: C(s)+ H2O(g)  CO(g)+ H2(g);
CO(g)+ H2(g);
② 用天然气跟水蒸气反应:CH4(g)+ H2O(g) CO (g)+ 3H2(g)
CO (g)+ 3H2(g)
已知有关反应的能量变化如下图,则方法②中反应的ΔH =__________ ___。
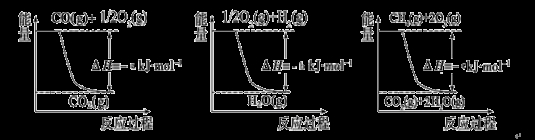
Ⅱ.在3个1L的密闭容器中,同温度下、使用相同催化剂分别进行反应:
3H2(g)+ N2(g) 2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3 mol H2、2 mol N2 | 6 mol H2、4mol N2 | 2 mol NH3 |
| 达到平衡的时间(min) | t | 5 | 8 |
| 平衡时N2的浓度(mol·L-1) | c1 | 3 | |
| N2的体积分数 | ω1 | ω2 | ω3 |
| 混合气体密度(g·L-1) | ρ1 | ρ2 | |
(1)下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.v(N2)正=3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(2)甲容器中达到平衡所需要的时间t 5min (填>、< 或=)
(3)乙中从反应开始到平衡时N2的平均反应速率 (注明单位)。
(4)分析上表数据,下列关系正确的是________.
a.2c1 =3mol/L b.ω1 = ω2 c.2ρ1 = ρ2
(5)该温度下,容器乙中,该反应的平衡常数K=____ __(用分数表示)(mol/L)-2。

CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。