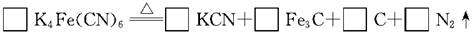-
食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6] •3H2O。
42.2gK4[Fe(CN)6] •3H2O(M=422g/mol)样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。
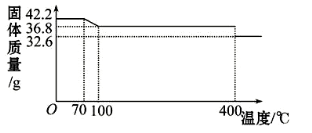
(1)试确定150℃时固体物质的化学式为_______________。
(2)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a_________0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=______________。
(3)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化。已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为 。
(4)不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。为了验证这一事实,某同学拟用下图装置进行实验(实验时压强为10lkPa,温度为0℃)。
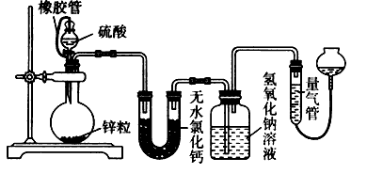
(I)若在烧瓶中投入d g锌,加入一定量的c mol/L浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中n(H2)=_____________(用含字母的代数式表示)。若撤走盛有无水氯化钙的U型管,n(SO2)/n(H2)的数值将 (填偏大、偏小或无影响)。
(II)在硫酸中加入硫酸铜可以加快氢气的生成速率的原因:_____________________。
(III)为进一步探究硫酸铜的量对氢气生成速率的影响,某同学设计如下一系列实验,将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中。
| 实验 溶液 | A | B | C | D | E |
| 5mol/LH2SO4/mL | 40 | V1 | V2 | V3 | V4 |
| 饱和CuSO4/mL | 0 | 1 | 2 | V5 | 10 |
| H2O/mL | V6 | V7 | V8 | 5 | 0 |
①完成此实验设计,其中V5=_________V7=___________。
②为探究氢气生成速率要收集产生的气体,还需记录:___________________。
-
(14分)食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6] •3H2O。
42.2g K4[Fe(CN)6] •3H2O样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如下图所示。
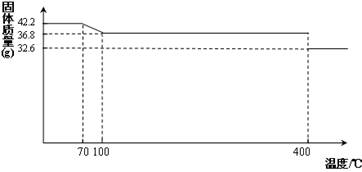
试回答下列问题:
(1)试确定150℃时固体物质的化学式为_______________。
(2)查阅资料知:虽然亚铁氰化钾自身毒性很低,但其水溶液与酸反应放出极毒的氰化氢(HCN)气体;亚铁氰化钾加热至一定温度时能分解产生氰化钾(KCN)。据此判断,烹饪食品时应注意的问题为___________________________________。
(3)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a_______0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=______________。
(4)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O=2H2SO4的转化。已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为________。则上述转化的重要意义在于________。
(5)已知Fe(OH)3的溶度积常数Ksp=1.1×10-36。室温时在FeCl3溶液中滴加NaOH溶液,当溶液中Fe3+沉淀完全时,控制pH应不小于________。
(提示:当某离子浓度小于10-5 mol•L-1时可以认为该离子沉淀完全了;lg1.1×10-36=-35.96)
-
黄血盐[亚铁氰化钾,K4Fe(CN)6·3H2O]可用作食盐添加剂,一种制备黄血盐的工艺如下所示:
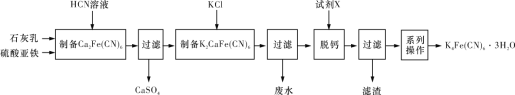
下列说法错误的是
A. HCN溶液有剧毒,含CN-的废水必须处理后才能排放
B. “废水”中含量较多的溶质为CaCl2
C. “试剂 X”可能是K2CO3
D. “系列操作”为蒸发结晶、过滤、洗涤、干燥
-
深井岩盐的主要配料为:精制盐、碘酸钾(KIO3)、亚铁氰化钾[K4Fe(CN)6·3H2O]。其中亚铁氰化钾的无水盐在高温下会发生分【解析】
3K4[Fe(CN)6] 2(CN)2↑+12KCN+N2↑+Fe3C+C。请回答下列问题:
2(CN)2↑+12KCN+N2↑+Fe3C+C。请回答下列问题:
(1)①基态Fe原子价电子排布图(轨道表示式)为_________________________
②C、N和O三种元素的第一电离能的大小顺序为_____________,原因是__________。
③IO3-的中心原子的杂化方式为______。一种与CN-互为等电子体的分子的电子式为_______。
④1molFe(CN)63−中含有σ键的数目为____mol。
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________(填晶体类型)。
(3)如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,该立方体中三价铁离子处于氧离子围成的________(填空间结构)空隙。
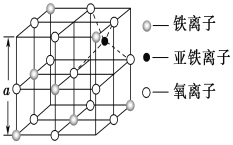
(4)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm﹣3,晶胞边长为4.28×10﹣10 m,则FexO中x=____。(用代数式表示,不要求算出具体结果)。
-
亚铁氰化钾俗称黄血盐,化学式为K4[Fe(CN)6].3H2O.黄血盐毒性很低,在空气中稳定且具有防止细粉状食品板结的性能,故用作食盐的抗结剂.但是在400℃左右黄血盐分解生成剧毒的氰化钾(KCN),与强酸作用也会生成极毒的氰化氢(HCN)气体。
完成下列填空:
(1)剧毒的KCN可以用双氧水处理,得到一种碱性气体和一种酸式盐.请写出该反应的化学方程式______。
(2)若往KCN溶液中通入少量的CO2气体,其反应的离子方程式______。已知电离常数(25℃):H2CO3:Ki1=4.3×10﹣7 ,Ki2=5.6×10﹣11,HCN:Ki1=4.9×10﹣10
(3)常温下,测得等物质的量浓度的KCN与HCN混合溶液的pH>7,则溶液中K+、H+、CN﹣、HCN浓度大小顺序为______。
(4)黄血盐作为食盐的抗结剂,必须严格控制其使用量,原因是______。
(5)黄血盐常用于Fe3+检验。请再写出一种检验Fe3+的试剂______,其相应的现象是______。
(6)FeCl3与Na2S反应,生成的产物与溶液的酸碱性有关.当pH<7时,有淡黄色沉淀产生,当pH>7时,生成黑色沉淀(Fe2S3).请写出往FeCl3溶液中滴加少量Na2S溶液的离子方程式:______。
-
黄血盐[亚铁氰化钾,K4[Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg•kgˉ1。一种制备黄血盐的工艺如下:
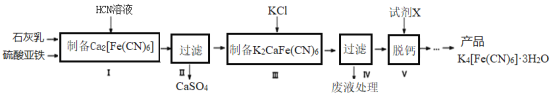
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为____________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为(填化学式)___________________。
(3)步骤Ⅴ所用的试剂 X 是______________________。
-
黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg·kg-1。一种制备黄血盐的工艺如下:
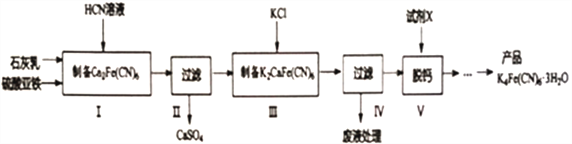
回答下列问题:
(1)步骤Ⅰ反应的化学方程式为_____________________________。
(2)步骤Ⅳ过滤所得的废液中含量较多的溶质为_______________________。(填化学式)
(3)步骤Ⅴ所用的试剂X是_________________。
(4)工艺中用到剧毒的HCN 溶液,含CN-的废水必须处理后才能排放。己知氢氰酸是一种具有苦杏仁特殊气味的无色剧毒液体,易挥发,25℃时,Ka(HCN)=6.25×10-10。
①NaCN 的电子式为_________________,反应CNˉ +H2O HCN+OHˉ在25℃时的平衡常数 K= _________________。(填数值)
HCN+OHˉ在25℃时的平衡常数 K= _________________。(填数值)
②处理含CN-废水的方法是:第一步控制pH>10,用NaClO溶液先将CN-“不完全氧化”为OCN-;第二步控制 pH为7.5~8.5,用NaClO“不完全氧化”OCNˉ生生成N2和两种盐。
第一步控制强碱性的主要目的是__________________________________。
第二步反应的离子方程式为______________________________。
-
(1)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是__________;1 mol该配离子中含σ键数目为________。
②该配合物中存在的作用力类型有_________(填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
(2)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其晶胞,晶胞边长为a nm。则硼原子与磷原子最近的距离为__________。 用M g·mol-1表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为__________g·cm-3。
(3) 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中3原子1的坐标为(1/2,1/2,0),则原子3的坐标分别为________________。

-
黄血盐[亚铁氰化钾,K4Fe(CN)6] 目前广泛用作食品添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg/kg。一种制备黄血盐的工艺如下:

回答下列问题:
(1)步骤I反应的化学方程式为______。
(2)步骤IV过滤所得的废液中含量较多的溶质为______(填化学式)。
(3)步骤V是将难溶的K2CaFe(CN)6与X反应脱钙生成K4Fe(CN)6,所用的试剂X是_____。(填名称)
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
①25°C时Ka(HCN)=6.25×10-10;计算25℃时0.01mol•L-1的HCN溶液的pH=____(lg2.5=0.4)。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN;第二步控制pH为7.5〜8.5,用NaClO溶液完全氧化OCN生成N2和两种盐(其中一种为酸式盐)。
第一步控制强碱性的主要目的是_______,第二步反应的离子方程式为______。
-
(7分)黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用做食盐添加剂(抗结剂),我国卫生部规定食盐中黄血盐的最大使用量为10mg·kgˉ1。黄血盐易溶于水,在水溶液中会电离出K+和[Fe(CN)6]4ˉ,其中CNˉ的电子式为 。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O
。它与硫酸反应的化学方程式为K4Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑
(1)上述反应是否为氧化还原反应?______ (填“是”或“不是”)。
(2)食盐经长时间火炒,“亚铁氰化钾”名称前的“亚铁”就去掉了,变成了剧毒物质氰化钾,这是因为黄血盐在超过4000C时会分解,试配平该反应的化学方程式:
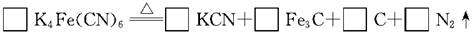
(3) 黄血盐可与高锰酸钾溶液反应,其化学方程式为
K4Fe(CN)6+ KMnO4+ H2SO4→KHSO4+ Fe2(SO4)3+MnSO4+HNO3+CO2↑+H2O(未配平)
①该反应的氧化产物有______________(填化学式)。
②若有1mol K4Fe(CN)6被高锰酸钾氧化,则消耗高锰酸钾的物质的量为______________mol。