已知:3CH4(g) + 2N2(g)3C(s) + 4N
H3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示:

下列说法正确的是
A.n(CH4)/n(N2)越大,CH4的转化率越高
B.n(CH4)/n(N2)不变时,若升温,NH3的体积分数会增大
C.b点对应的平衡常数比a点的大
D.a点对应的NH3的体积分数约为26%
高二化学选择题困难题
已知:3CH4(g) + 2N2(g)3C(s) + 4N
H3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示:

下列说法正确的是
A.n(CH4)/n(N2)越大,CH4的转化率越高
B.n(CH4)/n(N2)不变时,若升温,NH3的体积分数会增大
C.b点对应的平衡常数比a点的大
D.a点对应的NH3的体积分数约为26%
高二化学选择题困难题
已知:3CH4(g) + 2N2(g)3C(s) + 4N
H3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示:

下列说法正确的是
A.n(CH4)/n(N2)越大,CH4的转化率越高
B.n(CH4)/n(N2)不变时,若升温,NH3的体积分数会增大
C.b点对应的平衡常数比a点的大
D.a点对应的NH3的体积分数约为26%
高二化学选择题困难题查看答案及解析
氨气和氧气在某催化剂和不同温度下生成的产物如图所示。已知在800 ℃下,容积固定的密闭容器中发生反应①、②:
4NH3(g)+3O2(g)2N2(g)+6H2O(g) ①
4NH3(g)+5O2(g)4NO(g)+6H2O(g) ②
下列描述可说明两反应均达到平衡的是( )
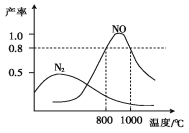
A.v(N2)=v(NO) B.反应①的焓变ΔH保持恒定
C.体系的密度不再发生变化 D.混合气体的平均相对分子质量不再发生变化
高二化学选择题困难题查看答案及解析
氨气和氧气在某催化剂和不同温度下生成的产物如图所示。已知在800 ℃下,容积固定的密闭容器中发生反应①、②:
4NH3(g)+3O2(g)2N2(g)+6H2O(g) ①
4NH3(g)+5O2(g)4NO(g)+6H2O(g) ②
下列描述可说明两反应均达到平衡的是( )
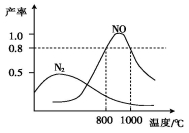
A.v(N2)=v(NO) B.反应①的焓变ΔH保持恒定
C.体系的密度不再发生变化 D.混合气体的平均相对分子质量不再发生变化
高二化学选择题困难题查看答案及解析
高二化学选择题中等难度题查看答案及解析
使反应4NH3(g)+3O2(g)⇌2N2(g)+6H2O在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol.此反应的平均速率v(X)为
A.v(NH3)=0.02 mol•L﹣1•s﹣1 B.v(O2)=0.01 mol•L﹣1•s﹣1
C.v(N2)=0.02 mol•L﹣1•s﹣1 D.v(H2O)=0.02 mol•L﹣1•s﹣1
高二化学选择题简单题查看答案及解析
使反应4NH3(g)+3O2(g)2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均反应速率可表示为
A.v(NH3)=0.02mol·L-1·s-1 B.v(O2)=0.01mol·L-1·s-1
C.v(N2)=0.02mol·L-1·s-1 D.v(H2O)=0.02mol·L-1·s-1
高二化学选择题简单题查看答案及解析
氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:
①4NH3(g)+3O2(g)2N2(g)+6H2O(g) △H=-1266.6kJ·mol-1,
②H2(g)+1/2O2(g)===H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)===H2O(g) △H3=+44.0kJ·mol-1
反应①在任何温度下都能自发进行的原因为___________;NH3分解为N2和H2的热化学方程式______________________。
(2)在Co-Al催化剂体系中,压强P0下氨气以一定流速通过反应器,在相同时间下测转化率。得到不同催化剂下氨气转化率随温度变化曲线如下图。使反应的活化能最小的催化剂为___________。同一催化剂下,温度高时NH3的转化率接近平衡转化率的原因_______________________________。如果增大氨气浓度(其它条件不变),则b点对应的点可能为___________。(填“a”、“c”或“d”)
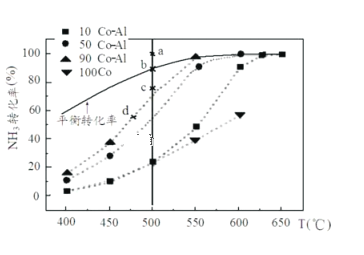
(3)T℃时,体积为2L的密闭容器中加入1.0molNH3和0.2molH2,20min达到平衡时,N2体积分数为20%,则T℃时平衡常数K=___________;0~20min时段,反应平均速率v(NH3)= _______;达到平衡后再加入1.0molNH3和0.2molH2,此时体系中v正___________v逆(填“>“<”或“=”)。
高二化学综合题困难题查看答案及解析
氨催化分解既可防治氨气污染,又能得到氢能源,得到广泛研究。
(1)已知:①反应I:4NH3(g)+3O2(g)2N2(g)+6H2O(g) ΔH1=-1266.6 kJ·mol-1
②H2(g)+O2(g)=H2O(l) △H2=-285.8 kJ·mol-1
③H2O(l)═H2O(g) ΔH3=+44.0 kJ·mol-1
则反应2NH3(g)N2(g)+3H2(g)的反应热△H=___。
(2)合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g) △H2,在10 L恒容密闭容器中加入4 mol CO和8 mol H2,测得CO的平衡转化率与温度和压强的关系如图所示,200℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |

①△H2_____(填“>”“<”或“=”)0。
②下列说法正确的是_______(填标号)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
③0〜3min内用CH3OH表示的反应速率v(CH3OH)=___(保留三位小数)。
④200℃时,该反应的平衡常数K=__。向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡__(填“正向”、“逆向”或“不”)移动。
(3)体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O22SO3,并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率(______________)
A. 等于p% B. 大于p% C. 小于p% D. 无法判断
高二化学综合题中等难度题查看答案及解析
(1)已知:N2(g)+3H2(g)2NH3(g)ΔH=﹣92.4 kJ•
,
2H2(g)+O2(g)====2H2O(l)ΔH=﹣571.6 kJ•,
则2N2(g)+6H2O(l)4NH3(g)+3O2(g) ΔH=_______。
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:

上图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出CO2和NO反应生成NO2和CO的热化学方程式:__________________________________。在反应体系中加入催化剂,E1和E2的变化是:E1__,E2__(填“增大”“减小”或“不变”),对反应热是否有影响?__(填“是”或“否”),原因是________________________________________。
(3)常温常压下断裂1 mol气体分子化学键所吸收的能量或形成1 mol气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):请完成下列问题。

热化学方程式2H2(g)+S2(g)===2H2S(g) ΔH=-229 kJ·mol-1,则X=________。
高二化学综合题中等难度题查看答案及解析

高二化学解答题中等难度题查看答案及解析