-
已知:①N2(g)+O2(g)=2NO(g) △H1=+180kJ·mol-1
②N2(g)+3H2(g) 2NH3(g) △H2=-92.4 kJ·mol-1
2NH3(g) △H2=-92.4 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6 kJ·mol-1
下列说法正确的是
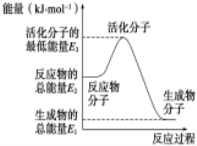
A.反应②中的能量变化如图所示,则△H2=E1-E3
B.N2的燃烧热为180 kJ·mol-1
C.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1molN2和3molH2,反应后放出的热量为Q1kJ,则Q1=92.4
D.氨的催化氧化反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-906 kJ·mol-1
-
已知:①N2(g)+O2(g)=2NO(g) ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)  2NH3(g) ΔH2=-92.4 kJ·mol-1
2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是( )
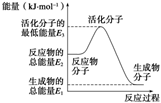
A.反应②中的能量变化如图所示,则ΔH2=E1-E3
B.H2的燃烧热为241.8 kJ·mol-1
C.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2充分反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1
D.氨的催化氧化反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g) ΔH=+906 kJ·mol-1
-
氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)已知:反应i:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ/mol
反应ii:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式_____。
(2)已知反应i断开1mol化学键所需的能量见下表:
| N≡N | H—H | N—H |
| 键能/kJ·mol-1 | 945 | 436 | ? |
则断开1molN-H键所需的能量是_______kJ
(3)如图表示反应i在500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中M点数据计算N2的平衡体积分数______;该反应的化学平衡常数K的表达式______。
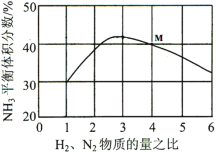
(4)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是______(填“温度”或“压强”);判断L1、L2的大小关系并说明理由_______。

(5)电化学气敏传感器可用于检测环境中NH3的含量,其工作原理如图所示:
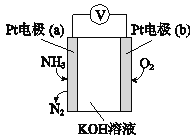
①反应消耗NH3和O2的物质的量之比为____。
②a极的电极反应式为______。
-
已知:
①N2(g)+O2(g)===2NO(g) ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)  2NH3(g) ΔH2=-92.4 kJ·mol-1
2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是
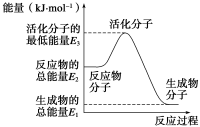
A.反应②中的能量变化如图所示,则ΔH2=E1-E3
B.H2的燃烧热为241.8 kJ·mol-1
C.氨的催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH=+906 kJ·mol-1
D.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1
-
已知:① N2 (g) + 3H2 (g) 2NH3 (g) ΔH=-92.4 kJ/mol
2NH3 (g) ΔH=-92.4 kJ/mol
② 2H2(g)+SO2 (g) S(g)+2H2O (g) ΔH =+90.4 kJ/mol
S(g)+2H2O (g) ΔH =+90.4 kJ/mol
③ 2H2(g)+CO(g) CH3OH (g) ΔH=-90.8 kJ/mol
CH3OH (g) ΔH=-90.8 kJ/mol
请回答:
(1)上述变化过程中放出热量的是____________(填序号,下同)。
(2)4 g H2 (g) 完全反应生成甲醇气体时,ΔH =____________kJ/mol。
(3)生成1 mol NH3 (g) 的放出的热量为____________kJ。
-
已知一定温度下:①N2(g)+O2(g)===2NO(g) ΔH1=+180 kJ·mol-1 ②N2(g)+3H2(g) 2NH3(g) ΔH2=-92.4 kJ·mol-1 ③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1下列说法正确的是( )
2NH3(g) ΔH2=-92.4 kJ·mol-1 ③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1下列说法正确的是( )
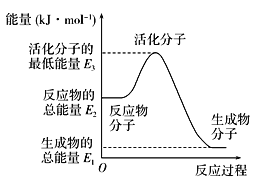
A. 反应②中的能量变化如上图所示,则ΔH=E1-E3
B. 2 mol H2(g)完全燃烧生成液态水时放出的热量小于483.6 kJ
C. 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1
D. 氨催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH=+906 kJ·mol-1
-
已知:① N2 (g) + 3H2 (g)  2NH3 (g) ΔH =-92.4 kJ/mol
2NH3 (g) ΔH =-92.4 kJ/mol
② 2H2 (g) + SO2 (g)  S (g) + 2H2O (g) ΔH =+90.4 kJ/mol
S (g) + 2H2O (g) ΔH =+90.4 kJ/mol
③ 2H2 (g) + CO (g)  CH3OH (g) ΔH =-90.8 kJ/mol
CH3OH (g) ΔH =-90.8 kJ/mol
请回答:
(1)上述变化过程中放出热量的是________(填序号,下同),吸收热量的是________。
(2)4 g H2 (g) 完全反应生成甲醇气体时,ΔH =________ kJ/mol。
(3)生成1 mol NH3 (g) 的放出的热量为________ kJ。
-
(1)已知:N2(g)+3H2(g) 2NH3(g)ΔH=﹣92.4 kJ•
2NH3(g)ΔH=﹣92.4 kJ• ,
,
2H2(g)+O2(g)====2H2O(l)ΔH=﹣571.6 kJ• ,
,
则2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ΔH=_______。
4NH3(g)+3O2(g) ΔH=_______。
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:

上图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出CO2和NO反应生成NO2和CO的热化学方程式:__________________________________。在反应体系中加入催化剂,E1和E2的变化是:E1__,E2__(填“增大”“减小”或“不变”),对反应热是否有影响?__(填“是”或“否”),原因是________________________________________。
(3)常温常压下断裂1 mol气体分子化学键所吸收的能量或形成1 mol气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):请完成下列问题。

热化学方程式2H2(g)+S2(g)===2H2S(g) ΔH=-229 kJ·mol-1,则X=________。
-
下列叙述正确的是( )
A. 已知2H2(g)+O2(g)=2H2O(g) ΔH=-480.4kJ/mol ,则H2的燃烧热为ΔH=-240.2kJ/mol
B. 已知N2(g)+3H2(g) 2NH3(g)ΔH=-92.0kJ/mol,则将1molN2(g))和3molH2(g)置于一密闭容器中充分反应后放出的热量小于92.0kJ
2NH3(g)ΔH=-92.0kJ/mol,则将1molN2(g))和3molH2(g)置于一密闭容器中充分反应后放出的热量小于92.0kJ
C. 已知甲烷氧化:CH4(g)+O2(g)=CO2(g) +2H2(g)ΔH=-322.0kJ/mol,则反应物的键能总和大于生成物的键能总和
D. 测量中和热的实验时,应选用的试剂为50ml 0.5mol/L的盐酸与50ml 0.5mol/L的NaOH溶液
-
在同温同压下,下列各组热化学方程式中△H1>△H2的是
A.2H2(g)+O2(g)═2H2O(l)△H1; 2H2(g)+O2(g)═2H2O(g)△H2
B.N2(g)+3H2(g)⇌2NH3(g)△H1; CaCO3(s)═CaO(s)+CO2 (g)△H2
C.C(s)+ O2(g)═CO(g)△H1; C(s)+O2(g)═CO2(g)△H2
O2(g)═CO(g)△H1; C(s)+O2(g)═CO2(g)△H2
D.H2(g)+Cl2(g)═2HCl(g)△H1;  H2(g)+
H2(g)+ Cl2(g)═HCl(g)△H2
Cl2(g)═HCl(g)△H2
2NH3(g)ΔH=﹣92.4 kJ•
,
,
4NH3(g)+3O2(g) ΔH=_______。







