-
某常用的血液抗凝剂由(NH4)2C2O4和Na2C2O4组成,为确定其成分,某同学进行如下实验:
①氮元素测定:精确称取a g样品,加适量蒸馏水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量浓NaOH溶液,加热装置A产生水蒸气,装置B中产生的氨气全部吹出,用V1mLc1mol/L的硫酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol/LNaOH标准溶液过剩的H2SO4,到终点时消耗V2mLNaOH溶液。
②C2O42-离子的测定:取实验①B装置中剩余溶液于锥形瓶中,先用稀硫酸酸化,再用0.1000mol/L的酸性KMnO4溶液滴定,终点时消耗酸性KMnO4溶液V3mL。
③计算:根据实验①计算氮元素的含量,根据②计算C2O42-的含量,从而得到样品中(NH4)2C2O4和Na2C2O4的比例。完成下列问题:

(1)装置A中长玻璃管的作用是 。
(2)用NaOH标准溶液滴定过剩H2SO4时, NaOH标准溶液盛装在 中(填仪器名称)。
(3)样品中氮元素的质量分数表达式为 。
(4)实验②中发生的离子方程式为 。用酸性高锰酸钾溶液滴定时终点现象为 。
(5)实验②中滴定开始和结束时,滴定管的读数如图所示,则所用酸性KMnO4溶液体积V3= mL

(6)下列操作可能使实验②测定结果偏低的是 。
A.滴定管在注入溶液前用蒸馏水洗后未用标准溶液润洗
B.开始时酸式滴定管尖嘴部分有气泡,滴定过程中消失
C.滴定前仰视滴定管读数,滴定后平视滴定管读数
-
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验。
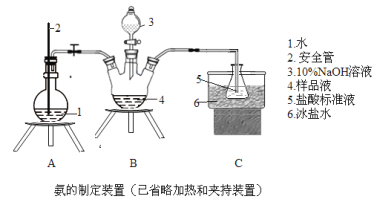
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL c1 mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液。

②氯的测定。
回答下列问题:
(1)装置中安全管的作用原理是______________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用________式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为_________________。
(4)测定氨前应该对装置进行气密性检查,若气密性不好测定结果将_________(填“偏高”或“偏低”)。
(5)氯的测定采用莫尔法,莫尔法是一种沉淀滴定法,用标准硝酸银溶液滴定,进行测定溶液中Cl-的浓度。已知:
| 银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| 溶解度(mol·L-1) | 1.3410-6 | 7.110-7 | 1.110-8 | 6.510-5 | 1.010-6 |
①若用AgNO3溶液滴定待测液,可选为滴定指示剂的是__________。
A.NaCl B.BaBr2 C.Na2CrO4 D KSCN
②滴定终点的现象是_____________________________________。
-
某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为测定其组成,进行如下实验。
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1mLc1mol·L-1的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。回答下列问题:
(1)装置中安全管的作用原理是___。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用___式滴定管,可使用的指示剂为___。
(3)样品中氨的质量分数表达式为___。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___(填“偏高”或“偏低”)。
(5)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1,c(CrO42-)为___mol·L-1。
(已知:Ksp(Ag2CrO4)=1.12×10-12)
(6)X的化学为[Co(NH3)6]Cl3。制备X的反应化学方程式为___。
-
某小组以CoCl2·6H2O、NH4Cl、H2O2、液氨、氯化铵为原料,在活性炭催化下合成了橙黄色晶体X。为测定其组成,进行如下实验。
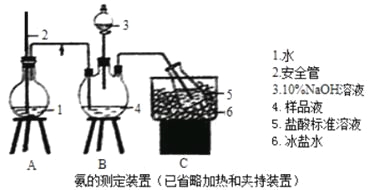
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mLc1mol·L—1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L—1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是_________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_____式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为____________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是___________;滴定终点时,若溶液中c(Ag+)=2.0×10—5mol·L—1,c(CrO42—)为______mol·L—1。(已知:Ksp(Ag2CrO4)=1.12×10—12)
(6)经测定,样品X中钴、氨、氯的物质的量之比为1:6:3,钴的化合价为______,制备X的化学方程式为____________________;X的制备过程中温度不能过高的原因是__________________。
-
Ⅰ.某小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入圆底烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mL c1mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不在消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)用NaOH标准溶液滴定过剩的HCl时,应使用___式滴定管,该滴定实验可使用的指示剂为___,达到滴定终点的现象为___。
(2)样品中氨的质量分数表达式为___。
(3)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1 ,c(CrO42-)为___mol·L-1。(已知:Ksp(Ag2CrO4)=1.12×10-12)。
Ⅱ.已知
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(4)则用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为___加入___调节pH为___(保留两位有效数字),铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。
-
某小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入圆底烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mL c1mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)用NaOH标准溶液滴定过剩的HCl时,应使用_______式滴定管,该滴定实验可使用的指示剂为_______,达到滴定终点的现象为____________________________
(2)样品中氨的质量分数表达式为__________________________
(3)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1 ,c(CrO42-)为________mol·L-1。(已知:Ksp(Ag2CrO4)=1.12×10-12)。
-
分析化学常用草酸钠晶体(Na2C2O4溶液无色)作为基准物质测定酸性KMnO4
溶液的浓度。请回答下列问题:
(1)Na2C2O4溶液与酸性KMnO4溶液反应的离子方程式是_________________________
(2)称取Wg Na2C2O4晶体配成100mL溶液,配制时使用的一种主要仪器是_________
(3)移取20.00 mLNa2C2O4溶液置于锥形瓶中,则酸性KMnO4溶液装在_______式滴定管中(填“酸”或“碱”)
(4)滴定终点的现象是_________________________________
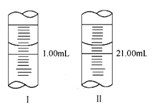
(5)若滴定管起始读数和终点读数如图所示,则酸性KMnO4溶液的物质的量浓度为_____________________________
(6)下列操作导致测定的酸性KMnO4溶液浓度偏高的是____
a.配制Na2C2O4溶液定容时俯视
b.锥形瓶用蒸馏水洗净后,再用Na2C2O4溶液润洗2—3次
c.滴定前滴定管中有气泡,滴定终点滴定管中气泡消失
d.滴定前仰视读数,滴定终点俯视读数
-
滴定实验是化学学科中重要的定量实验,氧化还原滴定实验与酸碱中和滴定类似。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
(1)写出KMnO4溶液滴定H2C2O4溶液的离子方程式______________________________________;滴定时,KMnO4溶液应装在______(“酸”或“碱”)式滴定管中,滴定终点时滴定现象是_________________________。
(2)下列操作会导致测定结果偏低的是_________。
A.滴定管在装液前未用标准KMnO4溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(3)计算:血液中含钙离子的浓度为_________mol/L。
-
我国国标推荐的食品药品中Ca元素含量的测定方法之一:利用Na2C2O4将处理后的样品中的Ca2+沉淀,过滤洗涤,然后将所得CaC2O4固体溶于过量的强酸,最后使用已知浓度的KMnO4溶液通过滴定来测定溶液中Ca2+的含量。针对该实验中的滴定过程,回答以下问题:
(1)KMnO4溶液应该用__(填“酸式”或“碱式”)滴定管盛装,除滴定管外,还需要的玻璃仪器有__。
(2)试写出滴定过程中发生反应的离子方程式:__。
(3)滴定终点的颜色变化:溶液由__色变为__色。
(4)以下哪些操作会导致测定的结果偏高__(填字母编号)。
a.装入KMnO4溶液前未润洗滴定管
b.滴定结束后俯视读数
c.滴定结束后,滴定管尖端悬有一滴溶液
d.滴定过程中,振荡时将待测液洒出
(5)某同学对上述实验方法进行了改进并用于测定某品牌的钙片中的钙元素(主要为CaCO3)含量,其实验过程如下:取2.00g样品加入锥形瓶中,用酸式滴定管向锥形瓶内加入20.00mL浓度为0.10mol·L-1的盐酸(盐酸过量),充分反应一段时间,用酒精灯将锥形瓶内液体加热至沸腾,数分钟后,冷却至室温,加入2~3滴酸碱指示剂,用浓度为0.10mol·L-1的NaOH溶液滴定至终点,消耗NaOH溶液8.00mL。[提示:Ca(OH)2微溶于水,pH较低时不会沉淀]
①为使现象明显、结果准确,滴定过程中的酸碱指示剂应选择__(填“石蕊”、“甲基橙”或“酚酞”)溶液;
②实验过程中将锥形瓶内液体煮沸的目的是___;
③则此2.00g钙片中CaCO3的质量为__g。
-
氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMn04滴定H2C2O4的离子方程式_____________________。
(2)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(3)判断滴定终点的方法是________________________。
(4)误差分析:(填“偏高”、“偏低”或“无影响”)
①如果滴定管用蒸馏水洗后未用酸性KMnO4标准液润洗,则测量结果________。
②滴定前后读数都正确,但滴定前有气泡,而滴定后气泡消失,则测量结果________。
(5)计算:血液中含钙离子的浓度为_____mol/L。





