-
取20.00 mL 0.50 mol·L-1 NaOH溶液,恰好将未知浓度的H2SO4溶液20.00 mL滴定至终点,下列说法正确的是( )
A.该实验不需要指示剂
B.用量筒量取上述硫酸的体积
C.H2SO4的浓度为1.00 mol·L-1
D.参加反应的H+和OH-的物质的量相等
高二化学选择题中等难度题查看答案及解析
-
取20.00 mL 0.50 mol·L-1 NaOH溶液,恰好将未知浓度的H2SO4溶液20.00 mL滴定至终点,下列说法正确的是( )
A.该实验不需要指示剂
B.用量筒量取上述硫酸的体积
C.H2SO4的浓度为1.00 mol·L-1
D.参加反应的H+和OH-的物质的量相等
高二化学单选题中等难度题查看答案及解析
-
室温下用0.10 mol·L-1的NaOH溶液滴定20.00mL未知浓度的CH3COOH,滴定终点消耗20.00mL的NaOH溶液。下列说法正确的是
A.滴定终点时溶液由无色变为浅红色且保持半分钟颜色不变
B.滴定终点时混合溶液的pH=7
C.滴定终点时反应的热效应即为中和热
D.滴定终点时两者恰好完全反应
高二化学选择题中等难度题查看答案及解析
-
某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液.
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
滴定次数
盐酸体积
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.30
3
20.00
0.00
16.22
回答下列问题:
(1)步骤①中,量取20.00mL待测液应使用________(填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果 ______(填“偏大”、“偏小”或“无影响”).
(2)步骤②中,滴定时眼睛应注视_______(填仪器名称),判断到达滴定终点的依据是_____________________________________________________________
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次,其可能的原因是(填字母)___
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡 B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成 D.滴定终点时,俯视读数
(4)根据上表记录数据,通过计算可得该盐酸的浓度为________ mol/L
高二化学实验题中等难度题查看答案及解析
-
(16分)某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液。
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
滴定次数
盐酸体积
NaOH溶液体积读数(mL)
滴定前
滴定后
1
20.00
0.00
18.10
2
20.00
0.00
16.30
3
20.00
0.00
16.22
请回答下列问题:
(1)步骤①中,量取20.00mL待测液应使用________ (填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果__________(填“偏大”、“偏小”或“无影响”)。
(2)判断到达滴定终点的现象是___________________________________________。
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次的体积,其可能的原因是___________________(填字母)
A.滴定前滴定管尖嘴有气泡,滴定结束时无气泡
B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成
D.滴定终点时,俯视读数
(4)由以上数据,该盐酸的物质的量浓度为________,若要计算盐酸溶液中盐酸的质量分数还缺少的物理量是:;(请注明单位)。如缺少的数据用字母a表示,则盐酸溶液中盐酸的质量分数为;
(5)下列操作会使结果偏高的是________(多选倒扣分)
A.碱式滴定管用蒸馏水洗净后,即注入标准NaOH溶液
B.用酸式滴定管取用待测酸液前,尖嘴部分有气泡,取用过程中气泡消失
C.滴定前,读碱液体积时仰视;滴定后,读碱液体积时俯视
D.滴定前,盛放盐酸的锥形瓶不干燥
高二化学实验题简单题查看答案及解析
-
如图是用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞作指示剂)的滴定曲线。下列说法正确的是( )
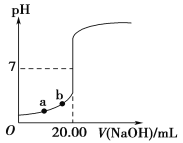
A.指示剂变色时,说明盐酸与NaOH恰好完全反应
B.当滴加NaOH溶液10.00 mL时,该混合液的pH=1+lg3
C.水电离出的氢离子浓度:a>b
D.盐酸的物质的量浓度为0.010 0 mol·L-1
高二化学单选题中等难度题查看答案及解析
-
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol/L的NaOH溶液滴定上述稀硫酸25mL,滴定终点时消耗NaOH溶液15mL。
(1)该学生用标准0.14mol/L NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO425mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。
C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。
F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度.
①滴定操作的正确顺序是(用序号填写):________。
②该滴定操作中应选用的指示剂是:_______。
③在G操作中如何确定终点?________。
(2)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度______mol/L。(计算出结果到小数点后二位)
高二化学实验题简单题查看答案及解析
-
常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。已知在点③处恰好中和。下列说法错误的是

A.该温度下CH3COOH的电离平衡常数约为1.8 ×10-5
B.点①处溶液中c(CH3COO-)<c(CH3COOH)
C.点③处溶液中c(OH-)= c(CH3COOH)+c(H+)
D.滴定过程中不可能出现:c(CH3COOH) >c(CH3COO-)> c(OH-)> c(Na+)> c(H+)
高二化学单选题中等难度题查看答案及解析
-
某学生用0.10 mol·L-1标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
实验序号
待测液体积(mL)
所消耗NaOH标准液的体积(mL)
滴定前
滴定后
1
20.00
0.50
20.54
2
20.00
6.00
26.00
3
20.00
1.40
21.36
(1)盐酸的物质的量浓度为_____。
(2)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是_____(填“偏高”或“偏低”或“无影响”)。
(3)下列有关实验的说法正确的是______。
A.在测定中和反应的反应热实验中,至少要读两次温度
B.可用pH试纸测定新制氯水中的pH
C.中和滴定实验中,洗净后的锥形瓶不需要干燥
D.向CH3COONa溶液中滴入石蕊试液,溶液变蓝
E.向白色ZnS沉淀上滴加CuSO4溶液,沉淀变为黑色,说明Ksp(ZnS)<Ksp(CuS)
(4)常温下,pH=5的盐酸和pH=9的氢氧化钠溶液以体积比9∶11混合,则混合液的pH=_________。
高二化学综合题中等难度题查看答案及解析
-
某学生用0.10 mol/L标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
实验序号
待测液体积(mL)
所消耗NaOH标准液的体积(mL)
滴定前
滴定后
1
20.00
0.50
20.54
2
20.00
6.00
26.00
3
20.00
1.40
21.36
(1)滴定时选用酚酞试液作指示剂,如何判断滴定达到终点。
(2)盐酸的物质的量浓度为_____________
(3)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是(填“偏高”或“偏低”或“无影响”,下同)。
(4)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在________中(填“甲”或“乙”),该反应的离子方程式为:。

高二化学填空题中等难度题查看答案及解析