-
(1)已知3N2H4(l) 4NH3(g)+N2(g) △H = —336.6kJ/mol,
4NH3(g)+N2(g) △H = —336.6kJ/mol,
N2(g)+3H2(g) 2NH3(g) △H = —92.4kJ/mol,
2NH3(g) △H = —92.4kJ/mol,
则N2H4(g) N2(g)+2H2(g) △H = ________________。
N2(g)+2H2(g) △H = ________________。
(2)写出下列物质的电离方程式:
①NaHSO4___________________________________,
②K2SO4_____________,
③NH4NO3___________________________。
(3)写出下列物质的电子式:
Na2S:_________; CO2:_________。
-
肼(N2H4)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图1。已知200 ℃时:
反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ/mol
反应Ⅱ:N2H4(g)+H2(g)=2NH3(g) ΔH2=-41.8 kJ/mol
下列说法不正确的是( )
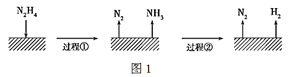
A.图1所示过程①是放热反应,②是吸热反应
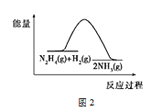
B.反应Ⅱ的能量过程示意图如图2所示
C.断开3 mol N2H4(g)中的化学键吸收的能量小于形成1 mol N2(g)和4 mol NH3(g)中的化学键释放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为:N2H4(g)= N2(g)+2H2(g) ΔH=-50.7 kJ/mol
-
化学反应N2+3H2  2NH3的能量变化如下图所示,该反应的热化学方程式是( )
2NH3的能量变化如下图所示,该反应的热化学方程式是( )
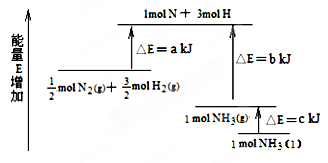
A.N2(g)+3H2(g)  2NH3(l) ⊿H =2(a—b—c)kJ·mol-1
2NH3(l) ⊿H =2(a—b—c)kJ·mol-1
B.N2(g)+3H2(g)  2NH3(g) ⊿H =2(b—a)kJ·mol-1
2NH3(g) ⊿H =2(b—a)kJ·mol-1
C.1/2N2(g)+3/2H2(g)  NH3(l) ⊿H = (b+c—a)kJ·mol-1
NH3(l) ⊿H = (b+c—a)kJ·mol-1
D.1/2N2(g)+3/2H2(g)  NH3(g) ⊿H = (a+b)kJ·mol-1
NH3(g) ⊿H = (a+b)kJ·mol-1
-
已知断裂1 molN≡N键吸收能量为945.6 kJ,形成1 mol H—N键放出能量为391 kJ,若1 mol N2和3 mol H2完全反应:N2+3H2 2NH3,放出的能量为92.4 kJ,则断裂1 molH—H键吸收的能量是( )
2NH3,放出的能量为92.4 kJ,则断裂1 molH—H键吸收的能量是( )
A. 436 kJ B. 433.6 kJ C. 463 kJ D. 869 kJ
-
已知断裂1 molN≡N键吸收能量为945.6 kJ,形成1 mol H—N键放出能量为391 kJ,若1 mol N2和3 mol H2完全反应:N2+3H2 2NH3,放出的能量为92.4 kJ,则断裂1 molH—H键吸收的能量是( )
2NH3,放出的能量为92.4 kJ,则断裂1 molH—H键吸收的能量是( )
A. 436 kJ B. 433.6 kJ C. 463 kJ D. 869 kJ
-
已知断裂1 molN≡N键吸收能量为945.6 kJ,形成1 mol H—N键放出能量为391 kJ,若1 mol N2和3 mol H2完全反应:N2+3H2 2NH3,放出的能量为92.4 kJ,则断裂1 molH—H键吸收的能量是( )
2NH3,放出的能量为92.4 kJ,则断裂1 molH—H键吸收的能量是( )
A. 436 kJ B. 433.6 kJ C. 463 kJ D. 869 kJ
-
已知断开1 mol H—H键吸收的能量为436 kJ,形成1 mol H—N键放出的能量为391 kJ,根据化学方程式N2+3H2 2NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N键需吸收的能量是
2NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N键需吸收的能量是
A. 431 kJ B. 945.6 kJ C. 649 kJ D. 869 kJ
-
已知断开1mol H—H键吸收的能量为436kJ,形成1mol H—N键放出的能量为391kJ,根据化学方程式N2+3H2 2NH3,反应完1mol N2放出的能量为92.4kJ,则断开1mol N≡N键需吸收的能量是( )
2NH3,反应完1mol N2放出的能量为92.4kJ,则断开1mol N≡N键需吸收的能量是( )
A.431kJ B.945.6kJ C.649kJ D.869kJ
-
已知N≡N键能为946 KJ/mol,H—N键能为391KJ/mol,根据化学方程式:N2 + 3H2  2NH3 ΔH=-92 KJ/mol,则H—H键的键能是
2NH3 ΔH=-92 KJ/mol,则H—H键的键能是
A. < 436 KJ/mol B. 436 KJ/mol C. 497 KJ/mol D. 467 KJ/mol
-
已知:①N2(g)+O2(g)===2NO(g) ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)  2NH3(g) ΔH2=-92.4 kJ·mol-1
2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是 ( )
A. 反应②中的能量变化如图所示:
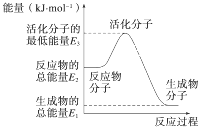
则ΔH2=E1-E3
B. H2的燃烧热为241.8 kJ·mol-1
C. 氨的催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+ 6H2O(g) ΔH=+906 kJ·mol-1
D. 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,最终反应放出的热量小于92.4 kJ,
4NH3(g)+N2(g) △H = —336.6kJ/mol,
2NH3(g) △H = —92.4kJ/mol,
N2(g)+2H2(g) △H = ________________。



