-
(1)化学反应速率可通过实验测定。要测定不同反应时刻反应物或生成物的浓度,可通过观察和测量体系中的某一物质的相关性质,再进行适当的转换和计算。如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的________来实现;在KMnO4与H2C2O4反应中,可通过观察单位时间内_________变化来测定该反应的速率;在Na2S2O3+H2SO4==Na2SO4+S↓+SO2+H2O反应中,该反应速率的快慢可通过_______来判断。
(2)已知:Na2S2O3 + H2SO4 == Na2SO4 + SO2↑+ S↓+ H2O。某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
实验序号
反应温度
Na2S2O3浓度
稀硫酸
H2O
V/mL
c/(mol/L)
V/mL
c/(mol/L)
V/mL
①
20
10.0
0.10
10.0
0.50
0
②
40
V1
0.10
V2
0.50
V3
③
20
V4
0.10
4.0
0.50
V5
该实验①、②可探究___________对反应速率的影响,因此V1、V2和V3分别是________、________、________。实验①、③可探究__________对反应速率的影响,因此V4、V5分别是_________、_________。
高二化学实验题中等难度题查看答案及解析
-
(6分)化学反应速率可通过实验测定。要测定不同反应时刻反应物或生成物的浓度,可通过观察和测量体系中的某一物质的相关性质,再进行适当的转换和计算。如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的________来实现;在KMnO4与H2C2O4反应中,可通过观察单位时间内________________变化来测定该反应的速率;在Na2S2O3+H2SO4→Na2SO4+S↓+SO2↑+H2O反应中,该反应的速率可通过___________来测定。
高二化学填空题简单题查看答案及解析
-
(6分) 通过实验测定反应速率的方法有多种,如比较锌粒与不同浓度硫酸反应时的速率,可通过测定收集等体积H2需要的__________来实现;在KMnO4与H2C2O4反应中,可通过测定________来测定该反应的速率;在Na2S2O3和H2SO4反应中,该反应的速率可通过___________________来测定。
高二化学填空题简单题查看答案及解析
-
(7分) 通过实验测定反应速率的方法有多种,如比较锌粒与不同浓度硫酸反应时的速率,可通过测定___________________来实现;在KMnO4与H2C2O4反应中,可通过测定_______________________来测定该反应的速率。请写出H2C2O4与H2SO4酸化的KMnO4反应的化学方程式_________________________________________________________。
高二化学填空题简单题查看答案及解析
-
对于反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,在测量化学反应速率时,以下相关性质不可以利用的为( )
A.气体的体积和体系的压强
B.溶液颜色的深浅
C.H+浓度的变化
D.固体物质的体积
高二化学选择题中等难度题查看答案及解析
-
19.下列说法正确的是
A.在“研究反应速率的影响因素”实验中:Na2S2O3+H2SO4=Na2SO4+S+SO2+H2O,可通过观察产生气泡的快慢来比较不同条件下该反应的速率大小
B.为了精确测定盐酸与氢氧化钠溶液反应的反应热,当两者混合后,立即读取温度计的读数,防止热量散失
C.将铁粉、碳粉、少量氯化钠和水混合放在塑料袋中搓揉,用手触摸会感觉到发热,袋里产生大量铁锈
D.酸碱中和滴定实验中,终点判断过迟,导致标准液滴多,只能重新滴定
高二化学选择题中等难度题查看答案及解析
-
(10分)某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积。
设计的简易实验装置如图。该实验的主要操作步骤如下:

a.配制浓度均为1 mol·L-1盐酸和醋酸溶液;
b.用________________量取10.00 mL1 mol·L-1盐酸和醋酸溶液分别加入两个锥形瓶中;
c.分别称取除去表面氧化膜的镁带a g,并系于铜丝末端,a的数值至少为________g;d.在广口瓶中装足量的水,按图连接好装置;检查装置的气密性;e.将铜丝向下移动,使足量镁带浸入酸中,至反应完全,记录________;
f.反应结束后待温度恢复到室温,若丙中液面高于乙中液面,读取量筒中水的体积前,应________,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题:
(1)用文字表述d检查该装置气密性的操作与观察方法:________。
(2)本实验中应选用________(填序号)的量筒。
A.100 mL B.200 mL C.500 mL
(3)简述速率不等的原因________,铜丝不与酸接触的原因是________。
高二化学实验题简单题查看答案及解析
-
(12分)某研究性学习小组为证明在同温同压下,相同浓度相同体积的不同强度的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积。设计的简易实验装置如图。
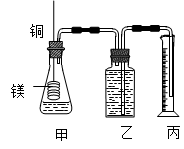
该实验的主要操作步骤如下:
a.配制浓度均为1 mol·L-1盐酸和醋酸溶液;
b.用 ①量取10.00 mL1 mol·L-1盐酸和醋酸溶液分别加入两个锥形瓶中;
c.分别称取除去表面氧化膜的镁带a g,并系于铜丝末端,a的数值至少为 ② g;d.在广口瓶中装足量的水,按图连接好装置;检查装置的气密性;e.将铜丝向下移动,使足量镁带浸入酸中,至反应完全,记录 ③ ;
f.反应结束后待温度恢复到室温,若丙中液面高于乙中液面,读取量筒中水的体积前,应 ④ ,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题:
(1)用文字表述d检查该装置气密性的操作与观察方法: ⑤ 。
(2)本实验中应选用 ⑥ (填序号)的量筒。
A.100 mL B.200 mL C.500 mL
(3)简述速率不等的原因 ⑦ ,铜丝不与酸接触的原因是 ⑧ 。
高二化学实验题极难题查看答案及解析
-
(12分)某研究性学习小组为了证明在同温同压下,相同浓度相同体积的酸性不同的一元酸与足量镁带反应时,生成氢气的体积相同而反应速率不同,同时测定实验室条件下的气体摩尔体积。设计的简易实验装置如图所示。该实验的主要操作步骤如下:
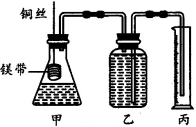
①配制浓度均为l mol·L-1的盐酸和醋酸溶液;
②用________量取10.00 mL l mol·L-1的盐酸和醋酸溶液分别加入到两个锥形瓶中;
③分别称取除去表面氧化膜的镁带a g,并系于铜丝,末端,a的数值至少为___________;
④在广口瓶中装足量的水,按图所示连接好装置,检查装置的气密性。
⑤将铜丝向下移动,使足量镁带浸人酸中(铜丝不与酸接触),至反应完全,记录___________;
⑥反应结束后待温度恢复到室温,调整乙与丙中液面相平,读出量筒中水的体积为V mL。请将上述步骤补充完整并回答下列问题:
(1)本实验中应选用___________(填序号)的量筒。
A.100 mL B.200 mL C.500 mL
(2)若水蒸气的影响忽略不计,在实验室条件下,气体摩尔体积的计算式为:Vm=_______。
(3)简述速率不等的原因___________,
高二化学实验题困难题查看答案及解析
-
中和热测定实验中,通过简易量热计直接测得的数据是
A. 反应的热量变化 B. 体系的温度变化
C. 酸或碱的浓度变化 D. 生成水的物质的量
高二化学单选题中等难度题查看答案及解析