-
溴化钙是一种重要的化工原料,常见有
和
等结晶形式。某兴趣小组以废铁屑为原料制备
的主要流程:
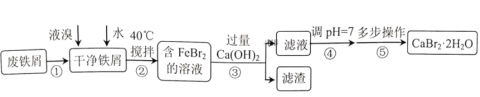
相关信息如下:
①
吸湿性强。
②34℃时结晶得到
,
加热至210℃得到
。
请回答:
(1)步骤①的目的是去除废铁屑表面的油污,方法是________。
(2)实验室模拟海水提取溴的过程中,用苯萃取溶液中的溴,选出其正确操作并按顺序列出字母:涂凡士林→检漏→()→()→()→()→()→清洗干净。________
a.打开玻璃塞放气
b.打开旋塞放气
c.将溶液和苯转移至分液漏斗中,塞上玻璃塞
d.双手托住分液漏斗,右手压住玻璃塞,左手握住旋塞,上下颠倒振荡
e.右手压住玻璃塞,左手握住旋塞,将分液漏斗倒转振荡
f.置于铁架台铁圈上静置,打开玻璃塞,将旋塞拧开,放出下层液体
g.从下口放出溴的苯溶液
h.从上口倒出溴的苯溶液
(3)步骤④调pH=7,适宜加入的试剂是________,通过调节分液漏斗的活塞可以控制添加液体的速率。当溶液pH接近7时,滴加试剂的分液漏斗的活塞应如图中的________(填序号)所示。

(4)下列有关说法正确的是________。
A.步骤②反应控制在40℃左右,原因是防止反应过于剧烈并减少液溴挥发
B.步骤③滤渣成分只有
、
和
C.为使
快速结晶,可用冰水浴进行冷却
D.步骤⑤包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等多步操作
(5)制得的
可以通过如下步骤测定其纯度:①称取样品质量;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤,洗涤,干燥;④称量。
若实验操作规范而测定结果偏低,其可能的原因是________。
高三化学工业流程困难题查看答案及解析
-
环戊烯(
,
)是一种重要的有机化工原料,可用环成二烯(
,
)制备。已知:
反应Ⅰ
反应Ⅱ
(环戊烷)
反应Ⅲ
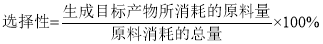
(1)某温度下,将环戊二烯和HI按物质的量之比1∶2(总物质的量为amol)充入容积为2L的恒容密闭容器中,发生反应:
。
①该反应自发进行的条件是__________。
②下列有关该反应的叙述,不正确的是__________。
A.气体压强不变,说明反应达到平衡状态
B.升高温度,有利于提高环戊烯的产率
C.反应达到平衡时,C5H6和HI的转化率相等
D.通入惰性气体,有利于提高环戊二烯的平衡转化率
(2)以
为催化剂,如图1为25℃时环戊二烯氢化过程,环戊烯与环戊烷的各组分含量(物质的量含量)随时间(t)的变化。为研究不同温度下催化剂活性,测得不同温度下反应4h时的转化率和选择性数据如图2(其它条件相同)。
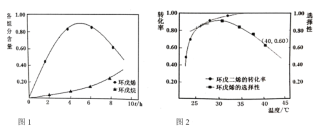
①环成二烯氢化制环成烯的最佳反应温度为__________,选择该温度的原因是__________。
②升高温度,环戊二烯转化率提高而环戊烯选择性降低,其原因是__________。
③在图1中画出40℃时环戊烯含量随t变化趋势的曲线。__________
(3)实际生产中,常由双环戊二烯通入水蒸气解聚成环戊二烯:

某温度,加入总压为70kPa的双环成二烯和水蒸气,达到平衡后总压为110kPa,双环戊二烯的转化率为80%,则该反应的平衡常数
__________(对于气相反应,用某组分B的平衡压强
代替物质的量浓度
也可表示平衡常数,记作
)。
高三化学综合题困难题查看答案及解析
-
I.固体A由四种元素组成的化合物,为探究固体A的组成,设计并完成如实验:
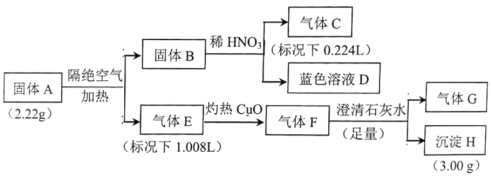
已知:固体B是一种单质,气体E、F都是G和另外一种气体组成。
请回答:
(1)组成A的四种元素是__________,气体E是__________。
(2)固体A隔绝空气加热分解的化学方程式是__________。
(3)蓝色溶液D和乙醇反应可获得固体A,同时还生成一种常见的温室气体,该反应的化学方程式为__________。
Ⅱ.某化学兴趣小组为探究SO2与
溶液的反应,用如下装置(夹持、加热仪器略)进行实验:制备SO2,将SO2通入
溶液中,迅速反应,得到无色酸性溶液和白色沉淀。
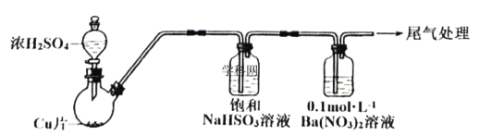
(1)SO2通入
溶液中,得到无色酸性溶液和白色沉淀的离子方程式是__________。
(2)若通入
溶液中的SO2已过量,请设计实验方案检验__________。
高三化学推断题困难题查看答案及解析
-
某固体X,可能含有BaCl2、NaHCO3、Fe2O3、Cu、NaAlO2中的一种或几种,进行如下实验:①取一定量样品溶于水中,得到固体A和溶液B;②向A中加入足量稀盐酸,得到澄清溶液C。下列说法不正确的是
A.固体A可能溶于NaOH溶液
B.溶液C能与NaHCO3溶液反应产生沉淀
C.向溶液C中加入KSCN溶液,若不变色,则混合物X不含Fe2O3
D.向溶液B中加入NaOH溶液,若出现白色沉淀,则X中必定有BaCl2和NaHCO3
高三化学推断题困难题查看答案及解析
-
室温下,用相同浓度的NaOH溶液分别滴定20.00mL浓度均为0.1mol·L-1的三种酸(HA、HB和HC)溶液,滴定的曲线如图所示,下列判断不正确的是
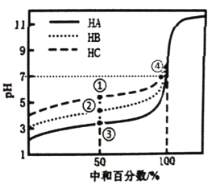
A.当中和百分数达50%时:
B.滴定至①点时,溶液中:
C.当中和百分数达100%时,消耗的NaOH溶液体积
D.①和④所示溶液中都有:
高三化学单选题困难题查看答案及解析
-
某温度下,HF和CH3COOH的电离常数分别为3.5×10-4和1.7×10-5。将pH和体积均相同的NaF和CH3COONa溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
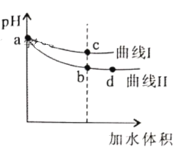
A.曲线I代表CH3COONa溶液
B.溶液中水的电离程度:c点>b点
C.从b点到d点,溶液中
保持不变(其中HA、
分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与HCl恰好反应后,溶液中
相同
高三化学单选题困难题查看答案及解析
-
莫沙朵林是一种镇痛药,它的合成路线如下:
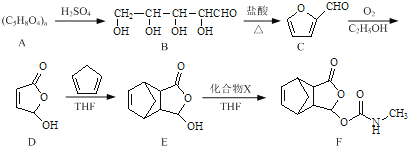
(1)B中手性碳原子数为____________;化合物D中含氧官能团的名称为____________。
(2)C与新制氢氧化铜反应的化学方程式为____________。
(3)写出同时满足下列条件的E的一种同分异构体的结构简式:____________
I.核磁共振氢谱有4个峰;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应.
(4)已知E+X→F为加成反应,化合物X的结构简式为____________。
(5)已知:
.化合物
是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以
和
为原料合成该化合物(用合成路线流程图表示,并注明反应条件).______________。
合成路线流程图示例如下:
 。
。高三化学填空题困难题查看答案及解析
-
合成氨反应是重要的化工反应,请回答下列问题:
(1)①NH3(g)+
O2(g)
NO2(g)+
H2O(g) △H=-299.6kJ·mol-1
②H2(g)+
O2(g)=H2O(g) △H=-241.8kJ·mol-1
③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1
由上述反应,可求出N2(g)+3H2(g)
2NH3(g)的△H=___。
(2)对于反应①,在恒温恒容(H2O为气态)的容器中,下列选项表明反应已达到平衡的是___。
A.混合气体的平均摩尔质量不变
B.混合气体的密度不变
C.气体的颜色不再变化
D.体系内压强不再变化
E.每消耗1molNH3的同时生成1molNO2
(3)已知:N2(g)+3H2(g)
2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应___(填“能”或“不能”)自发进行。
(4)如图为673K温度下,某合成氨塔里各气体组分压强变化图。
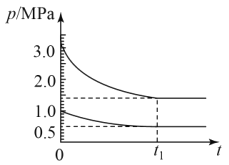
①t1平衡时,氨气的体积分数为___%(保留位小数)。
②在图中画出氨气组分压强变化图___。
③该温度下N2(g)+3H2(g)
2NH3(g)反应的压力平衡常数Kp=___(MPa)-2(保留1位小数,Kp为以气体分压表示反应的平衡常数)
高三化学综合题困难题查看答案及解析
-
废物利用有利于环境保护、资源节约,一种从废催化剂(含ZnO、CuO及少量石墨、Fe2O3及MnO2等)回收铜并制取活性氧化锌的工艺流程如图:
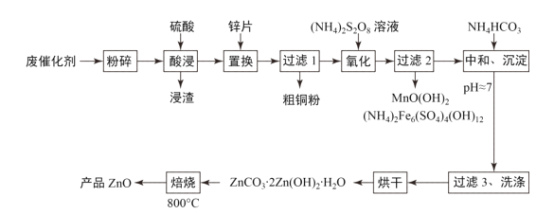
(1)为提高酸浸的速率,还可采取的措施为___。
(2)“氧化”时2molMn2+被氧化为MnO(OH)2,需要(NH4)2S2O8的物质的量为___。
(3)已知Zn(OH)2性质与Al(OH)3类似,在“中和、沉淀”时pH不能过大,请用文字结合离子方程式解释原因___。
(4)“过滤3、洗涤”时,对所得滤液蒸发浓缩、冷却结晶可得___(填主要物质的化学式)固体。
(5)“焙烧”过程中化学方程式为___。
(6)经测定,1kg废催化剂可得160g粗铜粉,又知粗铜粉中铜的质量分数为80%,则废催化剂中铜的质量分数为___%,若“酸浸”时硫酸浓度变小而又没有及时补充,则测定结果会比实际情况___(填“偏大”“偏小”或“无影响”)。
高三化学工业流程困难题查看答案及解析
-
碘酸钙[Ca(IO3)2]广泛用于食品工业、口腔洗涤,防腐等领域,某化学兴趣小组在实验室利用碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),溶液经氢氧化钾中和后,与氯化钙发生复分解反应制备碘酸钙,其制备步骤及装置(水浴加热装置略去)如图:
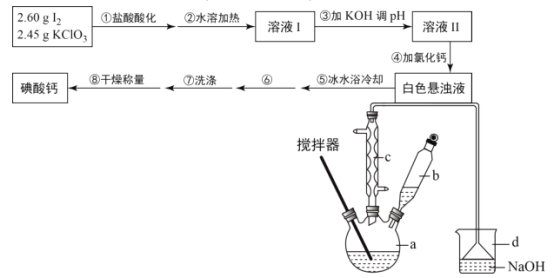
物质的摩尔质量如下表:
物质
I2
KClO3
Ca(IO3)2
摩尔质量/g·mol-1
354
122.5
390
请回答下列问题:
(1)加入b中盐酸后,碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),反应中有黄绿色的气体生成,该反应的化学方程式为___。
(2)步骤②与“直接加热”相比,“水浴加热”的优点为___。
(3)步骤④加入氯化钙后,得到白色悬浊液,说明KIO3的溶解度___(填“大于”“小于”或“等于”)Ca(IO3)2。
(4)步骤⑤冰水浴冷却的目的为___。
(5)步骤⑥的操作名称为___。
(6)步骤⑦洗涤后检验沉淀是否洗涤干净的方法为___。
(7)最终得到2..60g碘酸钙产品,则产率为___ %(保留2小数)。
高三化学实验题困难题查看答案及解析