某温度下,HF和CH3COOH的电离常数分别为3.5×10-4和1.7×10-5。将pH和体积均相同的NaF和CH3COONa溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
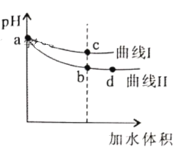
A.曲线I代表CH3COONa溶液
B.溶液中水的电离程度:c点>b点
C.从b点到d点,溶液中保持不变(其中HA、
分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与HCl恰好反应后,溶液中相同
高三化学单选题困难题
某温度下,HF和CH3COOH的电离常数分别为3.5×10-4和1.7×10-5。将pH和体积均相同的NaF和CH3COONa溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是

A.曲线I代表CH3COONa溶液
B.溶液中水的电离程度:c点>b点
C.从b点到d点,溶液中保持不变(其中HA、
分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与HCl恰好反应后,溶液中相同
高三化学单选题困难题
某温度下,HF和CH3COOH的电离常数分别为3.5×10-4和1.7×10-5。将pH和体积均相同的NaF和CH3COONa溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是

A.曲线I代表CH3COONa溶液
B.溶液中水的电离程度:c点>b点
C.从b点到d点,溶液中保持不变(其中HA、
分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与HCl恰好反应后,溶液中相同
高三化学单选题困难题查看答案及解析
保持在室温下,将pH和体积相同的这两种酸(HNO2和CH3COOH)分别加水稀释,其pH随加水体积的变化如下图所示。
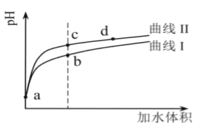
已知:在室温下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5,下列说法正确的是
A.曲线II代表的是CH3COOH溶液
B.溶液中水的电离程度:b点>c点>d点
C.体积相同的a点两溶液分别与NaOH溶液恰好中和时,两份溶液中:n()=n(Na+)=n(CH3COO-)
D.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
高三化学单选题中等难度题查看答案及解析
常温下CH3COOH 的电离常数为1.7×10-5,该温度下用0.1mol·L-1的醋酸溶液滴定10.00mL等物质的量浓度的碱ROH,滴定过程中加入醋酸的体积(V)与溶液中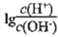 的关系如图所示。下列说法中正确的是
的关系如图所示。下列说法中正确的是
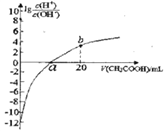
A. b点溶液显碱性
B. a>10.00
C. ROH 的电离方程式为ROHR++OH-
D. 25℃时,1mol·L-1的醋酸溶液中CH3COO-的浓度约为4.12×10-2mol·L-1(已知=4.12)
高三化学单选题困难题查看答案及解析
已知常温下CH3COOH和NH3·H2O的电离常数相等,向10ml浓度为0.1mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度始终增大
B.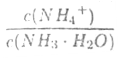 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10mL时c(NH4+)=c(CH3COO-)
高三化学选择题简单题查看答案及解析
25 ℃时,部分物质的电离常数如表所示:
| 化学式 | CH3COOH | H2CO3 |
| 电离常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 |
请回答下列问题:
(1)相同pH的CH3COONa、NaHCO3、Na2CO3浓度由大到小的顺序为__________
(2)常温下0.1mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填字母,下同)。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-) D.c(H+)/c(OH-)
(3)现有10mLpH=2的盐酸溶液,进行以下操作:
a.与pH=5的盐酸等体积混合,则pH=_____________;
b.向该盐酸溶液中加入10mL0.02mol/LCH3COONa溶液,则该混合溶液中存在的物料守恒式为__________________;
c.向该盐酸溶液中加入等体积等浓度的Na2CO3溶液,则混合溶液中存在的电荷守恒式为_______________________;
d. 下列关于体积都为10mL,pH=2的A(盐酸)和B(CH3COOH)溶液说法正确的是_____ (填写序号)。
①与等量的锌反应开始反应时的速率A=B
②与等量的锌反应(锌完全溶解,没有剩余)所需要的时间A>B
③加水稀释100倍,pH大小比较:4=A>B>2
④物质的量浓度大小比较:A>B
⑤分别与10mLpH=12的NaOH溶液充分反应后的溶液pH大小比较:A<B
e. 现用标准HCl溶液滴定氨水,应选用________指示剂,下列操作会导致测定结果偏高的是___。
A.未用HCl标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
高三化学综合题困难题查看答案及解析
下列说法正确的是( )
A.常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性
B.已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强
C.将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3·H2O)
D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)= c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6
高三化学选择题中等难度题查看答案及解析
常温下,CH3COOH与NH3•H2O的电离常数均为1.8×10-5。现向20mL浓度为0.1mol/LNH3•H2O的溶液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。
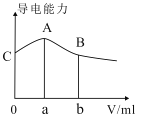
下列说法正确的是( )
A.a=20,A点溶液的pH=7
B.A、B两点中,B点溶液中水的电离程度最大
C.A点溶液中:c(CH3COO-)>c(NH4+)>c(H+)>c(OH-)
D.B、C两点中溶液的pH相等
高三化学单选题中等难度题查看答案及解析
25 ℃时,几种弱酸的电离平衡常数如下表所示。下列说法正确的是( )
| 化学式 | CH3COOH | H2CO3 | HCN |
| 电离平衡常数K | K=1.7×10–5 | K1=4.2×10–7 K2=5.6×10–11 | K=6.2×10–10 |
A.NaCN溶液中通入少量CO2的离子方程式为H2O+CO2+CN-=HCO3-+HCN
B.向稀醋酸溶液中加少量水,增大
C.等物质的量浓度的Na2CO3溶液pH比NaHCO3溶液小
D.等体积等物质的量浓度的NaCN溶液和HCN溶液混合后溶液呈酸性
高三化学单选题简单题查看答案及解析
已知HF比CH3COOH易电离。关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是 ( )
A.两溶液相比较,NaF溶液中的离子总数较多
B.在相同条件下,两溶液的pH大小为: CH3COONa< NaF
C.NaF溶液中:c(H+)+c(HF)= c(OH-)+ c(F-)
D.CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
高三化学选择题中等难度题查看答案及解析
在下列条件下,能大量共存的微粒组是
| 化学式 | CH3COOH | HClO | H2CO3 |
| 电离常数(25℃) | Ki =1.7×10-5 | Ki =3.0×10-8 | Ki1=4.3×10-7;Ki2=5.6×10-11 |
A.c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32-
B. 上表提供的数据下:HClO 、HCO3-、ClO-、CO32-
C.能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I-
D.中性的溶液中:CO32-、Na+、SO42-、AlO2-
高三化学选择题中等难度题查看答案及解析