-
可逆反应:aA(g)+ bB(g)
cC(g)+ dD(g);根据图回答:

(1)压强p1 _________p2(填“>”或“<”);
(2)a +b__________c +d(填“>”或“<”);
(3)温度t1℃_________t2℃(填“>”或“<”);
(4)正反应为_________反应。(填吸热或放热)
高三化学填空题简单题查看答案及解析
-
铝及其化合物在生产、生活中有极其广泛的用途。
(1)化学式Mg17Al12的合金是一种新型的纳米储氢合金,其储氢原来理为Mg17Al12+17H2=17MgH2+12Al,得到的混合物X(17MgH2+12Al)在一定条件下能释放出H2。
①MgH2中氢元素的化合价为____。
②将X与足量的NaOH溶液混合可得到H2,则766gX充分反应后可得到___molH2。
(2)将铝片放在汞盐溶液中,其表面会形成铝汞合金(铝表面的氧化膜被破坏了),从溶液中取出铝并放置在空气中,铝片表面会迅速长出胡须状的“白毛”(主要成分为Al2O3),同时放出大量的热.导致迅速长出“白毛”的原因可能有:一是铝、汞及介质共同形成了微小原电池,加速了铝的氧化反应;二是___。确定前一种可能原因是否存在的简单方法是___。
(3)无水AlCl3可用作有机合成的催化剂,工业上可用Al2O3、Cl2、焦炭混合反应制备无水AlCl3,该反应的另一种产物是可燃性气体,写出该反应的化学方程式:___。
(4)聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,它是应用广泛的高效净水剂。
①PAFC在强酸性和强碱性溶液中均会失去净水作用,原因是____。
②为检测PAFC中Al和Fe的含量,设计如图所示的流程:
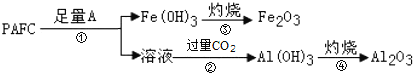
试剂A是____,步骤②中发生反应的离子方程式是____。
高三化学填空题简单题查看答案及解析
-
NH4Cl溶液呈酸性的原因是______(用离子反应方程式表示)。
高三化学填空题简单题查看答案及解析
-
今有常温下两种溶液:(A)0.1mol/L的NaCl溶液; (B) 0.1mol/LNH4Cl溶液。
①溶液(A)的pH____7(填“>”、“<”或“=”);
②溶液(B)呈_____性(填“酸”、“碱”或“中”),升高温度可以______(填“促进”或“抑制”)NH4Cl的水解。
高三化学填空题简单题查看答案及解析
-
锌银电池能量大、电压平稳,广泛用于电子手表、照相机、计算器和其他微型电子仪器。电解质溶液是KOH溶液,电池总反应为Zn+Ag2O═ZnO+2Ag,请回答下列问题:
①该电池的负极材料是______;电池工作时,阳离子向______(填“正极”或“负极”)移动;
②电极材料锌可由闪锌矿在空气中煅烧成氧化锌,然后用碳还原来制取,反应的化学方程式为ZnO+C
Zn+CO↑,此法为______。
A.电解法 B.热还原法 C.热分解法
高三化学填空题简单题查看答案及解析
-
已知:
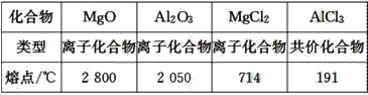
工业制镁时,电解MgCl2而不电解MgO的原因是__________________________________;
制铝时,电解Al2O3而不电解AlCl3的原因是________________________________________。
高三化学填空题简单题查看答案及解析
-
已知一定温度和压强下,在容积为VL的密闭容器中充入1 mol A和1 mol B,保持恒温恒压下反应:A(g)+B(g)
C(g) ΔH<0。达到平衡时,C的体积分数为40%。试回答有关问题:
(1)升温时,C的反应速率________(填“加快”“减慢”或“不变”)。
(2)若平衡时,保持容器容积不变,使容器内压强增大,则平衡________(填字母)。
A 一定向正反应方向移动 B 一定向逆反应方向移动
C 一定不移动 D 不一定移动
高三化学填空题简单题查看答案及解析
-
298K时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)
 2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4 kJ是______________________________________________。
高三化学填空题简单题查看答案及解析
-
太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。亚铜离子(Cu+)基态时的价电子排布式表示为________。
高三化学填空题简单题查看答案及解析
-
现有下列粒子:1H、2H、3H、1H+、234U、235U、238U、40K、40Ca、37Cl、14N、14C,请回答下列问题:
(1)它们分属_____种元素,属于氢元素的核素有_____种,属于铀元素的核素有_____种。互为同位素的原子分别为__________。
(2)质量数相等的粒子为_______、_______、_______。
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合成水,所得水分子的种数为__________;可得相对分子质量不同的水分子的种数为__________。
高三化学填空题简单题查看答案及解析