-
烯烃在金属卡宾催化下发生烯烃复分解反应,化学家将其形象地描述为“交换交谊舞舞伴”。其原理如下:C2H5CH=CHCH3+CH2=CH2
C2H5CH=CH2+CH2=CHCH3,2C2H5CH=CHCH3
C2H5CH=CHC2H5+ CH3CH=CHCH3。
以下是由烯烃A(C5H10)合称酯M和酯N的路线:
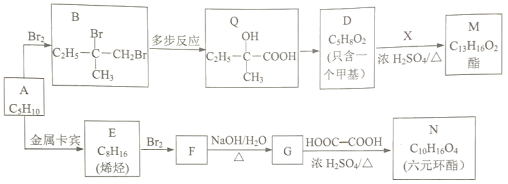
完成下列填空:
(1)Q中官能团的名称:_____________。Q→D的反应条件:________________。
(2)写出B→Q的合成路线(合成路线的表示方式为_______:
 )
)(3)E的结构简式为:______________。F→G的反应类型:__________反应。
(4)写出G→N的化学反应方程式_______________________________________________。
(5)有机物X的苯环只有一个侧链且不含甲基,写出X的结构简式:___________________。
(6)有机物Y是D的同分异构体,1mol Y与足量的新制氢氧化铜完全反应得到2mol沉淀,Y烷基上的一氯取代物只有一种,写出Y的结构简式_____________________________。
高三化学填空题困难题查看答案及解析
-
煤是重要能源。燃煤会释放SO2、CO等有毒气体。消除有毒气体的研究和实践从未停止。完成下列填空:
I.用CaSO4消除CO。CaSO4和CO可发生如下两个反应:
反应①:CaSO4(s)+4CO(g)
CaS(s)+4CO2(g)+175.6kJ
反应②:CaSO4(s)+4CO(g)
CaO(s)+SO2(g)+CO2(g)—218.4kJ
(1)写出反应①的平衡常数表达式:_____________;一定条件下的密闭容器中,两反应均达平衡后,若使反应①K的减小,需要改变的反应条件是______________,则反应②的K___________(选填编号)、反应①的v(CO2)正__________(选填编号)。
a. 增大 b. 减小 c. 不变 d. 无法判断
(2)补全下图中反应②的能量变化示意图_______________(即,注明生成物能量的大致位置及反应热效应数值)

(3)下图是不同温度下,CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。写出两种降低SO2生成量的措施___________________________________。

II. Fe2(SO4)3溶液可除去煤中以黄铁矿(FeS2)形式存在的硫元素,反应如下:8H2O + FeS2+ 7Fe2(SO4)3→15FeSO4+ 8H2SO4
(4)标出电子转移的数目和方向________;还原产物是_______。
(5)检验上述反应中Fe2(SO4)3是否消耗完的实验方案:___________________________。
(6)该方法的优点之一是Fe2(SO4)3易再生。向反应后的溶液中通入___________,就能达到使Fe2(SO4)3再生的目的,方便且价廉。
高三化学填空题困难题查看答案及解析
-
因在航空、核能、电池等高技术领域的重要作用——锂被称为“21世纪的能源金属”。完成下列填空:
(1)锂位于元素周期表的________。锂的很多化学性质与镁相似,请依据元素周期律进行解释:_________。
(2)氢化锂(LiH)是离子化合物,写出其阴离子的电子式_______________,LiH中阴离子半径大于阳离子半径,其原因是__________________________________________________。
(3) 工业上用Li2CO3制取锂的化合物及金属锂。碳原子核外电子有________种不同能量的电子,其中有两个电子的能量最高且能量相等,这两个电子所处的轨道是_____________________。
(4)用Li2CO3、氨水和液溴制备LiBr·H2O的流程如下:

①合成时,除生成LiBr外,还产生了两种参与大气循环的气体,补全产物并配平该反应的化学方程式:
Li2CO3+Br2+ NH3·H2O→LiBr+(___) __________。
②溴化锂的溶解度随温度变化曲线如图所示,请补全从溶液中得到LiBr·H2O晶体的实验步骤:_____、过滤、用乙醇洗涤,干燥。

高三化学填空题困难题查看答案及解析
-
知识的梳理和感悟是有效学习的方法之一。某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问题(显示的电极均为石墨)。
(1)图中,电解一段时间后,气球b中的气体是________(填化学式),U形管________(填“左”或“右”)边的溶液变红。
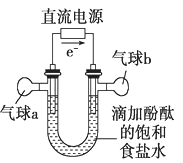
(2)利用图制作一种环保型消毒液发生器,可制备“84”消毒液的有效成分,则c为电源的________极;该发生器中反应的总离子方程式为_______________________________。
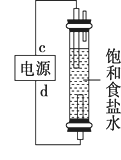
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。该工艺的相关物质运输与转化关系如图所示(其中的电极未标出,所用的离子膜都只允许阳离子通过)。

①燃料电池B中的电极反应式分别为
负极:_______________________________________________________,
正极:_______________________________________________________。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为________。
高三化学填空题困难题查看答案及解析
-
(18分)某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图的反应关系,写出下列B、C、D、E所含物质的化学式
固体B ;沉淀C ;沉淀D ;溶液E 。
(3)写出①、②、③、④四个反应的化学方程式
① ;② ;③ ;④
高三化学填空题中等难度题查看答案及解析
-
二乙酸
环己二醇酯可通过下列路线合成:
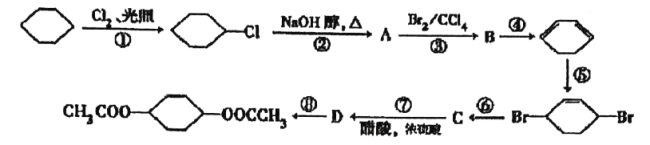
(1)属于取代反应的是______,属于加成反应的是______(填序号).
(2)A的结构简式为______.
(3)写出反应④、⑦的化学方程式:______、______.
高三化学填空题中等难度题查看答案及解析
-
已知固体甲为非金属,I、F均为常见的金属,E为气体单质;固体乙为一种红棕色固体;G为白色胶状沉淀,既能溶解于盐酸,又能溶解于氢氧化钠溶液.A在常温下为气态,与氧气完全反应时的体积比是
.W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为
.各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题:
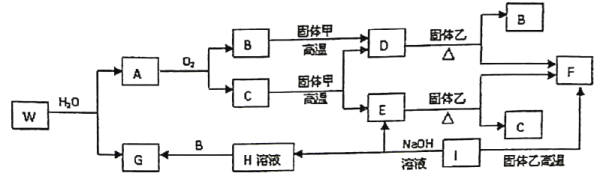
(1)B的电子式为______,固体甲、乙的化学式分别是______、______;
(2)上述转化中,①
②
③
④
⑤
⑥
其中属于置换反应的是(填序号)______;
(3)写出W和水反应的化学方程式______,
和
溶液反应的离子方程式______.
高三化学填空题中等难度题查看答案及解析
-
二氯化二硫(
)可用作橡胶的低温硫化剂和粘结剂,在工业上具有重要的应用.某实验室研究小组通过查阅硫与氯气反应的相关资料,得知:
,纯净的氯气在110~140℃时可以与硫反应得到淡红色的
粗产品.
有关物质的部分性质如下表:
物质
外观(常温下)
熔点/℃
沸点/℃
化学性质
淡黄色固体
112.8
444.6
淡黄色液体
135.6
①遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体
②能与
反应生成
③温度过高易分解,300℃以上完全分解
红色液体
—
59.6℃发生完全分解,分解产物为
与
现在需要利用如下仪器和药品制取纯净的氯气,并且进一步与硫反应来制备
.
提供的仪器:
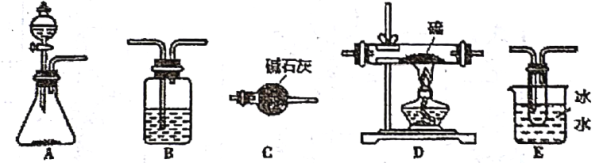
提供的药品:
浓盐酸、浓
、
、
、饱和
溶液、碱石灰、硫磺、
溶液、冰水、饱和食盐水.
(1)现需要使用装置A来制备氯气,写出制备
的离子方程式:______
(2)利用所提供的仪器组合实验装置,写出相应的连接顺序(仪器B可使用2次)______;第二次装置B中的药品是______;
(3)
分子中各原子均达到8电子稳定结构,写出其电子式_______;
遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体,写出相关化学方程式:______.
(4)装置C的作用是______.
(5)实验过程中需要控制装置D的加热温度,并且需要控制好
的通入量,原因是?______.
(6)装置E中收集到的粗产品
呈淡红色,如何进一步提纯?______.
高三化学填空题中等难度题查看答案及解析
-
2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
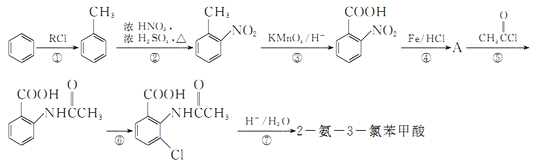
已知:

回答下列相关问题(1)
的名称是__________,2-氨-3-氯苯甲酸中含N官能团的电子式为__________。
(2)反应①中R代表的是_____________,反应②的反应类型为_____________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式_____________。
(4)A的结构简式为_____________,⑥的反应条件为_____________。
(5)符合下列条件的同分异构体的结构简式为_____________。
a.式量比
大42的苯的同系物;
b.与酸性KMnO4反应能生成二元羧酸
c.仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
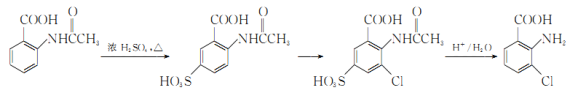
分析产率提高的原因是_____________。
高三化学填空题困难题查看答案及解析
-
碘化亚铜(CuⅠ)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水碘化亚铜的流程。
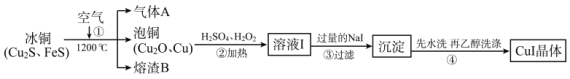
(1)FeS中S的化合价为_____________。
(2)步骤①中Cu2S被转化为Cu,同时有大气污染物A生成,相关化学反应方程式为_____________,熔渣B的主要成分为黑色磁性物质,其化学式为_____________。
(3)步骤②中H2O2的作用是_____________;步骤③中加入过量NaI涉及的主要离子反应方程式为_____________。
(4)步骤④用乙醇洗涤的优点是_____________;检验沉淀是否洗涤干净的方法是_____________。
(5)溶液I中通常含少量Fe(Ⅲ)。已知该工业条件下,Fe(OH)3的Ksp=1.0×10-38,据此分析除去Fe(Ⅲ)(即c(Fe3+)≤1.0×10-5mol/L)应调节pH不小于_____________(水的离子积以常温计)。
(6)准确称取 m g CuI样品,加入足量的Fe2(SO4)3溶液,发生反应为2CuⅠ+4Fe3+===2Cu2++4Fe2++I2,待样品完全反应后,用amol/L酸性KMnO4溶液滴定Fe(Ⅱ),消耗标准液的体积平均值为ⅴmL。样品中CuI的质量分数的计算表达式为_____________;如果滴定前,酸式滴定管没有用标准液润洗,CuI的质量分数_____________(填“偏低”、“偏高”或“无影响”)。
高三化学填空题困难题查看答案及解析