-
(本题共12分)乙酸正丁酯常用作香精,实验室用冰醋酸和正丁醇制备乙酸正丁酯
Ⅰ.乙酸正丁酯粗产品的制备
试管中加少许入沸石、7.4 mL正丁醇和6.4 mL冰醋酸,再加入3~4滴浓硫酸,然后安装好装置,加热使之反应。
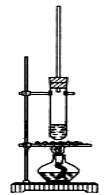
Ⅱ.乙酸正丁酯粗产品的精制
将试管中的液体转移到分液漏斗中,用10 mL水洗涤,除去下层水层;有机层继续用10 mL 10% Na2CO3洗涤至中性;再用10 mL 的水洗涤。
将酯层进行蒸馏。蒸馏收集乙酸正丁酯产品时,应将温度控制在126.1℃左右。
Ⅲ.计算产率
称量出制得的乙酸正丁酯的质量为5. 12 g。
已知:
物质
密度/g·cm-3
沸点/℃
溶解度/100g水
正丁醇
0.810
118.0
9
冰醋酸
1.049
118.1
互溶
乙酸正丁酯
0.882
126.1
0.7
完成下列填空:
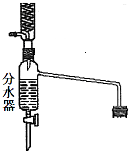
(1)上图装置中长导管有冷凝回流作用,它可以由分水回流装置代替。分水回流装置中回流下来的蒸气冷凝液进入分水器,待分层后,有机层会自动流回到反应器中,将生成的水从分水器中放出去。
分水回流代替长导管回流,对乙酸正丁酯的合成有什么作用 。
使用分水器装置进行回流的可逆反应,一般应具备 条件。
(2)分水器在使用时须预先加水,使其水面低于分水器回流支管下沿3~5 mm的水。
预先加水的目的是 。
(3)反应时加热有利于 提高酯的产率,但温度过高时酯的产率反而降低,
其可能的原因是 。
(4)水洗的目的是 。碱洗的目的是 。
测pH值的操作 。
(5)本次实验乙酸正丁酯的产率 。
高三化学实验题困难题查看答案及解析
-
(本题共12分)工业烧碱成分NaOH、Na2CO3和可溶于水但不与酸反应的杂质,工业纯碱成分Na2CO3、NaHCO3和可溶于水但不与酸碱反应的杂质。为测定碱中各成分的百分含量可采用滴定法、气体法等。
完成下列填空:
(1)滴定法测定工业烧碱样品:配制250mL待测液,所用的主要仪器有烧杯、量筒、胶头滴管、玻璃棒、 。
(2)测定工业烧碱的总碱量n Na2O(或总耗酸量):进行滴定时,先向盛待测液的锥形瓶中加 作为指示剂。
判断滴定终点的现象是 。
(3)气体法测定工业烧碱的Na2CO3含量(如图):

装置中B部分盛放的试液是 。
装置中A部分的分液漏斗与烧瓶之间连接的导管所起的作用是 。
(4)用中和滴定的氯化钡法测定工业烧碱中NaOH的含量时,可先在混合液中滴加过量的BaCl2溶液,再以酚酞作指示剂,然后用标准盐酸滴定。
滴加过量的BaCl2溶液目的是 。
向混有碳酸钡沉淀的氢氧化钠溶液中滴入盐酸,为什么不会使碳酸钡溶解而能测定氢氧化钠的含量 。
(5)用中和滴定的氯化钡法测定工业纯碱中NaHCO3的含量时,使用与测定烧碱相同的实验操作,过程稍作改变即可。
简述该操作过程 。
高三化学实验题困难题查看答案及解析
-
硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如下图所示:

已知:①SO2(g)+Cl2(g)
SO2Cl2(l)△H= -97.3kJ•mol-1
②硫酰氯常温下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中易“发烟”;
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是_____________________。
(2)仪器b的名称为____________,干燥管中碱石灰的主要作用是___________________。
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为______________。当装置E中排出氯气1.12L(已折算成标准状况)时,最终得到5.4g纯净的硫酰氯,则硫酰氯的产率为_____。长期存放的硫酰氯会发黄,其原因可能为_________________。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_________,分离这两种液态产物的方法是_____________。
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应。__________________(简要描述实验步骤、现象和结论)。
高三化学实验题困难题查看答案及解析
-
aF是一种重要的氟盐,主要用作农作物杀虫剂、木材防腐剂等。某课题组设计了以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵的实验,其工艺流程如下:

已知:20 ℃时氯化铵的溶解度为37.2 g,氟化钠的溶解度为4 g,Na2SiF6微溶于水。
(1)操作Ⅱ是洗涤、干燥,其目的是 ,
操作Ⅲ和操作Ⅳ的名称依次是 (填写序号)。
a.过滤 b.加热蒸发 c.冷却结晶 d.洗涤
(2)上述流程中①的化学反应方程式:
H2SiF6+ NH4HCO3
NH4F+ H2SiO3↓+ CO2↑+ ________
(3)流程①中NH4HCO3必须过量,其原因是 。
(4)若不考虑氟化钠的溶解,7.2 g氟硅酸理论上最多能生产 g氟化钠。
高三化学实验题困难题查看答案及解析
-
2-苯基-2-丁醇是重要的有机合成中间体,以溴苯为原料合成该中间体的反应原理如下:
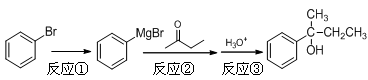
【实验装置】


装置Ⅰ 装置Ⅱ
【实验步骤】
步骤1:将镁条置于装置Ⅰ的三颈烧瓶中,加入100 mL乙醚(ρ=0.71g·cm-3),在冷却条件下缓缓滴入溴苯,微热并加入一小块碘引发反应①。
步骤2:滴加14.2 mL丁酮和30 mL乙醚混合物,发生反应②;滴加入20%的NH4Cl水溶液,发生反应③。
步骤3:分出油层,用水洗涤至中性,用无水CaCl2干燥。
步骤4:用装置Ⅱ先蒸出乙醚,再蒸馏出产品。
⑴步骤1中加入碘的作用是 。
⑵装置Ⅰ中滴加液体所用的仪器的名称是 ,反应②需将三颈烧瓶置于冰水中,且逐滴加入丁酮和乙醚,其目的是 。
⑶步骤三中分离出油层的具体实验操作是 。
⑷装置Ⅱ采用的是减压蒸馏,实验时需将吸滤瓶需连接 ;采用这种蒸馏方式的原因是 。
高三化学实验题困难题查看答案及解析
-
某化学兴趣小组拟用右图装置制备氢氧化亚铁并观察其颜色。提供化学药品:铁屑、稀硫酸、氢氧化钠溶液。
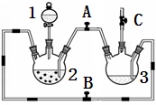
(1)稀硫酸应放在 中(填写仪器名称)。
(2)本实验通过控制A、B、C三个开关,将仪器中的空气排尽后,再关闭开关 、打开开关 就可观察到氢氧化亚铁的颜色为 。试分析实验开始时排尽装置中空气的理由 。
(3)实验时为防止仪器2中铁粉通过导管进入仪器3中,可采取的措施是 。
(4)在FeSO4溶液中加入(NH4)2SO4固体可制备摩尔盐晶体[(NH4)2SO4·FeSO4·6H2O] (相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是 。
A.用冷水洗
B.先用冷水洗,后用无水乙醇洗
C.用30%的乙醇溶液洗
D.用90%的乙醇溶液洗
②为了测定产品的纯度,称取a g产品溶于水,配制成500mL溶液,用浓度为c mol·L-1的酸性KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
实验次数
第一次
第二次
第三次
消耗高锰酸钾溶液体积/mL
25.52
25.02
24.98
滴定过程中发生反应的离子方程式为 。滴定终点的现象是 。
通过实验数据计算的该产品纯度为 (用字母ac表示).上表中第一次实验中记录数据明显大于后两次,其原因可能是 。
A.实验结束时俯视刻度线读取滴定终点时酸性高锰酸钾溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
D.该酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
高三化学实验题困难题查看答案及解析
-
(15分)
某化学研究小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,在实验室中按以下步骤进行实验:
①称取a g样品,置于烧杯中;
②取适量盐酸和适量蒸馏水使样品溶解,准确配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色,冷却至室温后,称量;
⑦……
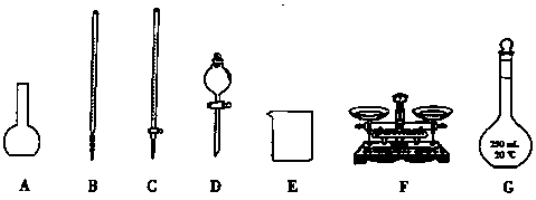
请根据上面的叙述回答下列问题:
(1)装置D的名称是 ,上图所给仪器中,实验步骤①②③中必须用到的仪器是E和_______ (填仪器序号)。
(2)步骤③中所发生反应的离子方程式为 ,
(3)步骤④中检验沉淀是否完全的操作是
步骤⑤中洗涤沉淀的操作是:________________________________
(4)检验沉淀是否洗净的操作是取最后一次洗涤液,加入几滴______ (填写序号)。
①KSCN溶液 ②NaOH溶液 ③AgNO3溶液 ④酚酞试液
(5)若坩埚质量是W1 g,最终坩埚和固体的总质量是W2 g,则样品中铁元素的质量分数为_______。
高三化学实验题困难题查看答案及解析
-
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和
,并含有3.5%(质量分数)
.
(1)
元素在周期表中位置是________,其原子结构示意图________.
(2)
与最活跃的非金属元素A形成化合物D,D的电子式为________,D的沸点比A与
形成的化合物E的沸点________.
(3)配平用钙线氧脱鳞的化学方程式:
________P+________FeO+ ________CaO
+ ________Fe
(4)将钙线试样溶于稀盐酸后,加入过量
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色
.则金属M为______;检测
的方法是_____(用离子方程式表达).
(5)取1.6g钙线试样,与水充分反映,生成224ml.
(标准状况),在想溶液中通入适量的
,最多能得到
g.
高三化学实验题困难题查看答案及解析
-
醋酸亚铬,通常以二水盐[Cr(CH3COO)2]2·2H2O的形式存在,是深红色晶体,潮湿时易被氧化。不溶于冷水,微溶于乙醇。醋酸亚铬的一种实验室制备装置和实验步骤如下:

易被氧化。不W 于冷水,微游于乙M。
①连接装置,检查装置气密性,加入药品
②__________________________,A中反应液变浅蓝色后,停止滴入盐酸,向C中通入N2
③打开a,关闭b,保持通入N2,再次滴入盐酸
④待C中有大量红色晶体析出,停止滴入盐酸
⑤取C中物质,抽滤,依次用水、乙醇洗涤沉淀,干燥,称重
回答下列问题:
(1)装置A的名称为_______________,导管c的作用是________________________。
(2)补充步骤②中的实验操作__________________________________。
(3)步骤②中Zn与K2Cr2O7反应的离子方程式为____________________________________。
(4)步骤③中出现的现象是______________________,保持通入N2的目的是______________________。
(5)洗涤时依次用水、乙醇,目的依次为___________________________________。
(6)铬离子会污染水,常温下处理上述实验中多余Cr2+时,可向溶液中通入足量的___________(填物质名称或化学式)再加入碱调节pH为6,此时溶液中残留的Cr3+浓度为__________mol/L。已知:Ksp[Cr(OH)3] =6.3×10-31
高三化学实验题困难题查看答案及解析
-
(本题共12分)下图是实验室制备1,2—二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略)。

有关数据列表如下:

请完成下列填空:
36.A中药品为1:3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:__________________。
37.气体发生装置使用连通滴液漏斗的原因_________________________________________。
38.请写出C装置中的离子反应方程式_______________________________________。
39.装置D中品红溶液的作用是__________________________________;
40.反应过程中应用冷水冷却装置E,其主要目的是___________________________;但又不能过度冷却(如用冰水),其原因是___________________________________________。
41.学生发现反应结束时,无水乙醇消耗量大大超过理论值,其原因是___________________。
42.有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,判断改用四氯化碳液体是否可行______(填“是”或“否”),其原因是__________________________。
高三化学实验题困难题查看答案及解析