-
铁及其化合物在生产生活中应用广泛,如铁红(Fe2O3)可作为颜料,电子工业常用一定浓度的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板。 aFe2(SO4) 3·b(NH4) 2SO4·cH2O,(硫酸铁铵)常用于生活饮用水、工业循环水的净化处理。
(1)现有一含有Fe2O3和Fe3O4的混合物样品,测得n(Fe):n(O)=1:1.375,则该样品中Fe2O3的物质的量分数为___________。(结果保留2位有效数字)
(2)CuO和Fe2O3的混合物9.6 g在高温下与足量的CO充分反应,反应后全部气体用100mL 1.2mol/L Ba(OH)2 溶液吸收,生成15.76 g白色沉淀。则吸收气体后溶液中的溶质的化学式为__________,混合物中CuO和Fe2O3的物质的量之比为___________。
(3)称取某硫酸铁铵样品7.00 g,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到1.07 g沉淀;向另一份溶液中加入含0.025 molBa (NO3)2的溶液,恰好完全反应,求该硫酸铁铵的化学式_________。
(4)现将一块敷有铜箔的绝缘板浸入800mL 3mol/L的FeCl3溶液中,一段时间后,将该线路板取出,向溶液中加入铁粉56.0 g,充分反应后剩余固体51.2 g,求所得溶液中溶质的物质的量浓度_________(忽略反应前后溶液体积的变化)。
高三化学计算题中等难度题查看答案及解析
-
镁及其化合物在工业上有广泛的应用。
完成下列计算:
(1)称取某镁铝合金10g,放入100mL3mol/L的NaOH溶液中,完全反应收集到6.72L的H2(标准状况)。该合金中镁的质量分数为___。
(2)将镁条在空气中燃烧后的产物溶解在50mL1.6mol/L的盐酸中恰好完全反应,再加入过量NaOH把NH3全部蒸发出来,经测定NH3为0.102g,则镁条在空气中燃烧的产物及质量为___。
(3)Mg(HCO3)2溶液加热分解,得到产品轻质碳酸镁。18.2g轻质碳酸镁样品经高温完全分解后得8.0g氧化镁固体,放出3.36L二氧化碳(标准状况),求轻质碳酸镁的化学式___。
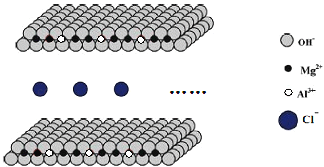
(4)氯离子插层的镁铝水滑石(Mg-Al-ClLDHs)是一种新型的阴离子交换材料。其结构示意图如图所示(每一层可视作平面无限延伸结构)。该离子交换原理是将插层离子与其它阴离子进行等电荷交换。取镁铝水滑石10.66g与0.02molNa2CO3发生完全交换,产物在高温下完全分解,得到金属氧化物和气体。将金属氧化物加入稀硝酸完全溶解后,再加入NaOH溶液直至过量,最终得到4.64g白色沉淀。求Mg-Al-ClLDHs的化学式___。
高三化学计算题困难题查看答案及解析
-
有三份不同质量的硫化铜与硫化亚铜的混合物样品①②③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中硫化铜的量。
(1)甲取2.56克样品①,置于空气中加强热,产物为氧化铜和二氧化硫。若产生0.448 L气体(标准状况),该气体被30 mL一定浓度氢氧化钠恰好完全吸收,将所得溶液小心低温蒸干得固体2.3克。则样品①中硫化铜的质量为_____g,氢氧化钠浓度_______mol·L-1;
(2)乙取3.52克样品②,投入过量的浓硝酸中加热,充分反应后,样品全部参与反应,溶液失重8.44克。样品②中硫化铜的物质的量为____mol;若浓硝酸的浓度为14.2 mol·L-1,则反应消耗浓硝酸____mL。(已知:Cu2S+14HNO3→2Cu(NO3)2+10NO2↑+H2SO4+6H2O)
(3)丙称量样品③强热后剩余的固体质量比原样品减小了a g,若该固体为氧化铜,则样品③中硫化铜物质的量(n)为_________mol。若要计算硫化亚铜的质量,则缺少_____________数据,若设该数据为b克,则硫化亚铜的质量为___________。
高三化学计算题中等难度题查看答案及解析
-
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠________ g。
(2)钠—钾合金可在核反应堆中用作热交换液。5.05 g钠—钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。________
②计算并确定该钠-钾合金的化学式。______________
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2―→2Al(OH)3↓+Na2CO3+H2O,己知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112 L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。_____________
高三化学计算题困难题查看答案及解析
-
碳酸氢纳俗称“小苏打”,是氨碱法和联合制碱法制纯碱的中间产物,可用作膨松剂,制酸剂,灭火剂等。工业上用纯碱溶液碳酸化制取碳酸氢钠。
(1)某碳酸氢钠样品中含有少量氯化钠。称取该样品,用0.1000mol/L盐酸滴定,耗用盐酸20.00mL。若改用0.05618mol/L硫酸滴定,需用硫酸____________mL(保留两位小数)。
(2)某溶液组成如表一:
化合物
Na2CO3
NaHCO3
NaCl
质量(kg)
814.8
400.3
97.3
问该溶液通入二氧化碳,析出碳酸氢钠晶体。取出晶体后溶液组成如表二:
化合物
Na2CO3
NaHCO3
NaCl
质量(kg)
137.7
428.8
97.3
计算析出的碳酸氢钠晶体的质量(保留1位小数)。____________
(3)将组成如表二的溶液加热,使碳酸氢钠部分分解,溶液中NaHCO3的质量由428.8kg降为400.3kg,补加适量碳酸钠,使溶液组成回到表一状态。计算补加的碳酸钠质量(保留1位小数)。____________
(4)某种由碳酸钠和碳酸氢钠组成的晶体452kg溶于水,然后通入二氧化碳,吸收二氧化碳44.8×103L(标准状况),获得纯的碳酸氢钠溶液,测得溶液中含碳酸氢钠504kg。通过计算确定该晶体的化学式____________
高三化学计算题中等难度题查看答案及解析
-
硝酸的工业制备包括氨的合成、氨的催化氧化及硝酸的浓缩等过程.完成下列计算:
(1)采用甲烷的二次转化法可以制备氢气.
第一次转化的化学方程式:CH4+H2O→CO+3H2;
第二次转化的化学方程式:2CO+CH4+2O2→3CO2+2H2;2CO+O2→2CO2.
现有标准状况下1m3的甲烷,若第一次转化80%,第二次转化20%,经过二次完全转化后可以得到H2__mol.
(2)用饱和K2CO3溶液吸收上述混合气体中的CO2以得到纯净的氢气.处理上述的CO2至少需要饱和K2CO3溶液____g.(已知:20℃K2CO3溶解度:110g/100g水)
(3)已知NH3+2O2→HNO3+H2O.现有氨气1.7吨,不补充水,理论上可制得硝酸的浓度为___%;在该硝酸中加入__吨水最终可得50%的硝酸.
(4)工业上常用98%的浓H2SO4作为制取浓HNO3的脱水剂.63.5%HNO3(质量为M1)中加98%的浓H2SO4(质量为M2)后蒸馏.分别得到97.7%的HNO3和49%的H2SO4溶液(不含HNO3).
①若蒸馏过程中HNO3、H2SO4、H2O均无损耗,求蒸馏前的投料比
的值__(列式计算).
②蒸馏过程中,若H2O的损耗占总质量的5.0%,即有(M1+M2)×5.0%的H2O流失.则投料时,
比值如何变化,请列式计算说明__.
高三化学计算题困难题查看答案及解析
-
我国是镁资源最为丰富的国家之一.
(1)将1mol镁铝合金(Mg17Al12)完全溶解于12L 6mol/L的盐酸中,放出氢气______mol,为使反应后溶液中的Mg2+、Al3+完全沉淀,需加入10mol/L的氨水至少______L。
(2)灼烧碱式碳酸镁可得到MgO.取碱式碳酸镁4.66g,灼烧至恒重,得到2g固体和1.76g CO2,某学生为确定碱式碳酸镁的化学式列了以下联立方程:
24+17x+60y+18z=4.66÷(
)…①
2﹣x﹣2y=0…②
(
)×(0.5x+z)×18=4.66﹣2﹣1.76…③
(a)①式表达的是求算碱式碳酸镁摩尔质量的关系式,则②式表达的是_______________;
(b)以上关系式是正确的,据此可求出该碱式碳酸镁的化学式为________________________________。
(3)氧化镁可用于烟气脱硫,反应原理为:
MgO+H2O=Mg(OH)2 Mg(OH)2+SO2=MgSO3+H2O
MgSO3+H2O+SO2=Mg(HSO3)2 2MgSO3+O2=2MgSO4
某小组模拟脱硫过程如下(实验在25℃进行):将MgO加入水中,不断搅拌,通入SO2和空气,得到550g滤液和若干克滤渣.取55g滤液依次加入足量的盐酸和BaCl2溶液,得到0.897g白色沉淀;另取55g滤液加入足量氯水和BaCl2混合溶液,得到1.992g白色沉淀.分析知滤渣中含MgSO3 16.82g(其它成分不含硫元素)。
①该实验过程中吸收的SO2的物质的量为________mol;消耗氧气的物质的量为_______mol。
②Mg(HSO3)2易溶于水;25℃溶解度,MgSO4:33.7g/100g水;MgSO3:0.652g/100g水.试通过计算确定550g滤液中镁盐的成分及物质的量(写出计算过程)___________________________。
高三化学计算题中等难度题查看答案及解析
-
硫酸是一种重要的化工原料。接触法生产的硫酸产品有98%的硫酸、20%的发烟硫酸(H2SO4和SO3的混合物,其中SO3的质量分数为0.2)。
完成下列计算:
(1)若不计生产过程的损耗,__________m3 SO2(折合成标准状况)经充分转化、吸收,可产出1吨 98%的硫酸(密度为1.84g/mL)。若98%的硫酸可表示为SO3•
H2O,20%的发烟硫酸可表示为SO3•aH2O,则a的值为 ___________(用分数表示)。
(2)铝和铝的化合物在社会生产和人类生活中也有着重要的作用。现有甲、乙两瓶无色溶液,已知它们可能是Na[Al(OH)4]溶液和H2SO4溶液。现经实验获得如下数据:
(已知:2Na[Al(OH)4]+H2SO4→2Al(OH)3↓+Na2SO4+2H2O)
组别
甲(mL)
乙(mL)
沉淀的物质的量(mol)
①
140
10
0.02
②
10
140
0.02
③
20
560
0.04
请通过必要的计算推断过程回答:乙溶液中的溶质是什么________?其物质的量浓度为多少________?
高三化学计算题困难题查看答案及解析
-
有三种镁铝合金样品(组分比例不一定相同)①、②、③。小奉、小贤、小红三同学各取一种样品,对合金中镁的质量分数进行下列实验探究:
(1)小奉取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则合金中镁的质量分数为___________。(保留小数点后面2位)
(2)小贤取样品②m2 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为VL,则m2的取值范围是_________。(结果转化为最简分数)
(3)小红取不同质量的样品③分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体的体积(标准状况下测定)如下所示:
实验序号
a
b
c
合金质量(g)
0.51
0.765
0.918
气体体积(mL)
560
672
672
求:I.盐酸的物质的量浓度_______
II.合金中镁的质量分数_______
III.要使c组实验后剩余合金中的铝恰好完全溶解,还需向容器中加入1.0 mol/L的氢氧化钠溶液多少mL_______?
高三化学计算题中等难度题查看答案及解析
-
I.中国科学家制得一种蓝色钨的氧化物(WOa ),其中钨的质量分数为 0.7985。
(1)a=______(保留2位小数)。
(2)WOa中存在五价和六价两种价态的钨。则蓝色钨的氧化物中这两种价态的钨原子数之比为________。
II.将铁锰的钨酸盐[(Fe,Mn)WO4]碱熔,发生如下反应(设空气中N2、O2的体积分数分别为0.8和0.2):
4FeWO4+4 Na2CO3+ O2
4 Na2WO4+ 2Fe2O3+ 4CO2 ①
2MnWO4+2Na2CO3+ O2
2 Na2WO4+ 2MnO2+ 2CO2 ②
(1)根据反应①,若反应前空气为100L,反应后气体为160L(气体体积在同温同压下测定),则反应后所得气体中CO2的体积分数为_________。
(2)某工厂投料550 mol Na2CO3制备Na2WO4,每反应1mol O2时,气体就增加1.5mol,则生成物中Fe2O3与MnO2的物质的量之比为_________;若反应后气体增加300 mol,制得Na2WO4_____mol。
III.由Na2WO4制备W的第一步反应为:Na2WO4+2HCl→H2WO4↓+2NaCl。往1L密度为1.190g /cm3的37%的浓盐酸加入6.030 mol Na2WO4,恰好完全反应。将产生的沉淀过滤后,溶液中溶质只有NaCl,求该溶液中NaCl的质量分数(25℃时NaCl的溶解度为36.0 g/100 g水)______________
高三化学计算题中等难度题查看答案及解析