-
有机物X(
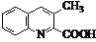 )是重要的化工试剂,一种合成路线如下:
)是重要的化工试剂,一种合成路线如下: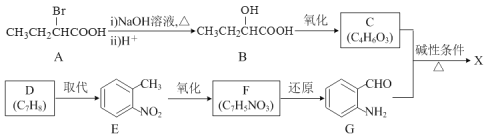
已知:①RNH2+
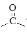

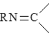 +H2O
+H2O②
 +H2O
+H2O(1)D→E的反应试剂及条件是_____。
(2)F的结构简式为_____。
(3)一定条件下,HCHO与
 以等物质的量发生反应。可能生成的所有有机产物的结构简式有___。
以等物质的量发生反应。可能生成的所有有机产物的结构简式有___。(4)有机物X的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:__。
①除苯环外无其他环状结构;
②能发生银镜反应,能与酸反应生成盐;
③核磁共振氢谱图中有4个峰。
高一化学原理综合题困难题查看答案及解析
-
下列实验原理和装置能达到实验目的的是
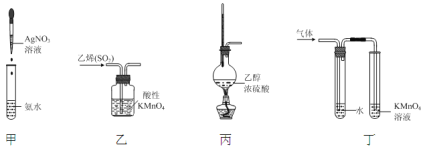
A.装置甲:制取银氨溶液 B.装置乙:除去乙烯中混有的SO2
C.装置丙:制取乙烯 D.装置丁:验证溴乙烷在氢氧化钠醇溶液加热条件下发生了消去反应
高一化学单选题困难题查看答案及解析
-
在一定条件下,将H2和N2置于一容积为2L的密闭容器中发生反应,反应过程中H2、N2和NH3的物质的量变化如图所示。
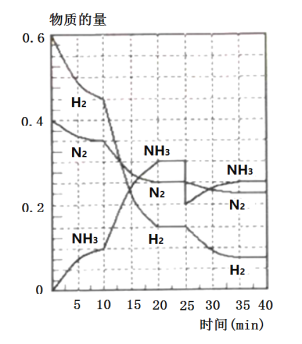
(1)反应开始10min内,NH3的平均反应速率为__________。
(2)反应处于平衡状态的时间段是__________。
(3)判断该反应达到平衡状态的标志是__________(填字母)。
a.N2和NH3的浓度之比等于1:2
b.NH3的百分含量保持不变
c.容器中气体的压强不变
d.3
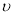 (NH3)=2
(NH3)=2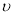 (H2)
(H2)e.容器中混合气体的密度保持不变
(4)图中10~20min内曲线发生变化的可能原因__________。
(5)25min时作出的改变是__________,此时
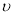 正__________
正__________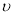 逆(填“>”“<”或“=”)。
逆(填“>”“<”或“=”)。高一化学原理综合题困难题查看答案及解析
-
某研究性学习小组学生根据氧化还原反应规律,探究NO2、NO与Na2O2反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析Na2O2和NO2都既有氧化性又有还原性,于是提出如下假设:
假设1:Na2O2氧化NO2;
假设2:NO2氧化Na2O2。
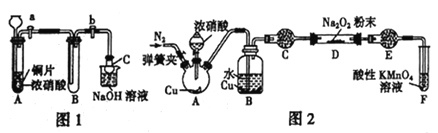
(1)甲同学设计如图1装置进行实验:
①试管A中反应的离子方程式是_________________________________________。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B;向其中加入适量Na2O2粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
③仪器C兼有防倒吸的作用,仪器C的名称为___________________。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是________________________。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设1正确,则NO2和Na2O2反应的化学方程式是_______________________。
Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被Na2O2氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与
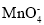 反应生成
反应生成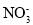 和Mn2+。
和Mn2+。(3)丙同学用图2所示装置(部分夹持装置略)探究NO与Na2O2的反应。
①在反应前,打开弹簧夹,通入一段时间N2,目的是_________________。
②B中不能观察到的现象是____________(填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色b.有红棕色气泡产生c.有无色气泡产生
③C、E中所盛装的试剂不能是________(填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④F中发生反应的氧化剂与还原剂的物质的量之比为_____________。
⑤充分反应后,检验D装置中产物的方法是:______________,则产物是NaNO2。
高一化学实验题困难题查看答案及解析
-
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
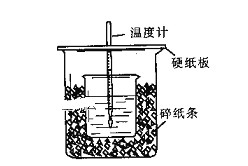
(1)从实验装置上看,图中尚缺少的一种玻璃用品是:______________。
(2)烧杯间填满碎纸条的作用是:_____________________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值___________(填“偏大、偏小、无影响”)
(4)加入NaOH溶液的正确操作是_____________(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(5)上述实验测得的结果与书上的57.3kJ/mol有偏差,产生偏差的原因可能是______________
a.实验装置保温、隔热效果差
b.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好.
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(6)若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量_______(填“小于”、“等于”或“大于”)57.3kJ
(7)已知:CH3COOH(aq)与NaOH(aq)反应的△H=﹣12.1kJ•mol﹣1;HCl(aq)与NaOH(aq)反应的△H=﹣55.6kJ•mol﹣1.则CH3COOH在水溶液中电离的△H等于______________.
A.﹣67.7kJ•mol﹣1 B.﹣43.5kJ•mol﹣1 C.+43.5kJ•mol﹣1 D.+67.7kJ•mol﹣1
高一化学实验题困难题查看答案及解析
-
短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列叙述正确的是( )
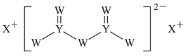
A.元素非金属性强弱的顺序为W>Y>Z
B.Y单质的熔点高于X单质
C.W分别与X、Y、Z形成的二元化合物均只有一种
D.化合物M中W不都满足8电子稳定结构
高一化学单选题困难题查看答案及解析
-
已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化,Z是NO,下列推 断不合理的是
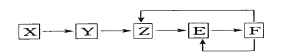
A.X可能是一种氢化物 B.X生成Z一定是化合反应
C.E可能是一种有色气体 D.F中M元素的化合价可能为+5
高一化学单选题困难题查看答案及解析
-
某学习小组设计实验制备Ca(NO2)2,实验装置如图所示(夹持装置已略去)。已知:2NO+CaO2===Ca(NO2)2;2NO2+CaO2==Ca(NO3)2。下列说法不正确的是
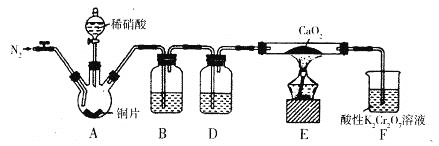
A. 通入N2是为了排尽装置中的空气
B. 装置B、D中的试剂可分别为水和浓硫酸
C. 将铜片换成木炭也可以制备纯净的亚硝酸钙
D. 借助装置A及氢氧化钠溶液和稀硫酸可以分离CO2和CO
高一化学单选题困难题查看答案及解析
-
已知:钴是一种中等活泼金属,常见化合价为+2价和+3价,CoC12 易溶于水。
巴蜀中学化学课外活动小组同学设计实验制取(CH3COO)2Co(乙酸钴)并验证其分解产物。请回答下列问题:
(1)甲同学用Co2O3与盐酸反应制备CoCl2,其实验装置如下:
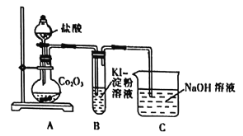
①盛装盐酸的仪器名称__________;烧瓶中发生反应的化学方程式为_________。
②由实验事实可得出结论,氧化性Co2O3_______MnO2 (填“大于”、“小于”或“无法判断”)。
(2)利用甲同学制得的CoCl2可进一步制得(CH3COO)2Co的结晶水合物。乙同学利用下列装置检验(CH3COO)2Co结晶水合物在氮气气氛中的分解产物。其中E、F、G中的试剂均足量。已知PdC12溶液能被CO还原为Pd。
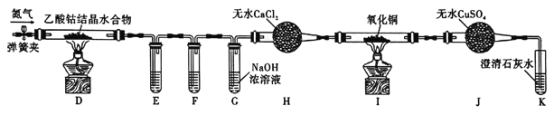
①装置E、F是用于检验分解产物中的CO和CO2,则E中所盛的溶液是_______。
②经分析知分解产物还有C2H6,已知C2H6在较高温度下具有还原性,则上述实验中可确定有C2H6生成的现象是_____________。
③实验结束时,先_______,一段时间后再_________。
④下图为乙酸钴结晶水合物[(CH3COO)2Co·xH2O]热分解时的失重率曲线(失重率等于某阶段分解后固体损失的质量占最初固体样品质量的百分比)。已知第二阶段分解所得固体产物为钴的一种氧化物,且无H2O生成,请通过计算并写出第二阶段分解反应的化学方程式________。
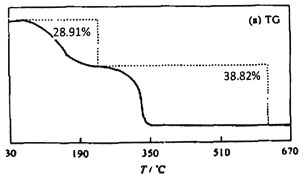
高一化学实验题困难题查看答案及解析
-
短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下n为气体。m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是( )

A.离子半径:Z>X
B.2.4 gm在足量的n中充分燃烧,固体质量增加1.6 g
C.最简单气态氢化物的稳定性:W>X
D.n+p→s+t的过程中,有离子键、共价键的断裂,也有离子键、共价键的形成
高一化学单选题困难题查看答案及解析