-
无水氯化铁是一种重要的化工原料,其熔点为306℃,沸点为315℃,极易潮解。工业制备氯化铁的一种工艺如下:
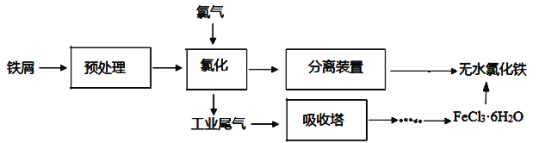
回答下列各题:
(1)向沸水中滴入几滴饱和氯化铁溶液,煮沸至溶液变为红褐色,该过程可用离子方程式表示为________________。
(2)由FeCl3·6H2O获得无水氯化铁的方法是_________。
(3) “氯化”时,若温度超过400℃产物中存在相对分子质量为325的物质,该物质的化学式为_______________。
(4)吸收塔内盛放的吸收剂为____________。
(5)某兴趣小组仿照工业制备无水氯化铁,设计如下实验:

①装置C中玻璃丝的作用为_____________;
②该实验设计存在的明显缺陷为_______________;
③通过下列实验测定实验后所得固体中FeCl3的质量分数。
a.称取mg所得固体,溶于稀盐酸,再转移到100mL容量瓶中,用蒸馏水定容;
b.取出10mL待测溶液液于锥形瓶中,加人稍过量的KI溶液充分反应;
c.以淀粉做指示剂,用bmol/LNa2S2O3溶液滴定(I2+2Na2S2O3=Na2S4O6+2NaI),共用去VmL。
通过上述实验测得所得固体中氯化铁的质量分数为_____________;若加入淀粉偏多,可能导致最终结果______(填“偏大”“偏小”或“无影响”)。
高一化学实验题困难题查看答案及解析
-
甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
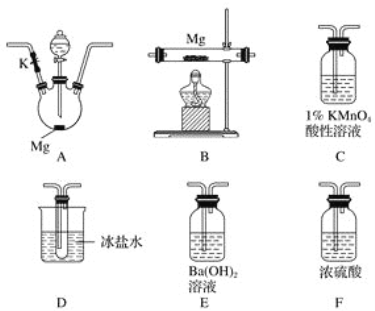
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是________________________________。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→____________→E,确定还原产物中有二氧化氮的现象是______________________________________,实验中要多次使用装置F,第二次使用F的目的是______________________________________________。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:________________________________。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是______________________________________。
(5)设计一种实验方案,验证镁与硝酸反应时确实有氮气生成:__________________________。
高一化学实验题困难题查看答案及解析
-
Ⅰ:某学习小组为了探究硝酸铁的热稳定性,设计如下实验:

利用如图所示装置进行实验。加热A中Fe(NO3)3固体,装置B中均能看到红棕色气体,装置A中试管内剩余红棕色粉末状固体。
(1)装置B的作用是______;
(2)甲同学认为装置A中试管内剩余的红棕色粉末固体为Fe2O3。乙同学为了验证甲的观点,设计了下列实验
①取该固体少量于洁净试管内加入盐酸,固体溶解成棕黄色溶液,该反应的离子方程式为:______。
②向该棕黄色溶液中滴入__________(填化学式)溶液,溶液变为血红色。
(3)经过检验发现C装置中生成了NaNO3和NaNO2。请写出生成这两种盐的化学反应方程式______,最后用排水法收集到少量无色气体,关于该无色气体,下列说法正确的是_______(选填编号)
A.该气体是NO B.主要是O2,还有少量N2 C.NO和O2
(4)通过以上实验,写出Fe(NO3)3受热分解的化学反应方程式____________________。
Ⅱ:CH4燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由CH4、空气(氧气)、KOH(电解质溶液)构成。其中负极的电极方程式为:______。则电池放电时通入空气的电极为______(填“正极”或“负极”);电解质溶液的pH______(填“变大”或“变小”);每转移0.8mol电子消耗______gCH4。
高一化学实验题困难题查看答案及解析
-
海洋是巨大的资源宝库。大连市充分利用沿海优势,优先发展海水淡化生 产与综合利用一体化绿色循环经济产业,逐步建立起较为完善的海水淡化产业链,全 面推动海水淡化相关技术研发、装备制造、原材料生产和盐化工等产业集聚发展。
Ⅰ.从海水中提取食盐和溴的过程如下:
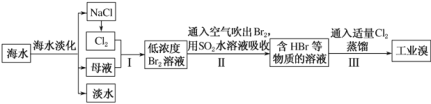
(1)海水淡化的方法主要有蒸馏法、_________________等(写出一种即可)。
(2)步骤Ⅰ中已获得 Br2,步骤Ⅱ中又将 Br2 还原为 Br-,其目的为_____________。
(3)步骤Ⅱ用 SO2 水溶液吸收 Br2,吸收率可达 95%,有关反应的离子方程式为_____;由此反应可知,除环境保护外,在该工业生产中应解决的主要问题是________。
(4)步骤Ⅲ蒸馏过程中,温度应控制在 80~90 ℃。温度过高或过低都不利于生产, 若温度过高,大量水蒸气随溴排出,溴蒸气中水分增加;若温度过低,则_____________________________。
Ⅱ.某化学研究性学习小组模拟工业上从浓缩的海水中提取液溴的过程,设计了如下 实验装置(夹持装置略去)和操作流程。已知:Br2 的沸点为 59 ℃,微溶于水,有毒。
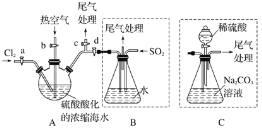
①连接 A 与 B,关闭活塞 b、d,打开活塞 a、c,向 A 中缓慢通入 Cl2 至反应完全;
②关闭活塞 a、c,打开活塞 b、d,向 A 中鼓入足量热空气;
③进行步骤②的同时,向 B 中通入足量 SO2;
④关闭活塞 b,打开活塞 a,再通过 A 向 B 中缓慢通入足量 Cl2;
⑤将 B 中所得液体进行萃取、分液,蒸馏并收集液溴。 请回答下列问题:
(1)步骤②中鼓入热空气的作用是_______________________________。
(2)进行步骤③时,B 中尾气可用___________________(填字母)吸收处理。
a.水 b.浓硫酸 c.NaOH 溶液 d.饱和 NaCl 溶液
(3)若直接连接 A 与 C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸, 再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C 中反应生成了 NaBrO3、NaBr、CO2,则该反应的化学方程式为____________________。
(4)与 B 装置相比,采用 C 装置的优点为___________________________。
高一化学实验题困难题查看答案及解析
-
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):_____接________,_____接_____,____接____;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中_______,丙中_______;
(3)丁中酸性KMnO4溶液的作用是_________;
(4)写出甲中反应的化学方程式________ 。
高一化学实验题困难题查看答案及解析
-
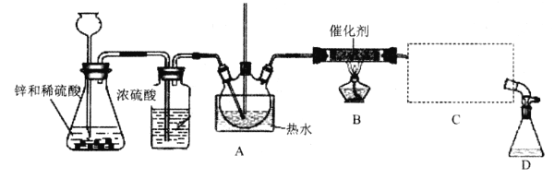
三氯甲烷又称氯仿,是一种无色透明液体,易挥发,有香气,略有甜味,不易燃烧,但在常温下与空气直接接触,易被氧化,并生成剧毒物光气,常用作有机溶剂和麻醉剂,结构简式为CHCl3。实验室中可用热还原CCl4法制备氯仿,装置示意图及有关数据如下:
物质
相对分子质量
密度/(g/Ml)
沸点/℃
水中溶解性
CHCl3
119.5
1.50
61.3
难溶
CCl4
154
159
76.7
难溶
实验步骤:
① ;
② 向三颈瓶中滴入20mL CCl4;
③ 开始通入H2;
④ 向A处水槽中加入热水,并接通C处冷凝装置的冷水;
⑤ 点燃B处酒精灯;
⑥ 反应结束后,停止加热,将D处锥形瓶中收集到的液体分别用适量NaHCO3溶液和水洗涤,分出的产物加入少量无水CaCl2固体,静置后过滤;
⑦ 对滤液进行蒸馏纯化,得到氯仿15g。请回答:
(1) A中长直玻璃管的作用为_____;①处的操作为_______。
(2) B处中发生主要反应的化学方程式为___________。
(3) C处中应选用的冷凝管为____(填选项字母);冷水应从该冷凝管的____(填“a”或 “b”)口接入。
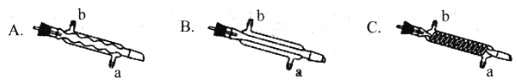
(4)该实验中,氯仿的产率为_______。
(5)氯仿在空气中能被氧气氧化生成HCl和光气(COCl2),该反应的化学方程式为_____.
高一化学实验题困难题查看答案及解析
-
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。根据如图转化回答有关问题:
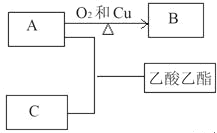
(1)依据所学内容写出A与C反应生成乙酸乙酯的化学方程式______,
(2)写出A到B的化学方程式______。
(3)实验室利用如图的装置制备乙酸乙酯。
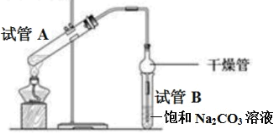
与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是______。
(4)已知下表数据:
物质
熔点/℃
沸点/℃
密度/(g/cm3)
乙醇
-144
78
0.789
乙酸
16.6
117.9
1.05
乙酸乙酯
-83.6
77.5
0.90
浓硫酸
——
338
1.84
①按装置图装好仪器,需要试剂为3mL乙醇,2mL乙酸,适量浓硫酸,请选择合适加入顺序______
A.先加浓硫酸,再加乙醇,最后加乙酸
B.先加浓硫酸,再加乙酸,最后加乙醇
C.先加乙酸,再加浓硫酸,最后加乙醇
D.先加乙醇,再加浓硫酸,最后加乙酸
②根据上表数据分析,为什么乙醇需要过量一些,其原因是______。
(5)停止加热,取下试管B,嗅闻管内液体气味,闻到更多的是刺激性气味。为进一步验证产物中某些杂质存在,在保持试管B相对稳定情况下,沿试管内壁滴入紫色石蕊试液,静置片刻会在试管内油层下方明显看到液体呈现三种颜色,由上而下分别为红色、紫色、蓝色,其原因可能是______、______、______,故产品需进行提纯。
(6)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
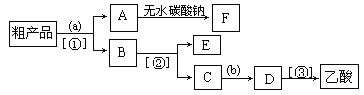
分离方法②是______,试剂b是______(填试剂名称);
(7)为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡试管B再测有机物的厚度,实验记录如表:
编号
试管A中试剂
试管B中试剂
有机层厚度/cm
A
3mL乙醇、2mL乙酸、1mL18mol/L浓硫酸
饱和Na2CO3溶液
5.0
B
3mL乙醇、2mL乙酸
饱和Na2CO3溶液
0.1
C
3mL乙醇、2mL乙酸、3mL2mol/L硫酸
饱和Na2CO3溶液
1.2
D
3mL乙醇、2mL乙酸、一定体积浓度的盐酸
饱和Na2CO3溶液
1.2
实验D的目的是与实验C对照,证明H+对该反应的催化作用。实验D中加入盐酸的体积和浓度分别是______mL和______mol/L。
(8)用30g乙酸与60g乙醇反应,如果实验产率是理论产率的55%,则可得到的乙酸乙酯的质量是______g(精确到0.1)
高一化学实验题困难题查看答案及解析
-
某些资料认为NO、NO2不能与Na2O2反应。南开中学化学学习小组提出质疑,他们分析过氧化钠和二氧化氮都有氧化性,根据化合价升降原则提出假设:
假设I:过氧化钠氧化二氧化氮,生成NaNO3;
假设II:二氧化氮氧化过氧化钠,生成O2。
(1)小组甲同学设计实验如下:
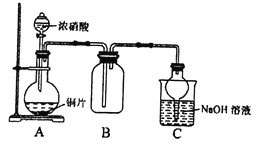
①试管A中反应的化学方程式是__________。
②待试管B中收集满气体,向试管B中加入适量Na2O2,塞紧塞子,振荡试管,观察到红棕色气体迅速消失;再将带火星木条迅速伸进试管内,木条复燃。甲同学认为假设I正确;乙同学认为该装置不能达到实验目的,为达到实验目的,应在A、B之间增加一个浓硫酸洗气装置,该装置的作用是_______。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星木条未复燃。得出结论:假设I正确。NO2和Na2O2反应的方程式是________。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化。
查阅资料:①2NO+Na2O2=2NaNO2
②亚硝酸盐在酸性条件下不稳定:2H++3
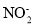 =
=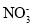 +2NO↑+H2O。
+2NO↑+H2O。丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
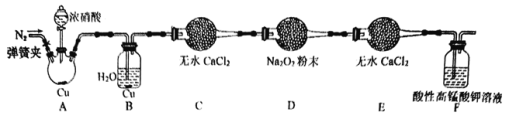
①在反应前,打开弹簧夹,通入一段时间N2,目的是_________。
②充分反应后,取D装置中产物少许,加入稀盐酸,若观察到________现象,则产物是亚硝酸钠。
③F装置的作用是________。该装置中发生反应的离子方程式为_________。
高一化学实验题困难题查看答案及解析
-
德国化学家凯库勒认为, 苯分子的结构中碳碳间以单 、双键交替排列结合成环状。为了验证凯库勒观点的正误,某学生设计了以下实验方案(尾气吸收装置已省略):
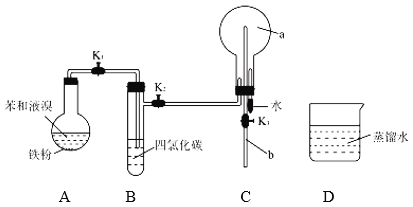
实验步骤:
①按如图所示的装置连接好仪器, ;
②在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞;
③打开止水夹K1、K2、K3;
④反应结束后,关闭 K2 , 将b插入烧杯D 的蒸馏水中,挤压胶头滴管使少量水进入烧瓶a 中;
⑤观察实验现象。
请回答:
(1)步骤①中,应补充的操作为 ________。
(2)烧瓶A中所发生反应的化学方程式为_________。
(3)装置B的作用为__________。
(4)证明凯库勒观点错误的实验现象为________。
(5)A中得到的粗产品经过一系列除杂操作后 ,获得苯和溴苯的混合物,将二者进行分离的操作名称为__________
高一化学实验题困难题查看答案及解析
-
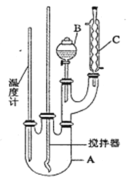
某科学小组制备硝基苯的实验装置如下,有关数据列如下表。已知存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯。
物质
熔点/℃
沸点/℃
密度/g.cm-1
溶解性
苯
5.5
80
0.88
微溶于水
硝基苯
5.7
210.9
1.205
难溶于水
间二硝基苯
89
301
1.57
微溶于水
浓硝酸
83
1.4
易溶于水
浓硫酸
338
1.84
易溶于水
实验步骤如下:
取100mL烧杯,用20 mL浓硫酸与足量浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)图中装置C的作用是_______________________________。
(2)制备硝基苯的化学方程式__________________________________________________。
(3)叙述配制混合酸操作:______________________________________________。
(4)为了使反应在50℃~60℃下进行,常用的方法是______________。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是________________________(用化学方程式说明),除去该有色物质选择的试剂是____________,分离提纯的方法为___________,涉及的离子方程式为_______________。
(5)在洗涤操作中,第二次水洗的作用是________________________________________。
(6)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用水直形冷凝管的原因是_______________________________________________________________。
(7)本实验所得到的硝基苯产率是______________________。
高一化学实验题困难题查看答案及解析