-
已知铜元素能形成多种化合物。
(1)写出基态Cu的M能层的电子排布式 ,Cu同周期的元素中,与铜原子最外层电子数相等的元素还有 (填元素符号)
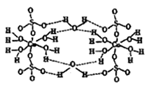
(2)CuSO4·5H2O也可写成[Cu(H2O)4]SO4·H2O,其结构示意图如右图所示:该晶体中所含元素电负性由大到小顺序是 ,该晶体属于 晶体,该晶体中由水分子参与形成的作用力有 。
(3)Cu2+能与NH3、Cl-等形成配位数为4的配合物,已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 ,NH3的VSEPR 模型为 。
-
已知A、B、C、D均为短周期元素,它们的原子序数依次递增. A是最外层为一个电子的非金属元素,C 原子的最外层电子数是次外层的3倍; C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物.A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3.
请回答下列问题:
(1)写出B的原子结构示意图________,写出C和D形成的淡黄色固体化合物的电子式________.
(2)元素原子的物质的量之比为A:B:C=4:2:3 的晶体名称为________.
(3)请写出与A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的微粒的符号(举两例)________、________.
(4)写出由B、C元素组成且元素原子质量比为B:C=7:12的化合物的化学式________.
-
已知A、B、C、D均为短周期元素,它们的原子序数依次递增。 A是最外层为一个电子的非金属元素,C 原子的最外层电子数是次外层的3倍; C和D可形成两种固态化合物,其中一种为淡黄色固体;B和C可形成多种气态化合物。A、B、C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为A:B:C=4:2:3。请回答下列问题:
(1)写出B的原子结构示意图 ,写出C和D形成的淡黄色固体化合物的电子式 。
(2)元素原子的物质的量之比为A:B:C="4:" 2:3 的晶体名称为 , 其水溶液显 性,其反应的离子方程式为 。
(3)请写出A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两种元素组成的微粒的符号(举两例) 、 。
(4)写出由B、C元素组成且元素原子质量比为B:C=7:12的化合物的化学式 。
-
已知X、Y、Z、W、T是短周期中原子序数依次增大的5种主族元素.其中Y和X两种元素可以组成1:1、1:2、1:3、1:4等多种化合物; Z原子最外层电子数是次外层电子数的3倍,W与X同主族,W与T形成的化合物WT是厨房必需的调味品,下列说法正确的是( )
A.原子半径:T>W>Z>Y
B.W与T的单质可通过电解饱和的WT水溶液获得
C.Z与W形成的两种化合物中化学键类型完全相同
D.元素X、Z与T可形成多种酸
-
已知X、Y、Z、W、T是短周期中原子序数依次增大的5种主族元素.其中Y和X两种元素可以组成1:1、1:2、1:3、1:4等多种化合物; Z原子最外层电子数是次外层电子数的3倍,W与X同主族,W与T形成的化合物WT是厨房必需的调味品.下列说法正确的是( )
A.原子半径:T>W>Z>Y
B.W与T的单质可通过电解饱和的WT水溶液获得
C.Z与W形成的两种化合物中化学键类型完全相同
D.元素X、Z与T可形成多种酸
-
X、Y、Z为前四周期元素,X与Y位于同一周期。X是生物体中不可缺少的元素之一,它能形成多种化合物。其基态原子中有15种电子运动状态.Y的负一价离子的最外层电子数与次外层的电子数相同;Z是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。
(1)基态X 原子中,电子占据的最高能层符号为_____;该能层中电子占据的能量最高的电子云在空间有___个伸展方向,原子轨道呈_______形.
(2)单质X与单质Y2反应,可以生成XY3和XY5,其中各原子满足最外层8电子稳定结构的化合物中,X原子的杂化轨道类型为________,其分子的空间构型为________。
(3)元素Z基态原子的核外电子排布式为______,其同周期元素中,第一电离能最小的是____(写元素符号)。
(4)Z与Y形成的一种化合物的立方晶胞如图所示.

①该晶胞中,含有____个Y原子。该化合物的化学式为_____,设晶胞棱长为anm,则此晶体密度为____g/cm3(写出计算表达式,摩尔质量用M表示,阿伏伽德罗常数用NA表示)
②该化合物难溶于水但易溶于氨水,其原因是_________。
-
元素X位于第四周期,其基态原子有4个未成对电子。Y原子最外层电子数是其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子,W原子的2p轨道上有3个未成对电子。
(1)Y与W、Z可形成多种化合物。
①元素Y与Z中电负性较大的是_________________(用元素符号描述)。
②离子ZY32-的空间构型为_______________ (用文字描述),杂化方式______________。
③ZY2空间构型_________,杂化方式________,分子的极性________(填“极性”或“非极性”)。
④元素Y与W中第一电离能较大的是___________________(用元素符号描述)。
(2)Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是_____________。
(3)含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH3)]。
①基态X2+的电子排布式是________________。
②1 mol配合物K3[X(CN)5(NH3)]中含σ键的数目为___________。
③画出X原子的价电子排布图___________________;
④ [X(CN)5(NH3)]3-配离子中存在的化学键类型有_____________(填序号):
a、配位键 b、氢键 c、极性共价键 d、非极性共价键 e、离子键
-
【物质结构与性质】元素X位于第四周期,其基态原子有4个未成对电子。Y原子最外层电子数是其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子。
(1)Y与Z可形成多种化合物。
①元素Y与Z中电负性较大的是 (用元素符号描述)。
②离子ZY32-的空间构型为 (用文字描述)。
③写出一种与ZY2互为等电子体的氧化物分子的化学式 。
(2)Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是 。
(3)含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH3)]。
①基态X2+的电子排布式是 。
②1 mol配合物K3[X(CN)5(NH3)]中含σ键的数目为 。
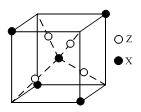
(4)右图为X与Z所形成的一种化合物的基本结构单元,推测该化合物的化学式: 。
-
《物质结构与性质》
元素X位于第四周期,其基态原子有4个未成对电子。Y原子最外层电子数是其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子。
(1) Y与Z可形成多种化合物。
① 元素Y与Z中电负性较大的是________(用元素符号描述)。
② 离子ZY的空间构型为________(用文字描述)。
③ 写出一种与ZY2互为等电子体的氧化物分子的化学式:________。
(2) Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是________。
(3) 含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH3)]。
① 基态X2+的电子排布式是________。
② 1 mol配合物K3[X(CN)5(NH3)]中含σ键的数目为________。
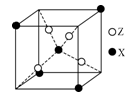
(4) 右图为X与Z所形成的一种化合物的基本结构单元,推测该化合物的化学式为________。
-
元素X位于第四周期,其基态原子有4个未成对电子。Y原子最外层电子数是其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子。
(1)Y与Z可形成多种化合物
① 元素Y与Z中电负性较大的是____________(用元素符号描述)。
② 离子ZY32-的空间构型为____________(用文字描述)。
(2) Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是____________。
(3) 含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH3)]。
① 基态X2+的电子排布式是____________。
② 1 mol配合物K3[X(CN)5(NH3)]中含σ键的数目为____________。
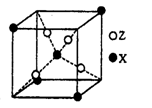
(4) 如图为X与Z所形成的一种化合物的基本结构单元,推测该化合物的化学式为________。




