-
钒(23V)是我国的丰产元素,广泛应用于催化及钢铁工业,有“化学面包”、金属“维生素”之称。回答下列问题:
(1)钒原子的核外电子排布式为________________,在元素周期表中的位置为______。
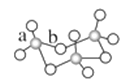
(2)V2O5常用作SO2转化为SO3的催化剂。基态S原子电子占据最高能级的电子云轮廓为________形;气态SO3以单分子形式存在,其分子的立体构型为_______形;固体SO3的三聚体环状结构如图所示,该结构中S—O键长有a、b两类,b的键长大于a的键长的原因为______________。
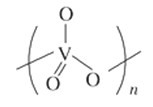
(3)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子中V的杂化轨道类型为___________;也可得到偏钒酸钠,其阴离子呈如图所示的无限链状结构,则偏钒酸钠的化学式为_____________。
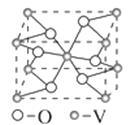
(4)钒的某种氧化物晶胞结构如图所示。该氧化物的化学式为__________,若它的晶胞参数为x nm,则晶胞的密度为__________ g/cm3。
-
(15分)[选修3—物质结构与性质]钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。回答下列问题:
(1)钒在元素周期表中的位置为 ,其价层电子排布图为 。
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为 、 。
(3)V2O5常用作SO2 转化为SO3的催化剂。SO2 分子中S原子价层电子对数是 对,分子的立体构型为 ;SO3气态为单分子,该分子中S原子的杂化轨道类型为 ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为 ;该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个σ键。
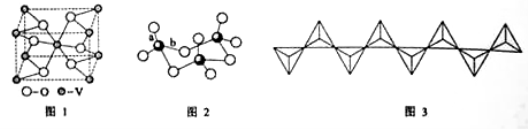
(4)V2O5 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 ____ 。
-
随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。已知钒的原子序数为23,回答下列问题:
(1)钒被认为是一种稀土元素,广泛分散于各种矿物中,钾钒铀矿中的钒原子最外层已达到8 电子稳定结构,其化学式为K2H6U2V2O15(其中钒元素的化合价为+5价)。若用氧化物的形式表示,该化合物的化学式为:_______________________________。
(2)五氧化二钒是工业制造中的常用催化剂,如工业制硫酸中就利用五氧化二钒作催化剂。从含钒废催化剂中回收钒,传统的技术是“氧化焙烧法”,其具体流程为:

其中焙烧是将食盐和钒铅矿在空气中焙烧,这时矿石中所含的V2O5就转化为NaVO3,然后用水从烧结块中浸出NaVO3,再用稀硫酸酸化就得到V2O5的水合物,经过煅烧就可得到V2O5。
①配料在焙烧前磨碎的目的是_______________________。
②写出焙烧过程中V2O5发生反应的化学方程式:___________________________。
(3)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO,再用盐酸、硫酸亚铁、草酸等测定钒。反应的化学方程式为:VO2++H2C2O4==VO++2CO2+H2O。若反应消耗0.9 g 草酸,参加反应的钒元素质量是_____g。
(4)以V2O5为催化剂,使SO2转化为SO3的反应如下:2SO2(g)+O2(g) 2SO3(g)。某温度下,SO2的平衡转化率(a)与体系总压强(P)的关系如图所示。
2SO3(g)。某温度下,SO2的平衡转化率(a)与体系总压强(P)的关系如图所示。

根据图示回答下列问题:
①将2.0mol SO2和1.0mol O2置于10L密闭容器中,反应达平衡后,体系总压强为0.10MPa.该反应的平衡常数表达式为__________,等于______________。
②平衡状态由A变到B时,平衡常数K(A)______K(B)(填“>”、“<”或“=”)。
-
随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。已知钒的原子序数为23,回答下列问题:
(1)钒被认为是一种稀土元素,广泛分散于各种矿物中,钾钒铀矿中的钒原子最外层已达到8电子稳定结构,其化学式为K2H6U2V2O15(其中钒元素的化合价为+5价)。若用氧化物的形式表示,该化合物的化学式为______________________。
(2)五氧化二钒是工业制造中的常用催化剂,如工业制硫酸中就利用五氧化二钒作催化剂。从含钒废催化剂中回收钒,传统的技术是“氧化焙烧法”,其具体流程为配料→
磨碎→焙烧→水浸→沉钒→煅烧→五氧化二钒。其中焙烧是将食盐和钒铅矿在空气中焙烧,这时矿石中所含的V2O5就转化为NaVO3,然后用水从烧结块中浸出NaVO3,再用稀硫酸酸化就得到V2O5的水合物,经过煅烧就可得到V2O5。
①配料在焙烧前磨碎的目的是
________________________________________________________________________。
②从水浸→沉钒必要的操作是________。
A.萃取 B.过滤
C.蒸馏 D.结晶
③写出焙烧过程中V2O5发生反应的化学方程式:
________________________________________________________________________。
(3)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO,再用盐酸、硫酸亚铁、草酸等测定钒。请配平下列反应的化学方程式。
________VO2++________H2C2O4===________VO++________CO2+________H2O。
若反应消耗0.9 g草酸,参加反应的钒元素质量是________g。
-
随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金的维生素”.已知钒的原子序数为23,相对原子质量为51,试回答下列问题:
(1)钒在元素周期表位于第________周期,第________族.
(2)钒被认为是一种稀土元素,广泛分散于各种矿物中,钾钒铀矿中的化学式为K2H6U2V2O15(其中钒元素的化合价为+5价).若用氧化物的形式表示,该化合物的化学式为________.
(3)测定钒含量的方法是先把钒转化成V2O5,V2O5在酸性溶液里转变成VO2+,再用盐酸、硫酸亚铁、草酸等测定钒.请配平下列反应的化学方程式:________VO2++________H2C2O4→________VO++________CO2+________H2O其中还原剂是________;若反应消耗0.90g草酸,参加反应的钒元素质量是________g.
(4)工业上由V2O5冶炼金属钒常用铝热剂法.试用化学方程式表示出来________.
-
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。下图是钒电池基本工作原理示意图:
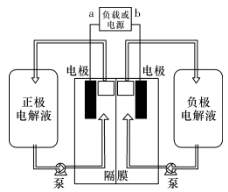
请回答下列问题:
(1) 钒的氧化物是化学工业中最佳催化剂之一,有“化学面包”之称。已知钒原子的质子数为23,则钒在元素周期表中的位置是_____________。
(2) 钒电池是以溶解于一定浓度硫酸溶液中的不同种类的钒离子(V2+、V3+、VO2+、VO2+)为正极和负极电极反应的活性物质,电池总反应为VO2++V3+ +H2O V2++VO2++2H+。放电时的正极反应式为______________,充电时,b为外界电源的_________极,充电时电池的负极反应式为______________。
V2++VO2++2H+。放电时的正极反应式为______________,充电时,b为外界电源的_________极,充电时电池的负极反应式为______________。
(3) 为保证电池稳定运行,“隔膜”选用质子交换膜,利用钒电池进行电解精炼铜,每得到64 g精铜,钒电池正负极电解液质量将相差__________g(水分子无法透过隔膜,假设原正负极电解液质量相同)。
-
钒的用途十分广泛,有金属“维生素”之称。某工厂为了从含有杂质的VOSO4样品中回收得到催化剂V2O5,设计流程如下:

请回答下列问题:
(1)步骤①所得废渣的成分是(写化学式)。NH4VO3在焙烧前要洗涤2-3次,该步操作方法为________。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
步骤②中萃取时必须加入适量碱,其原因是________。
步骤③中X试剂为________。
(3)⑤的离子方程式为________。
(4)该工艺流程中,可以循环利用的物质有________和________。
(5)若取VOSO4样品wg,测得消耗a mol·L—1氯酸钾溶液VmL(氯酸钾还原产物为氯化钾),则1kg样品理论上可制得的V2O5质量是________g(用含w、V的代数式表示)。
-
目前,我国是最大的钢铁生产国,钢铁是国民经济的基础产业,铁及其化合物的应用也越来越广泛。回答下列问题:
(1)画出铁的原子结构示意图:______________。
(2)工业炼铁时常用CO还原铁矿粉,已知:
① Fe2O3(s) + 3CO(g)=2Fe(s)+ 3CO2(g) △H=-24.8 kJ/mol
② Fe3O4(S)+CO(g)=-3FeO(g)+CO2(g) △H= +19.4 kJ/mol
③ FeO(s)+CO(g)=Fe(s)+CO2(g) △H= -11.0 kJ/mol
则反应3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)的△H= ________。
(3)Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) 反应温度与K的关系如右表:
| 反应温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数K | 64 | 50.7 | 42.9 |
恒温1000℃在体积为10L的恒容密闭容器中加入0.1molFe2O3和0.1molCO,气体混合物中CO2的体积分数φ(CO2)随时间t的变化关系如图所示。
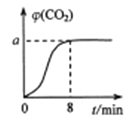
①前 8minCO 的反应速率为_______;平衡时a=____。
②若再向平衡混合物中加入0.01molCO 和0.02molCO2,平衡_______移动;若要使平衡混合气中CO2的体积分数增大,下列措施可行的是_______(填标号)。
A.增大Fe2O3用量 B.增大压强 C.降低温度 D.向容器中再充入少量CO
(4)纳米级的Fe3O4在催化剂、造影成像、药物载体、靶向给药等领域都有很好的应用前景,工业生产中常用“共沉淀法”来制备。将FeCl2和FeCl3按一定比例配成混合溶液,用NaOH溶液作为沉淀剂,在特定条件下即可制得纳米级的Fe3O4,反应的离子方程式是_____,在实际生产中Fe2+和Fe3+反应用量比常是2:3,甚至1:1,为什么?________。
(5)纳米铁粉可用于除去废水中的NO3-,反应的离子方程式为:4Fe+ NO3-+ 10H+=4Fe2++NH4++3H2O。研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是________;若加入少量Cu2+,废水中NO3-的去除速率大大加快,可能的原因是_____________。
-
金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1)一种镍催化法生产GaN的工艺如图:
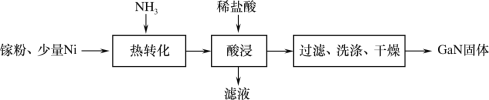
①镓(Ga)的原子结构示意图为 ,镓元素在周期表中的位置是___。
,镓元素在周期表中的位置是___。
②“热转化”时Ga转化为GaN的化学方程式是___。
③“酸浸”操作目的是___。
(2)某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
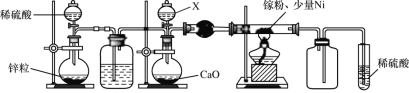
①仪器X中的试剂是__,加热前需先通入一段时间的H2,原因是__。
②取某GaN样品m克溶于足量热NaOH溶液,发生反应GaN+OH﹣+H2O GaO2-+NH3↑,用H3BO3溶液将产生
GaO2-+NH3↑,用H3BO3溶液将产生 NH3完全吸收,滴定吸收液时消耗浓度为cmol/L的盐酸VmL,则样品的纯度是___。
NH3完全吸收,滴定吸收液时消耗浓度为cmol/L的盐酸VmL,则样品的纯度是___。
已知:NH3+H3BO3=NH3•H3BO3;NH3•H3BO3+HCl=NH4Cl+H3BO3
-
金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1)一种镍催化法生产GaN的工艺如图:
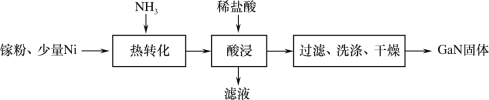
①镓(Ga)的原子结构示意图为 ,镓元素在周期表中的位置是___。
,镓元素在周期表中的位置是___。
②“热转化”时Ga转化为GaN的化学方程式是___。
③“酸浸”操作目的是___。
(2)某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
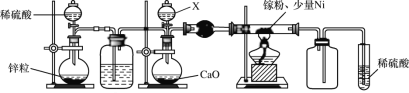
①仪器X中的试剂是__,加热前需先通入一段时间的H2,原因是__。
②取某GaN样品m克溶于足量热NaOH溶液,发生反应GaN+OH﹣+H2O GaO2-+NH3↑,用H3BO3溶液将产生
GaO2-+NH3↑,用H3BO3溶液将产生 NH3完全吸收,滴定吸收液时消耗浓度为cmol/L的盐酸VmL,则样品的纯度是___。
NH3完全吸收,滴定吸收液时消耗浓度为cmol/L的盐酸VmL,则样品的纯度是___。
已知:NH3+H3BO3=NH3•H3BO3;NH3•H3BO3+HCl=NH4Cl+H3BO3





 2SO3(g)。某温度下,SO2的平衡转化率(a)与体系总压强(P)的关系如图所示。
2SO3(g)。某温度下,SO2的平衡转化率(a)与体系总压强(P)的关系如图所示。






