-
25℃时,0.1 mol/L的NH4HCO3溶液pH=7.7。向0.1mol/L的NH4HCO3溶液中逐滴加入0.1mol/LNaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量分数)。根据图象判断,下列说法正确的是

A.NH4HCO3溶液中,水解程度:NH4+>HCO3-
B.开始阶段,HCO3-略有增加的主要原因是发生反应:2NH4HCO3+2NaOH=(NH4)2CO3+Na2CO3+2H2O
C.由图中数据可知:CO32-的水解常数约为5.3×10-11
D.由图中数据可知:NH3•H2O的电离常数约为1.5×10-5
-
25℃下,水中碳酸化合物的三种微粒占总浓度的百分比随pH变化如图所示。25℃时,向10mL0.1mol・L-lNa2CO3溶液中逐滴加入0.1mol・L-1稀盐酸,下列说法正确的是( )
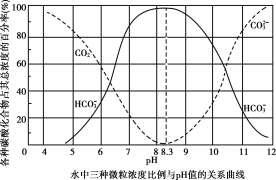
A.0.1mol・L-lNa2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
B.溶液pH=8.3时,c(Na+)=c(C1-)
C.溶液pH=7时,加入盐酸体枳大于10mL
D.溶液pH=6时的导电能力强于pH=11时的导电能力
-
如图表示在20ml0.1mol⋅L-1CH3COOH溶液中逐滴加入0.1mo1⋅L-1的NaOH溶液的pH变化曲线。下列说法正确的是( )
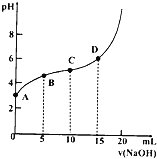
A.A点溶液存在的关系:c(H+)=c(OH-)+Ka(CH3COOH)-
B.C点溶液中各微粒浓度的大小关系为:c(CH3COOH)>c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C.在C点溶液中加少量的酸或碱溶液,pH变化不大
D.D点为该反应的滴定终点
-
常温下,向0.1 mo1·L-1的NH4HCO3溶液中逐滴加入NaOH,溶液中部分含氮、含碳微粒的分布情况如下图所示。下列说法不正确的是
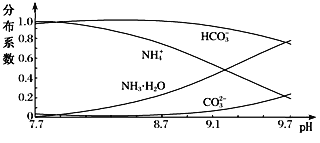
A. 开始阶段,HCO3- 增加的原因可能是:HCO3-的水解平衡逆向移动
B. pH在8.7~9.7之间,HCO3-和NH4+同时与OH-反应
C. 通过分析可知常温下:Kb(NH3·H2O)<Ka1(H2CO3)
D. pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3·H2O)>c(CO32-)
-
常温下,关于下列溶液的说法错误的是
A.某物质的溶液中由水电离出的c(H+)=1×10-10mol/L,则该溶液的pH可能为4或10
B.已知0.1 mol/L NaClO溶液的pH为9.7,0.1 mol/LNaF溶液的pH为7.5,则等体积两溶液中离子总数大小关系为:N(NaClO)>N(NaF)
C.将0.2 mol/L的某一元酸HA溶液和0.1 mol/LNaOH溶液等体积混合后溶液pH大于7,则所得溶液中:2c(OH-)=2c(H+)+c(HA)-c(A-)
D.向饱和氯水中加入NaOH溶液至PH=7,则所得溶液中:c(Na+) >c(Cl-) >c(ClO-) >c(OH-)= c(H+)
-
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法正确的是:
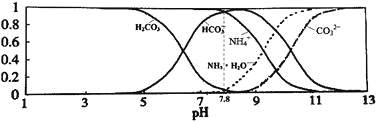
A. 当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3·H2O)>c(CO32-)
B. NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3·H2O)+c(H+)=c(OH-)+2c(CO32-)+c(H2CO3)
C. 往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小
D. 通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3)
-
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法正确的是:
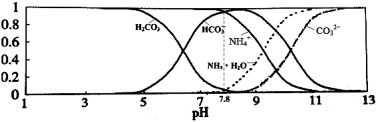
A.当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3·H2O)>c(CO32-)
B.NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3·H2O)+c(H+)=c(OH-)+2c(CO32-)+c(H2CO3)
C.往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小
D.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3)
-
常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法正确的是:
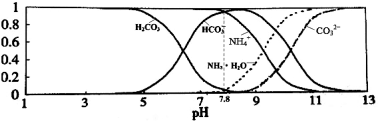
A.当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3-)>c(NH3·H2O)>c(CO32-)
B.NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3·H2O)+c(H+)=c(OH-)+2c(CO32-)+c(H2CO3)
C.往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小
D.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3)
-
已知常温下,0.1 mol/L的NH4HCO3溶液pH=7.8。往碳酸的饱和水溶液中通入NH3,测得含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示。下列说法错误的是 ( )
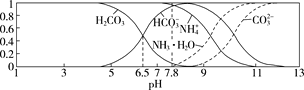
A.常温下,Kb(NH3·H2O)>Ka1(H2CO3)
B.向pH=6.5的上述溶液中通入NH3时,NH4+和HCO3-浓度都逐渐减小
C.NH4HCO3溶液中存在关系:c(NH4+)+c(NH3·H2O)=c(HCO3-)+c(CO32-)+c(H2CO3)
D.当溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3·H2O)>c(CO32-)
-
向0.1mol/I.的NH4HCO3溶液中逐渐加入0.1mol/LNaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量分数)。根据图象,下列说法不正确的是( )
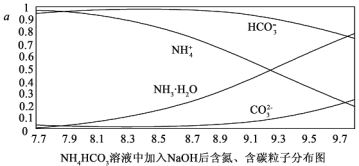
A. 开始阶段,HCO3-反而略有增加,可能是因为NH4HCO3溶液中存在H2CO3发生的主要反应是H2CO3+OH-═HCO3-+H2O
B. 当pH大于8.7以后,碳酸氢根离子和铵根离子同时与氢氧根离子反应
C. pH=9.5时,溶液中c(HCO3-)>c(NH3•H2O)>c(NH4+)>c(CO32-)
D. 滴加氢氧化钠溶液时,首先发生的反应为2NH4HCO3+2NaOH═(NH4)2CO3+Na2CO3








