-
“可燃冰”的主要成分是甲烷与水分子的结晶水合物(CH4·nH2O)。其晶体类型是( )
A.离子晶体
B.分子晶体
C.原子晶体
D.金属晶体
高三化学单选题简单题查看答案及解析
-
我国将与德国合作,在近期启动钻探“可燃冰”的实物样品的工作,实现“可燃冰”钻探零的突破.“可燃冰”的主要成分是甲烷水合物[CH4•nH2O]晶体.有关甲烷水合物的说法正确的是( )
A.它属于原子晶体
B.它属于混合物
C.可燃冰可以燃烧说明水具有可燃性
D.甲烷水合物中H2O是极性分子,CH4是非极性分子高三化学选择题中等难度题查看答案及解析
-
据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4·nH2O)。
(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是________。
(2)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油。
①在101 KPa时,1.6 g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64 kJ。则甲烷与H2O(g)反应的热化学方程式:________。
②CH4不完全燃烧也可制得合成气:CH4(g)+
O2(g)===CO(g)+2H2(g);
△H=-35.4 kJ·mol-1。则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为(填序号);原因是________。
③在温度为T,体积为10L的密闭容器中,加入1 mol CO、2 mol H2,发生反应
CO(g)+ 2H2(g)
CH3OH(g);△H=-Q kJ·mol-1(Q>O),达到平衡后的压强是开始时压强的0.6倍,放出热量Q1kJ。
I.H2的转化率为________;
II.在相同条件下,若起始时向密闭容器中加入a mol CH3 OH(g),反应平衡后吸收热量Q2 kJ,且Q1+Q2=Q,则a=________mol。
III.已知起始到平衡后的CO浓度与时间的变化关系如右图所示。则t1时将体积变为5L后,平衡向________反应方向移动(填“正”或“逆”);
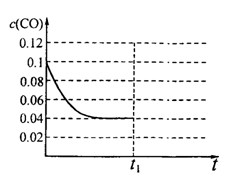
在上图中画出从tl开始到再次达到平衡后,
CO浓度与时间的变化趋势曲线。
(3)将CH4设计成燃料电池,其利用率更高,装置示意如右图(A、B为多孔性碳棒)。
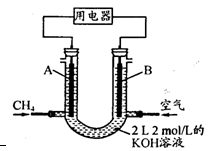
持续通人甲烷,在标准状况下,消耗甲烷体积VL。
①O<V≤44.8 L时,电池总反应方程式为________;
②44.8 L<V≤89.6 L时,负极电极反应为________;
③V=67.2 L时,溶液中离子浓度大小关系为________;
高三化学填空题中等难度题查看答案及解析
-
2017年11月16日,国土资源部召开新闻发布会,宣布天然气水合物,即“可燃冰”新矿种获得国务院批准,成为我国第173个矿种。“可燃冰”主要成分的分子式是CH4·8H2O,一旦温度升高或压强降低,甲烷气就会逸出,固体水合物便趋于崩解。“可燃冰”将成为人类的后续能源。
(1)将320 g可燃冰释放的甲烷完全燃烧生成液态水时,可放出1 780.6 kJ的能量,则表示甲烷燃烧热的热化学方程式是__________________。
(2)CH4不仅是优质的气体燃料,还能利用它和CO2重整,发生反应:CO2(g)+CH4(g)
2CO(g)+2H2(g),获得合成气(主要成分为CO、H2),从而减少温室气体的排放。在一定条件下CH4的平衡转化率与温度及压强(单位:Pa)的关系如图所示。则y点:v(正)____(填“>”、“=”或“<”,下同)v(逆);压强:p1____p2;该反应的ΔH____0。
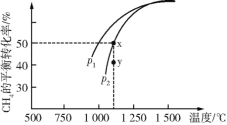
(3)在恒温、p2下,在一容积可变的容器中,达到平衡状态x时四种气体的物质的量均为1 mol,若此时再充入四种气体各1 mol,则平衡____(填“向左”、“向右”或“不”)移动。
(4)一定条件下,CH4还可与NO2反应,改善雾霾天气,其化学方程式为CH4(g)+2NO2(g)
CO2(g)+2H2O(g)+N2(g),在恒温恒容下,下列可以判断该反应达到平衡状态的是____(填序号)。
a.v逆(N2)=2v正(H2O)
b.混合气体的密度不再变化
c.混合气体的物质的量不再变化
d.单位时间内有1 mol NO2消耗同时消耗1 mol CO2
e.混合气体的平均相对分子质量不变
f.CH4与CO2的物质的量之比不再发生变化
(5)在恒温恒容下,使1 mol CH4(g)与2 mol NO2反应,达平衡后,再往反应器中分别充入下列气体,可以使CH4(g)+2NO2(g)
CO2(g)+2H2O(g)+N2(g)中NO2转化率增大的是____(填序号)。
A.CH4 B.CO2
C.物质的量之比为1∶2的CH4与NO2 D.N2
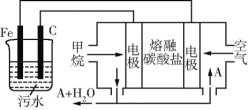
(6)CH4还可以运用到电化学中,某课外小组用CH4为燃料,空气为氧化剂,稀土金属材料作电极,电浮选凝聚法处理污水,设计如图所示装置。则甲烷 燃料电池的总反应式为______。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(如图),A物质的化学式是______。
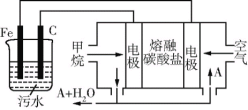
高三化学综合题中等难度题查看答案及解析
-
2017年11月16日,国土资源部召开新闻发布会,宣布天然气水合物,即“可燃冰”新矿种获得国务院批准,成为我国第173个矿种。“可燃冰”主要成分的分子式是CH4·8H2O,一旦温度升高或压强降低,甲烷气就会逸出,固体水合物便趋于崩解。“可燃冰”将成为人类的后续能源。
(1)将320 g可燃冰释放的甲烷完全燃烧生成液态水时,可放出1 780.6 kJ的能量,则表示甲烷燃烧热的热化学方程式是__________________。
(2)CH4不仅是优质的气体燃料,还能利用它和CO2重整,发生反应:CO2(g)+CH4(g)
2CO(g)+2H2(g),获得合成气(主要成分为CO、H2),从而减少温室气体的排放。在一定条件下CH4的平衡转化率与温度及压强(单位:Pa)的关系如图所示。则y点:v(正)____(填“>”、“=”或“<”,下同)v(逆);压强:p1____p2;该反应的ΔH____0。
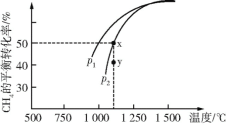
(3)在恒温、p2下,在一容积可变的容器中,达到平衡状态x时四种气体的物质的量均为1 mol,若此时再充入四种气体各1 mol,则平衡____(填“向左”、“向右”或“不”)移动。
(4)一定条件下,CH4还可与NO2反应,改善雾霾天气,其化学方程式为CH4(g)+2NO2(g)
CO2(g)+2H2O(g)+N2(g),在恒温恒容下,下列可以判断该反应达到平衡状态的是____(填序号)。
a.v逆(N2)=2v正(H2O)
b.混合气体的密度不再变化
c.混合气体的物质的量不再变化
d.单位时间内有1 mol NO2消耗同时消耗1 mol CO2
e.混合气体的平均相对分子质量不变
f.CH4与CO2的物质的量之比不再发生变化
(5)在恒温恒容下,使1 mol CH4(g)与2 mol NO2反应,达平衡后,再往反应器中分别充入下列气体,可以使CH4(g)+2NO2(g)
CO2(g)+2H2O(g)+N2(g)中NO2转化率增大的是____(填序号)。
A.CH4 B.CO2
C.物质的量之比为1∶2的CH4与NO2 D.N2
(6)CH4还可以运用到电化学中,某课外小组用CH4为燃料,空气为氧化剂,稀土金属材料作电极,电浮选凝聚法处理污水,设计如图所示装置。则甲烷 燃料电池的总反应式为______。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(如图),A物质的化学式是______。
高三化学综合题中等难度题查看答案及解析
-
科学家最近又发现了一种新能源——“可燃冰”它的主要成分是甲烷与水分子的结晶水合物(CH4·nH20)。其形成:埋于海底地层深处的大量有机质在缺氧环境中,厌氧性细菌把有机质分解,最后形成石油和天然气(石油气),其中许多天然气被包进水分子中,在海底的低温与高压下形成了类似冰的透明晶体,这就是“可燃冰”。又知甲烷同CO2一样也是温室气体。这种可燃冰的晶体类型是 ( )
A.离子晶体 B.分子晶体
C.原子晶体 D.金属晶体
高三化学单选题中等难度题查看答案及解析
-
天然气水合物,也称“可燃冰”(主要组成为CH4 •nH2O),在我国南海地区预计有680亿吨油当量的“可燃冰”。下列有关说法正确的是
A. “可燃冰”属于纯净物
B. “可燃冰”代替燃油可减少大气污染
C. “可燃冰”开采不当,CH4释放到空气中对环境没有影响
D. “可燃冰”作为能源不会产生污染物CO和温室气体CO2
高三化学选择题中等难度题查看答案及解析
-
目前人类正在研究发展从海底开采可燃冰(CH4•nH2O)的技术,以解决能源问题。下列有关说法错误的是
A.可燃冰是分子晶体,熔沸点低
B.CH4分子结构是对称的
C.H2O是非极性分子
D.使用可燃冰替代煤和石油,可以解决酸雨问题
高三化学选择题中等难度题查看答案及解析
-
目前人类正在研究发展从海底开采可燃冰(CH4?nH2O)的技术,以解决能源问题。下列有关说法错误的是
A.可燃冰是分子晶体,熔沸点低
B.CH4分子结构是对称的
C.H2O是非极性分子
D.使用可燃冰替代煤和石油,可以解决酸雨问题
高三化学选择题中等难度题查看答案及解析
-
下列说法错误的是( )
A. 用聚乙烯塑料代替聚乳酸塑料可减少白色污染
B. 大量燃烧化石燃料是造成雾霾天气的一种重要因素
C. 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
D. 乙烯可作水果的催熟剂
高三化学选择题中等难度题查看答案及解析