-
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别是bmol/L和2bmol/L,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用( )
A.Ca(OH)2 B.NaOH
C.NaHCO3 D.Na2CO3]
高三化学单选题中等难度题查看答案及解析
-
1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别为b mol/L和2b mol/L,请在下列试剂中选用最合适的一种试剂把溶液中的Mg2+、Ca2+去掉( )
A.NaHCO3 B.Na2CO3 C.NaOH D.Ca(OH) 2
高三化学选择题简单题查看答案及解析
-
某自来水厂利用河水处理成自来水的工艺流程示意图如下图所示:
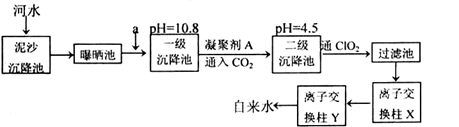
提供的试剂:饱和Na2CO3溶液、NaOH溶液、生石灰、CC14、BaCl2溶液,KOH溶液
(1)为除水中含有Ca2+、Mg2+、HCO3-、Cl-、SO42-,试剂a代表两种化学物质,主要是除去水中SO42-、Mg2+和HCO3-,这两种试剂是_______和______(只填化学式)。
(2)凝聚剂A常用FeSO4·7H2O,最终生成红褐色胶状沉淀,该胶状沉淀的化学式为______,可以除去其中的悬浮固体颗粒,该过程是______ (填序号)。
A.只有物理变化,无化学变化 B.只有化学变化,无物理变化
C.既有化学变化,又有物理变化
(3)通入CO2的目的是______和______。
(4)传统的氧化剂是Cl2,现代工艺用ClO2取代Cl2,通入CIO2的作用是______,优点是______。
(5)离子交换柱X、Y中有一种是H+型交换柱,另一种是H-型离子交换柱,目的是除去水中残留的杂质离子,则X应是哪种交换柱______(填“H+型”、“OH-型”);如果两个交换柱位置颠倒会产生什么后果____________。
高三化学填空题困难题查看答案及解析
-
某自来水厂利用河水处理成自来水的工艺流程示意图如下图所示:
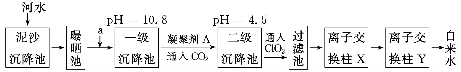
提供的试剂:饱和Na2CO3溶液、NaOH溶液、生石灰、CCl4、BaCl2溶液、KOH溶液
(1)为除去水中含有的Ca2+、Mg2+、HCO3-、Cl-、SO42-,试剂a代表两种化学物质,主要是除去水中SO42-、Mg2+和HCO3-,这两种试剂是________和________(只填化学式)。
(2)凝聚剂A常用FeSO4·7H2O,最终生成红褐色胶体沉淀,该胶状沉淀的化学式为________,可以除去其中的悬浮固体颗粒,该过程是________(填序号)。
A.只有物理变化,无化学变化
B.只有化学变化,无物理变化
C.既有化学变化,又有物理变化
(3)通入CO2的目的是__________和__________。
(4)传统的氧化剂是Cl2,现代工艺用ClO2取代Cl2,通入ClO2的作用是________________________;优点是________________________________。
(5)离子交换柱X、Y中有一种是H+型交换柱,另一种是OH-型离子交换柱,目的是除去水中残留的杂质离子,则X应是哪种交换柱?________(填“H+型”或“OH-型”);如果两个交换柱位置颠倒会产生什么后果?_______________________________________
________________________________________________________________________。
高三化学填空题困难题查看答案及解析
-
某地海水中主要离子的含量如下表:
成分
Na+
K+
Ca2+
Mg2+
Cl-
SO42-
HCO3-
含最/mg·L-1
9360
83
200
1100
16000
1200
118
利用电渗析法技术可将海水淡化,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过。下列说法中不正确的是

A. 电解一段时阳后阴极区会发生反应:Ca2++OH-+HCO3-==CaCO3↓+H2O
B. 阳极的电极反应式为2H2O-4e-=O2+4H+
C. 电解时b室中阴离子移向a室,阳离子移向c室
D. 淡水的出口为b出口
高三化学选择题中等难度题查看答案及解析
-
实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
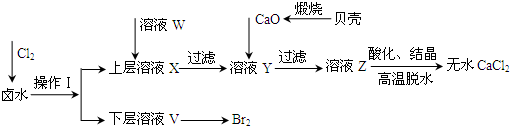
(1)操作Ⅰ使用的试剂是______,所用的主要仪器名称是______.
(2)加入溶液W的目的是______.用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择的pH最大范围是______.酸化溶液Z时,使用的试剂为______.
(3)实验室用贝壳与稀盐酸反应制备并收集气体,下列装置中合理的是______.开始沉淀时的pH 沉淀完全时的pH Mg2+ 9.6 11.0 Ca2+ 12.2 c(OH-)=1.8mol•L-1 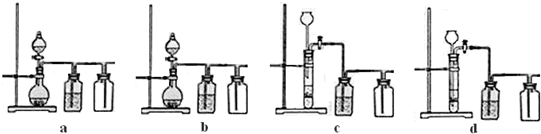
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11.某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3.该实验设计不正确,错误在于______.
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论).______.
仪器自选.
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸.高三化学解答题中等难度题查看答案及解析
-
某研究性学习小组拟取盐湖苦卤的浓缩液(富含Ca2+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的无水CaCl2及液溴,他们设计了如下流程:
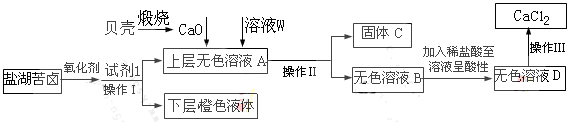
回答以下问题:
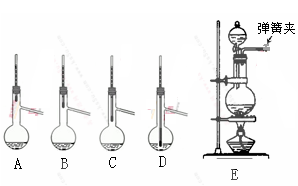
(1)操作Ⅰ中加入的试剂1是________;在从橙色液体中分离出溴时,可能会导致收集到的产品中混有低沸点杂质的装置(见图A、B、C、D)是________。
(2)加入溶液W的目的是________。
(3)操作Ⅲ所用的仪器除三脚架、酒精灯,还需要________。
(4)某同学用如上图E所示的实验装置制取操作1前的氧化剂,写出该反应的离子方程式________,试简述该装置气密性的检验方法________。
高三化学实验题中等难度题查看答案及解析
-
(15分)海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
成分
Na+
K+
Ca2+
Mg2+
Cl-
SO42-
HCO3-
含量/mg∙L-1
9360
83
160
1100
16000
1200
118
(1)海水显弱碱性的原因是(用离子方程式表示): ,该海水中Ca2+的物质的量浓度为__________mol/L 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过,电极均为惰性电极。
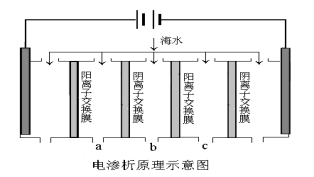
① 开始时阳极的电极反应式为 。
② 电解一段时间, 极(填“阴”或“阳”)会产生水垢,其成份为 (填化学式)。
③ 淡水的出口为a、b、c中的__________出口。
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图所示:
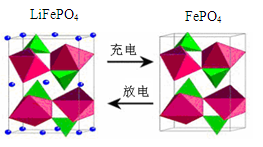
该电池电解质为能传导 Li+的固体材料。
上面左图中的小黑点表示 (填粒子符号),充电时该电极反应式为 。
(4)利用海洋资源可获得MnO2 。MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾。该制备过程中消耗相同条件下氯气和空气的体积比为 (空气中氧气的体积分数按20%计)。
高三化学填空题极难题查看答案及解析
-
Ⅰ.从海水得到的粗食盐水中常含Ca2+、Mg2+、SO
,需要分离提纯。现有含少量CaCl2、MgSO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中Ca2+、Mg2+、SO
。提纯时的操作步骤和加入试剂的情况如图。
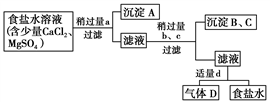
图中a、b、c、d分别表示上述4种试剂中的一种,试回答:
(1)沉淀A的名称是________。
(2)试剂d是________;判断试剂d已经足量的方法是
________________________________________________________________________。
(3)加入b、c后溶液中发生的化学反应的化学方程式为
________________________________________________________________________。
(4)现有下列仪器,过滤出沉淀A、B、C时必须用到的是____(填序号),仪器③的名称是________。
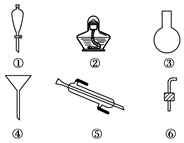
Ⅱ.海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的 ________(填序号),该仪器名称为________,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做________。
高三化学简答题简单题查看答案及解析
-
实验室以含有Ca2+、Mg2+、Cl-、SO
、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
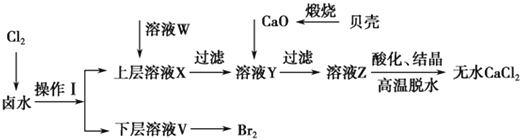
(1)操作Ⅰ使用的试剂是____________,所用主要仪器的名称是________。
(2)加入溶液W的目的是______________。用CaO调节溶液Y的pH,可以除去Mg2+。由表中数据可知,理论上可选择的pH最大范围是____________。酸化溶液Z时,使用的试剂为__________。
开始沉淀时的pH
沉淀完全时的pH
Mg2+
9.6
11.0
Ca2+
12.2
c(OH-)=1.8 mol·L-1
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是__________。
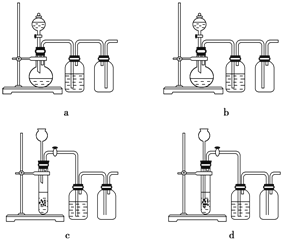
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3的酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于___________________________。用一个化学方程式表示H2SO3酸性强于H2CO3: __________________。
高三化学综合题中等难度题查看答案及解析