-
完成下列问题。
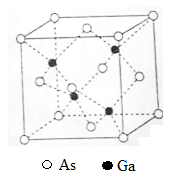
(1)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等.
①As的基态原子的电子排布式[Ar]_______________.
②第一电离能:As___Ga(填“>”、“<”或“=”).
(2)配合物Fe(CO)5常温下呈液态,熔点为-20.5 ℃,易溶于 CCl4 中,则Fe(CO)5是______分子(非极性或极性)。
(3)BF3常温下是气体,有强烈的接受孤电子对的倾向。BF3与NH3相遇,立即生成白色固体。BF3的杂化轨道类型为:____ ;写出该白色固体的结构式,并标注出其中的配位键___________。
(4)下列有关说法不正确的是____。
A.沸点:NH3 >PH3,CH3OH > HCHO
B.SO2与CO2的化学性质有些类似,但空间结构与杂化方式不同
C.熔、沸点: SiF4< SiCl4< SiBr4 <SiI4 , 原因是分子中共价键键能逐渐增大
D.熔点: CaO > KCl > KBr,原因是晶格能逐渐减小

(5)钠钾合金属于金属晶体,某种合金的晶胞结构如图所示,晶体中K 原子的配位数为______;已知金属原子半径r(Na)、r(K),计算晶体的空间利用率 __________(假设原子是刚性球体)
-
太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______;S原子的价电子排布式为________;Ga、As和Se的第一电离能由大到小的顺序是________。
(2)Na3As3中As原子的杂化方式为_____;AsCl3的空间构型为____。
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________。
(4)写出一种与SO42-互为等电子体的分子_________。
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_____。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,则GaAs晶胞中Ga之间的最短距离为________pm。
-
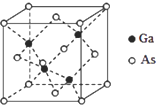
太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______;S原子的价电子排布式为________;Ga、As和Se的第一电离能由大到小的顺序是________。
(2)Na3As3中As原子的杂化方式为_____;AsCl3的空间构型为____。
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________。
(4)写出一种与SO42-互为等电子体的分子_________。
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_____。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,则GaAs晶胞中Ga之间的最短距离为________pm。
-
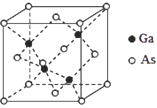
太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______;S原子的价电子排布式为________;Ga、As和Se的第一电离能由大到小的顺序是________。
(2)Na3As3中As原子的杂化方式为_____;AsCl3的空间构型为____。
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________。
(4)写出一种与SO42-互为等电子体的分子_________。
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_____。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,则GaAs晶胞中Ga之间的最短距离为________pm。
-
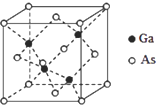
常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、砷化镓(GaAs)太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)镓元素位于元素周期表的____周期_____族,砷原子核外的电子有___种运动状态。
(2)Si、P、S 的第一电离能由大到小的顺序是 _____________, 二氧化硅和干冰晶体的熔点差别很大,其原因是________________________________________________。
(3)与AsF3互为等电子体的分子为___________(只写一中),其空间构型为_________。
(4)硼酸(H3BO3)本身不能电离出H+,在水溶液中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为______________。
②[B(OH)4]-的结构式为________________。
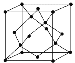
(5)金刚石的晶胞如图所示,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。
①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是________________(用化学式表示);
②金刚石的晶胞参数为a pm(1 pm=10-12 m)。 金刚石晶胞的密度为_________g/cm3(只要求列算式,阿伏加德罗常数为NA)。
-
【化学——选修3:物质结构】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式 。
(2)根据元素周期律,原子半径Ga As,第一电离能Ga As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为 ,其中As的杂化轨道类型为 。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是 。
(5)GaAs的熔点为1238℃,密度为 ,其晶胞结构如图所示。
,其晶胞结构如图所示。
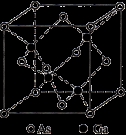
该晶体的类型为 。Ga与As的摩尔质量分别为 和
和 ,原子半径分别为
,原子半径分别为 和
和 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则
,则 晶胞中原子的体积占晶胞体积的百分率为 。(已知1m=1012pm)
晶胞中原子的体积占晶胞体积的百分率为 。(已知1m=1012pm)
-
砷化镓(GaAs)是优良的半导体材料或用于制作微型激光器或太阳能电池的材料等。部分元素在周期表中位置如下:
回答下列问题:
(1)六种元素中,非金属性最强的元素是:________.写出As原子的最外层的电子排布式_________,As原子核外有_____个未成对电子。
(2)根据元素周期律,可判断原子半径Ga_____As。(选填“>”、 “<”或“=”)。写出铝的最高价氧化物对应水化物的电离方程式:________________
(3)NH3 的分子构型是_______。GaF3的熔点高于1000°C,GaCl3的熔点为77.9°C,可能的原因是_______.写出C2H2的电子式为:_________
(4)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因___________
| GeCl4 | GeBr4 | GeI4 |
| 熔点/°C | -49.5 | 26 | 146 |
| 沸点/°C | 83.1 | 186 | 约400 |
-
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。部分元素在周期表中位置如下:

回答下列问题:
(1)六种元素中,非金属性最强的元素是:_______。写出 As 原子的最外层的电子排布式_______,As 原子核外有_______个未成对电子。
(2)根据元素周期律,可判断原子半径Ga_______As。(选填“>”、“<”或“=”)。写出铝的最高价氧化物对应水化物的电离方程式:______。
(3)NH3 的 分 子 构 型 是_____。 GaF3 的 熔 点 高 于 1000℃ , GaCl3 的 熔 点 为 77.9℃ , 可 能 的 原 因 是_____。写出 C2H2 的电子式为:____。
(4)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____。

-
[化学——选修3:物质结构与性质]
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
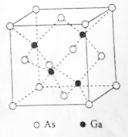
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1 和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
-
[化学——选修3:物质结构与性质]砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。