-
X、Y、Z、M、R、W均为周期表中前四周期的元素。X的基态原子外围电子排布式为3s2;Y原子的L电子层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍。回答下列问题(相关回答均用元素符号表示):
(1)X的基态原子的外围电子排布式为 ,其基态原子有 种运动状态不同的电子;
(2)R的氢化物的稳定性比其上一周期同族元素氢化物的稳定性 (高或低)其原因是 ;
(3)ZM3﹣空间构型为 ,其中Z的杂化方式为 ;
(4)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为 ;与YM分子互为等电子体的离子的化学式为 .
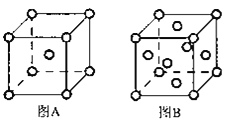
(5)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如下图A、B所示:

图B中原子堆积方式为 ,A、B中W原子的配位数之比为 .A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为 。
(6)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为 。
-
X、Y、Z、M、R、W均为周期表中前四周期的元素.X的基态原子外围电子排布式为3s2;Y原子的L电子层的p能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为__,其基态原子有__种能量不同的电子。
(2)R的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是__。
(3)ZM3-空间构型为___,其中Z的杂化方式为__。
(4)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为___;与YM分子互为等电子体的离子的化学式为___。
(5)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图A、B所示:图B中原子堆积方式为___,A、B中W原子的配位数之比为___。A、B晶胞的棱长分别为acm和bcm,则A、B两种晶体的密度之比为___。
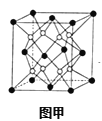
(6)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为___。
-
X、Y、Z、M、R、W均为周期表中前四周期的元素.X的基态原子外围电子排布式为3s2;Y原子的L电子层的p能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子;M的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;R是海水中除氢、氧元素外含量最多的元素;W为过渡元素,它的基态原子外围电子排布成对电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为__,其基态原子有__种能量不同的电子。
(2)R的氢化物的沸点比其上一周期同族元素氢化物的沸点低的原因是__。
(3)ZM3-空间构型为___,其中Z的杂化方式为__。
(4)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为___;与YM分子互为等电子体的离子的化学式为___。
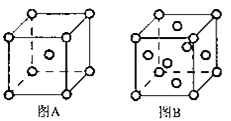
(5)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如图A、B所示:图B中原子堆积方式为___,A、B中W原子的配位数之比为___。A、B晶胞的棱长分别为acm和bcm,则A、B两种晶体的密度之比为___。
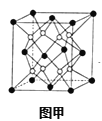
(6)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为___。
-
[化学—选修3:物质结构与性质]
X、Y、Z、M、W均为周期表中前四周期的元素.X元素的基态原子外围电子排布式为3s2;Y原子的L能层的P能级上有一个空轨道;Z元素的基态原子最外层有3个未成对电子,次外层有2个电子; M 的基态原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;W为过渡元素,它的基态原子外围电子排布成对的电子数和未成对电子数相同且为最外层电子数的两倍.回答下列问题(相关回答均用元素符号表示):
(1)W的基态原子的外围电子排布图为 其基态原子核外有 种不同电子运动状态;
(2)Z的氢化物的沸点比其下一周期同族元素氢化物的沸点高的原因是
。
(3)W与YM易形成配合物W(YM)5,在W(YM)5中W的化合价为 ;与YM分子互为等电子体的离子的化学式为 。(写一种即可)
(4)W单质的晶体在不同温度下有两种原子堆积方式,晶胞分别如下图A、B所示:

图B中原子堆积方式为 ,A、B中W原子的配位数之比为 。A、B晶胞的棱长分别为a cm和b cm,则A、B两种晶体的密度之比为 。
(5)X和W组成的合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图甲(黑球代表W,白球代表X).则该合金的化学式为 。
-
A、B、C、D、E、F、G均是原子序数小于36的元素。A的基态原子外围电子排布式为3s2;B原子的L电子层的P能级上有一个空轨道; C元素的基态原子最外层有3个未成对电子,次外层有2个电子; D 的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2。
根据信息回答下列问题:
(1)C的外围电子排布图为________。C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为________;
(2)用电子式表示化合物AE2的形成过程________。
(3)F与BD易形成配合物F(BD)5,在F(BD)5中F的化合价为_______;与BD分子互为等电子体的离子的化学式为 。
(4)E有多种含氧酸根①EO- ②EO2- ③EO3- ④EO4-,其中空间构型为四面体型的是________。(填序号)
(5)B、C、D、E原子两两相互化合形成的分子有多种,请列举一种分子内所有原子都满足最外层8电子稳定结构的分子:_________(写分子式)
(6) G的价电子排布式为________。GD晶体晶胞结构为NaCl型, 晶胞边长为428 pm。
晶胞中两个G原子之间的最短距离为___________m(精确至0.01)。由于晶体缺陷,晶体的化学式为 G0.88D,若晶体中的G分别为G2﹢、G3﹢,此晶体中G2﹢与G3﹢的最简整数比为_________。
-
已知A、B、C、D、E 为原子序数依次增大的前四周期元素。已知前四种元素的基态原子p能级都有2个单电子,E 的原子序数等于A、B、C三种元素原子序数之和。
试回答下列问题:
(1)基态E原子外围电子排布图为_________;其中M 能层有_____种能量不同的电子。
(2)从原子结构角度解释B 电负性大于D的原因是:_______________。
(3) 含A元素的化合物中,A 的原子间常有π键,但是含C元素的化合物中,C的原子间只能存在σ键,其主要原因是___________________。
(4)H2D2B8是一种具有强氧化性的二元酸(其中分子结构中有2个B原子显-1价),则H2D2B8的结构式为___________,分子中采取sp3杂化的B原子有______个。
(5)E 晶胞内粒子的堆积模型如图所示。

已知:E 晶胞的密度为ρg/cm3,NA代表阿伏加德罗常数值,E 的相对原子质量为M。
①E 粒子的配位数为_______。
②E 粒子半径为_______pm。
③E 晶胞中粒子的空间利用率φ=_____(用含π 的式子表示)。
-
如图是元素周期表的一部分:

⑴ 阴影部分元素的外围电子排布式的通式为_________。Sb的元素名称为________。基态P原子中,电子占据的最高能级符号为______,该能层具有的原子轨道数为______。
⑵ 氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如上右图所示,则Y轴可表示的氢化物(RH3)性质可能有________。
A.稳定性 B.沸点 C.R—H键能 D.分子间作用力
⑶ 某种新型储氧材料的理论结构模型如下左图所示,图中虚线框内碳原子的杂化轨道类型有____________种。

⑷ CN-和Fe2+、Fe3+及K+能形成一种蓝色配位化合物普鲁士蓝。上右图是该物质的的结构单元(K+未标出),该图是普鲁士蓝的晶胞吗?_______ (填“是”或“不是”),平均每个晶胞中含有______个K+。

⑸磷酸盐与硅酸盐之间具有几何形态的相似性。如多磷酸盐与多硅酸盐一样,也是通过四面体单元通过共用顶角氧离子形成岛状、链状、层状、骨架网状等结构型式。不同的是多硅酸盐中是{SiO4}四面体,多磷酸盐中是{PO4}四面体。右图为一种无限长单链结构的多磷酸根,该多磷酸根的化学式为___________。
-
M是原子序数小于30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于半充满状态。
(1)M原子的外围电子排布式为 ,在周期表中属于 区元素。
(2)M的堆积方式属于钾型,其晶胞堆积方式为 ,其空间利用率为 。
(3)MCl3·6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3 B、[M(H2O)5Cl]Cl2·H2O C、[M(H2O)4Cl2]Cl·2H2O。
为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为_______________ (填A或B或C)。
(4)难溶碳酸盐受热易分解,试比较MgCO3和CaCO3的稳定性,并说明理由 .
(5)已知A12 Cl6 分子中每个原子都满足8电子稳定结构,写出其结构式 (用箭头表示配位键)。
(6)金刚石晶胞(如图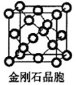 )含有 个碳原子。若碳原子半径为r pm ,金刚石晶胞的边长为a pm ,则r= a,列式并计算金刚石晶胞的空间利用率 。
)含有 个碳原子。若碳原子半径为r pm ,金刚石晶胞的边长为a pm ,则r= a,列式并计算金刚石晶胞的空间利用率 。
-
周期表前四周期的元素Q、R、X、Y、Z原子序数依次增大,Q元素的原子形成的离子就是一个质子;R基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;X基态原子s能级的总电子数比p能级的总电子数多1;Y原子的核外成对电子数是未成对电子数的3倍;Z原子的价电子排布为3d74S2。
回答下列问题:
(1)R、X、Y中第一电离能最大的是 (填元素符号),其中Y原子的电子排布式为 。
(2)Q、R元素形成的某分子中共有14个电子,该分子中R原子采取 杂化,该分子的立体构型为 。
(3)RY可以和很多过渡金属形成配合物,如Fe( RY)5、Ni(RY)4。其中Fe(RY)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe (RY)5晶体属于 (填晶体类型)。RY与N2互为等电子体,与RY互为等电子体的离子有 (任写一种)。
(4)向含Z2+的溶液中加入过量的氨水,并通入适量的Y2气体,生成有[Z(NH3)6]3+离子,则该反应的离子方程式为 。
-
具有下列电子层结构的原子,其对应元素一定属于同一周期的是 ( )
A.两种原子的电子层上全部都是s电子
B.3p能级上只有一个空轨道的原子和3p能级上只有一个未成对电子的原子
C.最外层电子排布为2s22p6的原子和最外层电子排布为2s22p6的离子
D.原子核外的M层上的s能级和p能级都填满了电子,而d轨道上尚未排有电子的两
种原子










 )含有
)含有