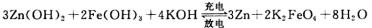-
硫酸在生活和生产中应用广泛。某工厂以黄铁矿(主要成分为FeS2)为原料,采用接触法制备硫酸。
(1)已知在298 K和101 kPa条件下:
FeS2(s)=FeS(s)+S(s) ∆H1
S(s)+ O2(g)=SO2(g) ∆H2
4FeS(s)+7O2(g)=2Fe2O3(s) +4SO2(g) ∆H3
则在该条件下FeS2与O2生成Fe2O3和SO2的热化学方程式为_______。
(2)催化氧化反应:2SO2(g) +O2(g) 2SO3(g) ∆H<0。在体积可变的密闭容器中,维持压强为101 kPa和初始n(SO2)=2mol,充入一定量的O2,SO2的平衡转化率α(SO2)随O2物质的量n(O2)的变化关系如图所示:
2SO3(g) ∆H<0。在体积可变的密闭容器中,维持压强为101 kPa和初始n(SO2)=2mol,充入一定量的O2,SO2的平衡转化率α(SO2)随O2物质的量n(O2)的变化关系如图所示:
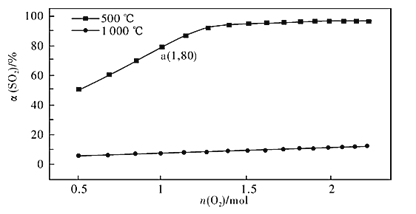
①在1000℃时,SO2平衡转化率随着O2物质的量的增大缓慢升高,解释其原因________。
②a点时SO3的平衡分压p(SO3)=_________Pa(保留两位有效数字,某组分的平衡分压=总压×某组分的物质的量分数)。
(3)保持温度不变,向固定体积的密闭容器中充入一定量的SO2、O2。请画出平衡体系中SO3的体积分数φ(SO3)随初始SO2、O2的物质的量之比[n(SO2)/n(O2)]的变化趋势图______:
(4)已知活性氧可以把SO2快速氧化为SO3,根据计算机模拟结果,在炭黑表面上O2转化为活性氧的反应历程与能量变化关系如图所示。下列说法不正确的是_______(填字母代号)。
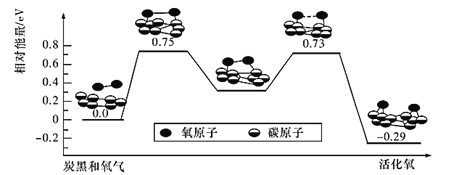
A.O2转化为活性氧是氧氧键的断裂与碳氧键的生成过程
B.该过程的最大能垒(活化能)E正=0.73 eV
C.每活化一个O2分子最终吸收0. 29 eV能量
D.依题炭黑可以作为SO2转化为SO3的催化剂
E.其他条件相同时,炭黑颗粒越小,反应速率越快
(5)硫酸工厂尾气中的SO2可被NaOH溶液吸收,用惰性电极将所得的Na2SO3溶液进行电解,可循环再生NaOH的同时得到H2SO4,写出阳极的电极反应式:___________
-
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(主要成分为FeS2)是生产硫酸的冶炼钢铁的重要原料。高温下可发生反应:其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,该过程若有1.5mol FeS2参加反应,则反应过程中转移_____ mol电子;
6SO2+Fe3O4,该过程若有1.5mol FeS2参加反应,则反应过程中转移_____ mol电子;
(2)氯化铝溶液显酸性,原因是_________________________(用离子方程式稀释);
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素(CO(NH2)2;它易被氧化),原理如下图所示。
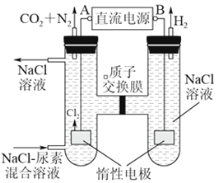
①电源的负极为_________(填“A”或“B”)。
②阳极室中发生的反应依次为_________、_________。
③电解结束后,阴极室溶液的pH与电解前相比将_________;若阴极共收集到气体6.72L(标准状况),则除去的尿素为________ g(忽略气体的溶解)。
(4)为了减少CO对大气的污染,某研究性学习小组拟研究利用CO和H2O反应转化为绿色能源H2。已知:2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•moL-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•moL-1
H2O(g)═H2O(l)△H=-44.0kJ•moL-1
写出CO和H2O(g)作用生成CO2和H2的热化学方程式:_________。
-
(14分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(主要成分为FeS2)是生产硫酸和冶炼钢铁的重要原料。高温下可发生反应:
3FeS2+8O2 6SO2+Fe3O4,该过程中若有1.5mol FeS2参加反应,则反应过程中转移_____mol电子。
6SO2+Fe3O4,该过程中若有1.5mol FeS2参加反应,则反应过程中转移_____mol电子。
(2)氯化铁溶液显酸性,原因是___________________________(离子方程式解释),用惰性电极电解氯化铁溶液之初,阳极电极反应式为:___________________________。
(3)K2FeO4可作为一种“绿色高效多功能”水处理剂。原因是 。目前,人们针对K2FeO4的稳定性进行了大量的探索,并取得了一定的进展。下列物质中有可能提高化合物K2FeO4水溶液稳定性的是
A.亚硫酸钠 B.KOH C.醋酸 D.Fe(NO3)3
(4)K2FeO4与Zn组成新型二次电池高铁电池,电解液为碱溶液,其反应式为:
3Zn(OH)2+2Fe(OH)3+4KOH  3Zn+2K2FeO4+8H2O
3Zn+2K2FeO4+8H2O
放电时电池的负极反应式为_______;充电时电解液的pH________(填“增大”“减小”或“不变”之一)。
-
(10分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(主要成分为FeS2)是生产硫酸和冶炼钢铁的重要原料。高温下可发生反应:
3FeS2+8O2 6SO2+Fe3O4
6SO2+Fe3O4
该过程中若有1.5mol FeS2参加反应,则反应过程中转移_____mol电子。
(2)氯化铁溶液显酸性,原因是___________________(用适当的文字和离子方程式解释),用惰性电极电解氯化铁溶液之初,阳极电极反应式为:____________________________________。
(3)高铁电池是一种新型二次电池,电解液为碱溶液,其反应式为:
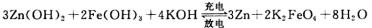
放电时电池的负极反应式为____________________;充电时电解液的pH________(填“增大”“减小”或“不变”之一)。
-
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 Fe3O4+6SO2,有3mol FeS2参加反应,转移________mol电子。
Fe3O4+6SO2,有3mol FeS2参加反应,转移________mol电子。
(2)FeCl3溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________;从腐蚀废液回收得到金属铜,还需要的试剂是________。
(3)与明矾相似,Fe2(SO4)3也可用作净水剂,在使用时发现Fe2(SO4)3并不能使酸性废水中的悬浮物沉降除去,其原因是。
(4)钢铁的电化学腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在下图虚线框中作出修改,并用箭头标出电子流动的方向。
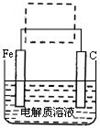
-
铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,有3 mol FeS2参加反应,转移________ mol电子。
6SO2+Fe3O4,有3 mol FeS2参加反应,转移________ mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为________________;从腐蚀废液回收得到金属铜,还需要的试剂是__________________________。
(3)与明矾相似,硫酸铁也可作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是____________________________
(4)钢铁的电化学腐蚀原理如图所示,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在图中虚线框内作出修改,并用箭头标出电子流动方向。
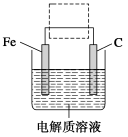
-
(10分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:
3FeS2+8O2 6SO2+Fe3O4,若3 mol FeS2参加反应转移 mol电子。
6SO2+Fe3O4,若3 mol FeS2参加反应转移 mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为 ;腐蚀废液回收得到金属铜还需要的试剂为 。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是 。
(4)下表中,对陈述I、II及其有无因果关系的判断,都正确的是_____(填字母)
| 选项 | 陈述I | 陈述II | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | I对;II对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | I对;II对;无 |
| C | 铁属于过渡金属元素 | 铁和铁的某些化合物可以用作催化剂 | I错;II对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | I对;II对;有 |
-
(10分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,有3 mol FeS2参加反应,转移________mol电子。
6SO2+Fe3O4,有3 mol FeS2参加反应,转移________mol电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_____________;从腐蚀废液回收得到金属铜,还需要的试剂是________。
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是______________________________________ 。
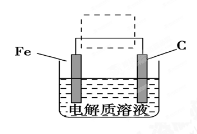
(4)钢铁的电化腐蚀原理如图所示,将该图稍作修改即可成为钢铁电化学防护的简单示意图,请在图中虚线框内作出修改,并用箭头标出电子流动方向。
-
铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,有3mol FeS2参加反应,转移______mol电子.
6SO2+Fe3O4,有3mol FeS2参加反应,转移______mol电子.
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为______;从腐蚀废液回收得到金属铜,还需要的试剂是______.
(3)与明矾相似,硫酸铁也可用作净水剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是______.
(4)钢铁的电化腐蚀简单示意图如图,将该图稍作修改 即可成为钢铁电化学防护的简单示意图,请在虚线框内作出修改,并用箭头标出电子流动方向______.

-
铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 6SO2+Fe3O4,3 mol FeS2参加反应转移________mol 电子。
6SO2+Fe3O4,3 mol FeS2参加反应转移________mol 电子。
(2)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
________________________________________________________________________。
从腐蚀废液回收得到金属铜还需要的试剂为
________________________________________________________________________。
(3)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是____________________________________________________ 。
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母)。
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应生成氢气 | 高温下氢气能还原氧化铁生成铁 | Ⅰ 对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可以用作催化剂 | Ⅰ 错;Ⅱ对;无 |
| D | 铁在空气中表面生成致密氧化膜 | 可用铁罐储存运输浓硫酸、浓硝酸 | Ⅰ 对;Ⅱ对;有 |
2SO3(g) ∆H<0。在体积可变的密闭容器中,维持压强为101 kPa和初始n(SO2)=2mol,充入一定量的O2,SO2的平衡转化率α(SO2)随O2物质的量n(O2)的变化关系如图所示: