如图所示为工业合成氨的流程图。有关说法不正确的是( )
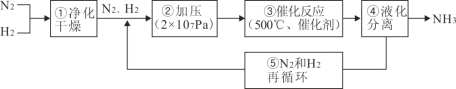
A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.产品液氨除可生产化肥外,还可用作制冷剂
D.步骤③、④、⑤均有利于提高原料平衡的转化率
高三化学单选题简单题
如图所示为工业合成氨的流程图。有关说法不正确的是( )

A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.产品液氨除可生产化肥外,还可用作制冷剂
D.步骤③、④、⑤均有利于提高原料平衡的转化率
高三化学单选题简单题
如图所示为工业合成氨的流程图。有关说法不正确的是( )

A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.产品液氨除可生产化肥外,还可用作制冷剂
D.步骤③、④、⑤均有利于提高原料平衡的转化率
高三化学单选题简单题查看答案及解析
下图所示为工业合成氨的流程图。有关说法错误的是
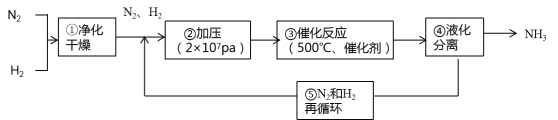
A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C. 步骤③、④、⑤均有利于提高原料的转化率
D. 产品液氨除可生产化肥外,还可用作制冷剂
高三化学单选题简单题查看答案及解析
下图所示为工业合成氨的流程图。有关说法错误的是
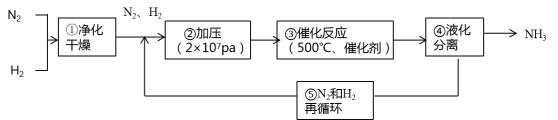
A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C. 步骤③、④、⑤均有利于提高原料的转化率
D. 产品液氨除可生产化肥外,还可用作制冷剂
高三化学单选题简单题查看答案及解析
下图所示为工业合成氨的流程图。有关说法错误的是
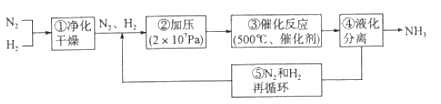
A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C. 步骤③、④、⑤均有利于提高原料平衡的转化率
D. 产品液氨除可生产化肥外,还可用作制冷剂
高三化学单选题简单题查看答案及解析
下图所示为工业合成氨的流程图。有关说法错误的是
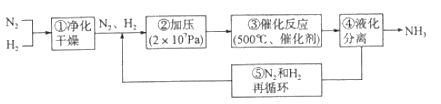
A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C. 步骤③、④、⑤均有利于提高原料平衡的转化率
D. 产品液氨除可生产化肥外,还可用作制冷剂
高三化学单选题简单题查看答案及解析
氨是制造化肥的重要原料,如图为工业合成氨的流程图。下列有关说法错误的是

A.工业上制氮气一般用分离液态空气法
B.步骤②、③、④、⑤均有利于提高反应物的平衡转化率
C.步骤①中“净化”N2、H2混合气体可以防止催化剂中毒
D.步骤③中温度选择500℃,主要是考虑催化剂的活性
高三化学单选题中等难度题查看答案及解析
下列在有关工业生产的主要设备中采取的措施能达到相应目的的是( )
| 选项 | 化学工业 | 主要设备 | 措施 | 目的 |
| A. | 合成氨 | 合成塔 | 500℃左右 | 防止催化剂中毒 |
| B. | 电解食盐水 | 电解槽 | 石棉隔膜 | 防止氯气和氢氧化钠反应 |
| C. | 接触法制硫酸 | 接触室 | 五氧化二钒 | 提高二氧化硫的转化率 |
| D. | 侯式制碱 | 沉淀池 | 先通氨气,再通二氧化碳 | 有利于二氧化碳的吸收 |
A.A B.B C.C D.D
高三化学多选题中等难度题查看答案及解析
1923年以前,甲醇一般是用木材或其废料的分解蒸馏来生产的。现在工业上合成甲醇几乎全部采用一氧化碳或二氧化碳加压催化加氢的方法,工艺过程包括造气、合成净化、甲醇合成和粗甲醇精馏等工序。
已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
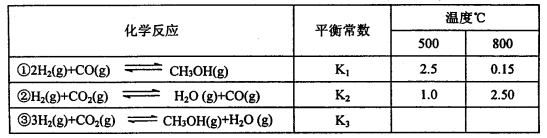
(1)反应②是____________(填“吸热”或“放热”)反应。
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如下图所示。则平衡状态由A变到B时,平衡常数K(A)_____K(B)(填“>”、“<”或“=”)。
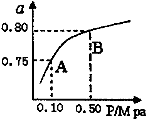
据反应①与②可推导出K1、K2与K3之间的关系,则K3=_________(用K1、K2表示
(3)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如下图所示,若在t0时刻分别改变一个条件,则曲线Ⅰ可变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_____________。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是________。
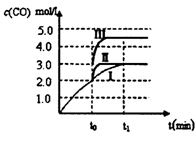
(4)甲醇燃料电池有着广泛的用途,若采用铂为电极材料,两极上分别通入甲醇和氧气,
以氢氧化钾溶液为电解质溶液,则该碱性燃料电池的负极反应式是_________________;
(5)一定条件下甲醇与一氧化碳反应可以合成醋酸。通常状况下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为_____________。
高三化学简答题中等难度题查看答案及解析
氮的固定意义重大,氮肥的使用大面积提高了粮食产量。人工固氮最有效的方法是合成氦,一种工业合成氨的简易流程如图所示(净化、后期处理等流程未列出):
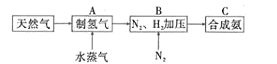
回答下列问题:
Ⅰ.步骤A制氢气的原理之一是CH4(g)+2H2O(g)⇌CO2(g)+4H2(g) ∆H=a kJ/mol
(1)已知:H2、CH4的燃烧热分别为285.8kJ/mol、890.31k/mol;H2O(g)⇌H2O(l) ∆H=-44kJ/mol则a=____kJ/mol。
(2)在密闭容器中,既能加快反应速率,又一定能提高平衡体系中H2体积分数的措施是_____(填序号)。
a.加入催化剂 b.升高温度 c.降低压强 d.增大c(H2O)
Ⅱ.步骤B完成了原料气准备后,通过步骤C合成氨,其原理为N2(g)+3H2(g)2NH3(g) ∆H=-92.4kJ/mol。
(3)若T℃下,向一个容积为2L的真空密闭容器中(有催化剂)通入lmol N2、3mol H2,1分钟后达到化学平衡状态,测得容器内的压强是开始时的0.8倍。则:
①下列叙述可说明该反应已经达到化学平衡状态的是______(填序号)。
a.3v(H2)正=2v(NH3)逆 b.混合气体的平均相对分子质量不再发生改变
c.混合气体的密度不再发生改变 d. 1个N≡N键断裂的同时有3个H—H键生成
②t分钟内v(H2)=_______。
③T℃下该反应的K=___________(列出计算式即可)。
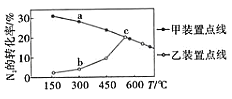
④一定条件下,向体积相同的甲(含催化剂)、乙两个容器中分别充入等物质的量的N2和等物质的量的H2进行合成氨反应,均反应1小时、测得N2的转化率随温度变化如图所示,a、b、c三点中达到化学平衡状态的点有_________,乙装置中N2转化率随着温度的升高先升后降的原因可能是______。
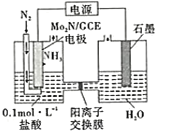
(4)我国科学家成功研制出一种高效电催化固氮催化剂Mo2N,其固氮原理如图所示,该装置中,阴极上的电极反应式为______。
高三化学综合题困难题查看答案及解析
合成氨工业中的原料气制取与净化是重要的环节。
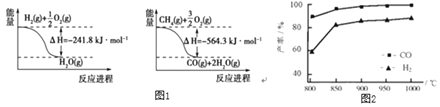
(1)已知有关反应的能量变化如图1:写出与
反应制取
和
的热化学方程式:______。
(2)“催化重整法”制氢气:
,
不仅可以得到合成气
和
,还对温室气体的减排具有重要意义。上述反应中相关的化学键键能数据如表所示。
①根据键能计算,该反应的______
。
| 化学键 | C-H | C=O | H-H | |
| 键能kJ/mol | 413 | 745 | 436 | 1075 |
②按一定体积比加入和
,在恒压下发生反应,温度对CO和
产率的影响如图2所示。实际生产中此反应优选温度为900℃,原因是______。
③某温度下,将、
以及催化剂进行加入
容器中,达到平衡时
,平衡常数
______
。
(3)合成气在进入合成塔前常用醋酸二氨合铜Ⅰ
溶液来吸收其中的CO杂质,其反应是:
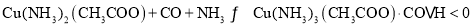 ,必须除去原料气中CO的原因是______。醋酸二氨合铜
,必须除去原料气中CO的原因是______。醋酸二氨合铜Ⅰ
吸收CO的生产适宜条件应是______
填序号
。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
高三化学综合题中等难度题查看答案及解析