汽车尾气含有烃类、CO、NO、SO2等物质,是城市空气的主要污染源。在汽车排气管上加装"催化转化器"可使CO和NO反应生成无毒气体。下列说法错误的是( )
A.CO和NO反应的化学方程式为:2CO + 2NO 2CO2 + N2
B.此法的缺点是由于CO2的增多会大大提高空气的酸度
C.汽车改用天然气为燃料或用氢气为能源,可减少对空气的污染
D.CO和NO均可与人体血红蛋白结合而使人中毒
高三化学单选题中等难度题
汽车尾气含有烃类、CO、NO、SO2等物质,是城市空气的主要污染源。在汽车排气管上加装"催化转化器"可使CO和NO反应生成无毒气体。下列说法错误的是( )
A.CO和NO反应的化学方程式为:2CO + 2NO 2CO2 + N2
B.此法的缺点是由于CO2的增多会大大提高空气的酸度
C.汽车改用天然气为燃料或用氢气为能源,可减少对空气的污染
D.CO和NO均可与人体血红蛋白结合而使人中毒
高三化学单选题中等难度题
汽车尾气含有烃类、CO、NO、SO2等物质,是城市空气的主要污染源。在汽车排气管上加装"催化转化器"可使CO和NO反应生成无毒气体。下列说法错误的是( )
A.CO和NO反应的化学方程式为:2CO + 2NO 2CO2 + N2
B.此法的缺点是由于CO2的增多会大大提高空气的酸度
C.汽车改用天然气为燃料或用氢气为能源,可减少对空气的污染
D.CO和NO均可与人体血红蛋白结合而使人中毒
高三化学单选题中等难度题查看答案及解析
汽车尾气(含有烃类、CO、NOx、SO2等)是城市空气的主要污染源,治理方法之一是在汽车排气管安装“催化转化装置器”。它能使CO和NOx反应生成可参与大气生态环境循环的无毒气体,并使烃类充分燃烧、SO2转化。下列说法中正确的是( )
A.CO和NOx反应的化学方程式为2xCO+2NOx===2xCO2+N2
B.上述方法的缺点是导致空气中CO2的含量增大,从而大大提高空气的酸度
C.植树造林,增大绿化面积,能从根本上控制城市的各种污染源
D.汽车改用天然气或氢气作为燃料,不会减少对空气的污染
高三化学选择题简单题查看答案及解析
高三化学选择题中等难度题查看答案及解析
(11分)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源之一。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式:
________________________________________________________________________。
(2)“催化转换器”的缺点是在一定程度上提高了空气的酸度,其原因是______________。
(3)控制城市空气污染源的方法可以有___________________________________(填字母序号)。
A.开发氢能源 B.使用电动车 C.植树造林 D.戴上呼吸面具
高三化学填空题简单题查看答案及解析
(7分)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1) 写出一氧化碳与一氧化氮反应的化学方程式:________。
(2) “催化转化器”的缺点是在一定程度上提高空气的酸度,其原因是________
________。
(3) 控制城市污染源的方法可以有________(多选扣分)
A. 开发氢能源 B. 使用电动车 C. 植树造林 D. 戴上呼吸面具
高三化学填空题简单题查看答案及解析
高三化学解答题中等难度题查看答案及解析
(5分)汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,反应原理:2NO(g)+2CO(g)===N2(g)+2CO2(g),在298 K、100 kPa下,ΔH=-113 kJ·mol-1,ΔS=-145 J·(mol·K)-1.
(1)为了提高该反应的速率和NO的转化率,采取的正确措施为________
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N2
D.降低温度同时增大压强
(2)若升高温度,则该反应的平衡常数________ (填“增大”、“减小”或“不变”).
(3)判断该条件下反应(填能、不能)自发.
高三化学填空题简单题查看答案及解析
汽车尾气排放的CO、NOx等气体是大气污染的主要来源,NOx也是雾霾天气的主要成因之一。
i.在汽车排气管加装催化转化器,可有效降低污染物的浓度,发生反应:2NO(g)+2CO(g)N2(g)+2CO2(g)△H<0。为了模拟催化转化器的工作原理,在t℃时,将2molNO与1mol CO充入1L反应容器中,反应过程中NO(g)、CO(g)、N2(g)的物质的量变化如图所示,
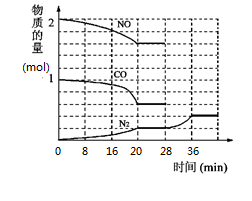
(1)①则反应进行到20min时,CO2的平均反应速率为________________.
②28min~36min内NO、CO、N2的物质的量发生了变化(NO、CO图像未画出),引起该变化的条件可能是______.
a.加入催化剂 b.通入0.2mol N2
c.缩小容器体积 d.增加CO2的物质的量
③当36min达到平衡后,若保持体系温度为t℃,再向容器中充入CO、CO2气体,使两者物质的量浓度均加倍,平衡将__________移动(填“向左”、“向右”或“不”)
(2)若均取2molNO和1molCO的混合气体分别放入3种不同的容器中进行该反应,A容器保持恒温恒压,B容器保持恒温恒容,C容器保持恒容绝热,且初始时3个容器的容积和温度均相同,下列说法正确的是______.
a.3个容器中NO的平衡转化率的大小顺序为 aA>aB>aC.
b.当A容器内气体的平均摩尔质量不变时,说明该反应处于化学平衡状态
c.A、B两个容器达到平衡所用的时间:tA>tB
d.当C容器内平衡常数不变时,说明该反应处于化学平衡状态
ii. 某温度下,NO2(g)+SO2(g)⇌SO3(g)+NO(g)的平衡常数K=,该温度下在甲、乙、丙三个体积为2L的恒容密闭容器中,投入NO2(g)和SO2(g),其起始浓度如表所示,
| 起始浓度 | 甲 | 乙 | 丙 |
| c(NO2)/mol•L﹣1 | 0.10 | 0.20 | 0.20 |
| c(SO2)/mol•L﹣1 | 0.10 | 0.10 | 0.20 |
(3)①10min后,甲中达到平衡,则甲中NO2的转化率α(NO2)=_______________.
②达到平衡后,设甲、乙、丙中SO2(g)的转化率分别为a、b、c,则三者的大小关系为_____________.
(4)利用反应NO2+NH3→N2+H2O(未配平)消除NO2的简易装置如图所示。
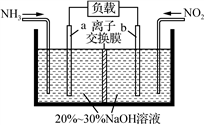
电极b的电极反应式为__________________;常温下,若用该电池电解0.6L饱和食盐水,消耗标准状况下448mL NH3时, 发现两极产生相同体积的气体,则此时溶液的PH=____(假设电解过程溶液体积不变)。
高三化学简答题中等难度题查看答案及解析
为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① ∆H=180.5kJ·
∆H=180.5kJ·
②C和CO的燃烧热(∆H)分别为-393.5kJ·和-283kJ·
则2NO(g)+2CO(g)=N2(g)+2CO2(g) ∆H=_________kJ·
(2)将0.20molNO和0.10molCO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
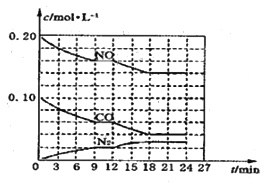
①CO在0—9min内的平均反应速率=__________ mol·L-1·
(保留两位有效数字);第12min时改变的反应条件可能为_________。
A.升高温度 B.加入NO
C.加催化剂 D.降低温度
②该反应在第18min时又达到平衡状态,此时的体积分数为________(保留三位有效数字),化学平衡常数K=____________(保留两位有效数字)。
(3)通过人工光合作用能将水与燃煤产生的转化为HCOOH和
。已知常温下0.1mol·
的HCOONa溶液pH=10,则HCOOH的电离常数Ka=__________。
高三化学填空题中等难度题查看答案及解析
(15分)为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
②C和CO的燃烧热(△H)分别为-393.5kJ·mol-1和-283kJ·mol-1
则2NO(g+2CO(g)=N2(g)+2CO2(g)) △H= kJ·mol-1
(2)将0.20 mol NO和0.10 mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
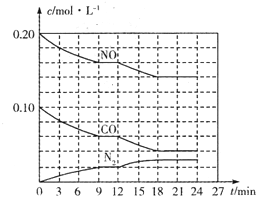
①CO在0-9min内的平均反应速率v(CO)=________mol(保留两位有效数字);第12 min时改变的反应条件可能为________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24 min时达到平衡状态,CO2的体积分数为________(保留三位有效数字),化学平衡常数K=________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收得到Na2SO3和NaHSO3混合溶液,且所得溶液呈中性,该溶液中c(Na+)=________(用含硫微粒浓度的代数式表示)。
(4)通过人工光合作用能将水与燃煤产生的CO2转化成HCOOH和O2。已知常温下0.1 mol的HCOONa溶液pH =10,则HCOOH的电离常数
=_________。
高三化学填空题困难题查看答案及解析